Biotrasformazione o Metabolismo dei tossici: assorbimento e detossificazione
Slide da Piccin Ed. su Biotrasformazione o Metabolismo. Il Pdf, utile per l'Università in Biologia, illustra i processi di biotrasformazione e metabolismo dei tossici, con focus su assorbimento, distribuzione e detossificazione, esaminando percorsi metabolici di benzene, paracetamolo e aflatossina B1.
Mostra di più35 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
BIOTRASFORMAZIONE O METABOLISMO
ESPOSIZIONE AL TOSSICO
- ASSORBIMENTO (entrata) TOSSICO nel plasma
- DISTRIBUZIONE Tossico nei tessuti
- METABOLISMO Biotrasformazione dei tox in metaboliti polari che possono essere eliminati attraverso le urine
BIOTRASFORMAZIONE (METABOLISMO) - TOSSIFICAZIONE E DETOSSIFICAZIONE
Il metabolismo può: - AUMENTARE - DIMINUIRE -ABOLIRE le proprietà tossiche di un composto
SCOPO della biotrasformazione
- mantenimento della composizione fisiologica del mezzo intra- ed extracellulare
- trasformazione in molecole più polari, perciò più idrosolubili e facilmente eliminabili
IMPORTANZA DELLO STUDIO DELLE BIOTRASFORMAZIONI IN TOSSICOLOGIA
- evidenziare la presenza di metaboliti attivi, inattivi, tossici
- prevedere interferenze con altri xenobiotici
- prevedere variazioni di risposta in seguito ad assunzione protratta (INDUZIONE E REPRESSIONE ENZIMATICA)
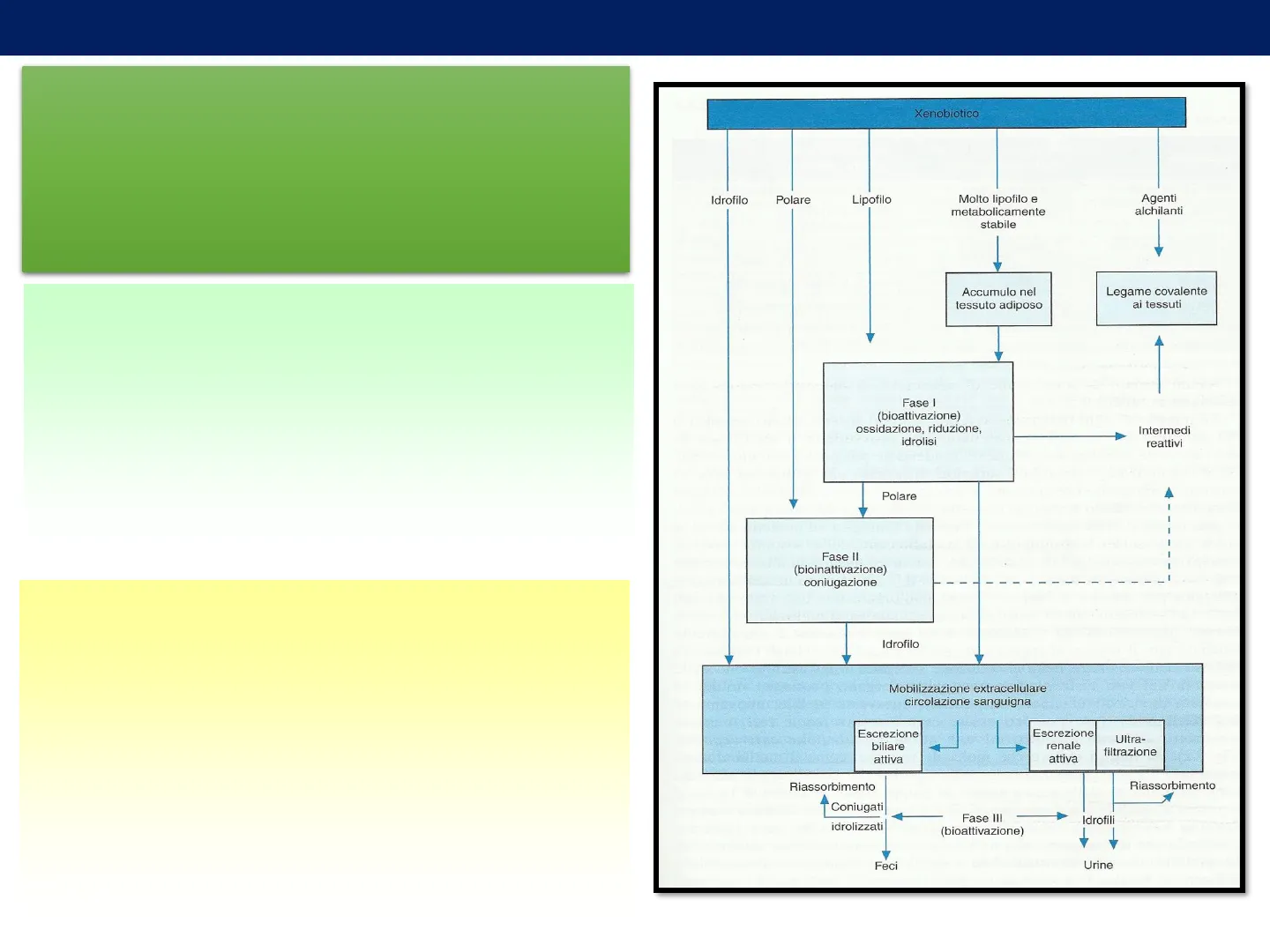
Xenobiotico Idrofilo Polare Lipofilo Molto lipofilo e metabolicamente stabile - Agenti alchilanti Accumulo nel tessuto adiposo Legame covalente ai tessuti
Fase I (bioattivazione)
ossidazione, riduzione, idrolisi Intermedi reattivi Polare
Fase II (bioinattivazione)
coniugazione Idrofilo Mobilizzazione extracellulare circolazione sanguigna Escrezione biliare attiva Escrezione renale attiva Ultra- filtrazione Riassorbimento Riassorbimento Coniugati idrolizzati Idrofili
Fase III (bioattivazione)
Feci Urine Tossicologia - Galli - Corsini - Marinovich - Piccin Ed.
SITI DI BIOTRASFORMAZIONE
FEGATO POLMONE RENE TRATTO G.I.
Attività metabolizzante dei vari organi rispetto al fegato
FEGATO 100% POLMONE 20-30% RENE 8% INTESTINO 6% PLACENTA (a termine) 5% CUTE 1%
Enzimi
- bassa specificità di substrato, scarsa efficienza catalitica
- elevato numero, notevole ubiquità
BIOTRASFORMAZIONE O METABOLISMO
TOSSICO
FASE I
Ossidazione, Riduzione e/o idrolisi In seguito alla Fase I il tox può risultare attivato, immodificato o, nella maggior parte dei casi, inattivato
FASE II
Prodotti di coniugazione Il F. coniugato solitamente è inattivo
CYP3A 50% CYP2D6 25% 5% CYP2C9 15% 5% Other J. Perkins MS, MFA CYP1A2
IN SEGUITO ALLE BIOTRASFORMAZIONI GLI XENOBIOTICI POSSONO AVERE DIVERSI DESTINI:
- essere escreti invariati (es. etere etilico)
- essere attivati o inattivati (es. glucosidi antrachinonici-> antrachinoni, es. codeina -> morfina)
- essere trasformati in metaboliti tossici
BIOTRASFORMAZIONE O METABOLISMO
METABOLISMO PRESISTEMICO
Intestino Fegato (primo passaggio) Limita molto la disponibilita' di composti ingeriti
METABOLISMO SISTEMICO
circolo enteroepatico Sangue Tessuti Arteria epatica Vena epatica Fegato Glucuronidation Dotto biliare Farmaco Vena porta Farmaco-coniugato Bglucuronidase Intestino
BIOTRASFORMAZIONE O METABOLISMO
METABOLISMO PRESISTEMICO
Intestino Fegato (primo passaggio) Limita molto la disponibilità di composti ingeriti
METABOLISMO SISTEMICO
Sangue Tessuti
BIOTRASFORMAZIONE O METABOLISMO
Localizzazione ENZIMI
Extracellulare (salvaguardia cellule) Intracellulare Mitocondriali Microsomiali Citoplasmatici
All'interno della cellula la maggiore attività metabolica è localizzata nucleo involucro nucleare. nucleolo nucleoplasma microtubuli membrana plasmatica coppia di centrioli Reticolo endoplasmatico microsomi citoplasma vescicola lisosoma apparato di Golgi reticolo endoplasmico liscio reticolo endoplasmico mitocondrio rugoso
Le reazioni di biotrasformazione possono avvenire anche nei mitocondri o a livello della membrana nucleare o plasmatica
Le sostanze liposolubili (in grado di permeare più facilmente all'interno della cellula) sono più soggette a biotrasformazione
BIOTRASFORMAZIONE O METABOLISMO
FASE I
esposizione/aggiunta di gruppi funzionali accumulo tissutale metaboliti assenza di biotrasformazione XENOBIOTICO eliminazione metaboliti eliminazione
FASE II
coniugazione
Tabella 3.2 - Esempi di conversione di xenobiotici a prodotti tossici
Sostanza Reazione di biotrasformazione Metabolita tossico (effetto tossico) Amine aromatiche N-idrossilazione Idrossilamina (cancerogena) Anilina N-idrossilazione N-idrossianilina (metaemoglobina) Idrocarburi aromatici Epossidazione Derivati epossidico policiclici (teratogeno cancerogeni) Metanolo Ossidazione alcolica Acido formico (retinopatia) Isoniazide Acetilazione e idrolisi Acetilidrazina (epatotossica) Paracetamolo N-idrossilazione N-idrossiacetaminofene (epatotossico) da: Tossicologia - Galli - Corsini - Marinovich - Piccin Ed.
BIOTRASFORMAZIONE O METABOLISMO
Fase I Fase II sostanza attiva metabolita primario metabolita secondario coniugato lipofilo eliminazione biliare idrofilo eliminazione renale
BIOTRASFORMAZIONE O METABOLISMO
Reazioni di fase 1
REAZIONI DELLA FASE I PORTANO ALL'INTRODUZIONE O LIBERAZIONE DI UN GRUPPO POLARE (idrofilo)
- ossidazioni (es. alcool) ADH R-C=0 ALDH R-C=0 R-CH2OH < 1 1 H OH V + + + + NAD NADH + H NAD + H2O NADH + H Figura 6-23. Ossidazione degli alcoli ad aldeidi e ad acidi carbossilici da parte dell'alcol deidrogenasi (ADH) e dell'aldeide deidrogenasi (ALDH).
- riduzioni (es. riduzione di ponti S-S dell'a-bungarotossina)
- idrolisi (composti di natura esterea, peptidica, glicosidica)
BIOTRASFORMAZIONE O METABOLISMO
Reazioni di fase 2
TRASFERISCONO SUBSTRATI ENDOGENI (attivati, con dispendio di energia) SULLA MOLECOLA DEL TOX O DEI SUOI METABOLITI
- coniugazioni con - ac. glucuronico, ac. solforico, ac. acetico ES: (alcoli aromatici e alifatici -> O-glucuronidi ( amine aromatiche e alifatiche ) -> N-glucuronidi (gruppi SH) -> S-glucuronidi N.B. presenza di beta-glucuronidasi a livello intestinale - metionina, glicina, cisteina (fenoli, tioli, eterocicli) - glutatione reazione tra gruppo SH nucleofilo del glutatione e gruppi elettrofili ↓ previene legame covalente con costituenti vitali cellulari Es: epossidi - danno DNA
BIOTRASFORMAZIONE O METABOLISMO
Tabella 6-1 Vie di biotrasformazione degli xenobiotici e loro principale localizzazione subcellulare
REAZIONE ENZIMA O REAZIONE SPECIFICA LOCALIZZAZIONE Idrolisi Carbossil esterasi Microsomi, citosol, lisosomi, sangue Epossido idrolasi Microsomi, citosol Fosfatasi alcalina Membrana plasmatica Peptidasi Sangue, lisosomi Riduzione Dealogenazione riduttiva Microsomi Deidrogenasi di diidropirimidine Citosol Deidrossilazione (citocromo b5) Microsomi Deidrossilazione (aldeide ossidasi) Citosol Riduzione di azo- e di nitro-gruppi Flora microbica intestinale Riduzione di chinoni Citosol, microsomi Riduzione di gruppi carbonilici (aldo-cheto) Citosol, sangue, microsomi Riduzione di gruppi disolfuro Citosol Riduzione di gruppi solfossido Citosol Ossidazione Alcol deidrogenasi Citosol Aldeide deidrogenasi Mitocondri, citosol Aldeide ossidasi Citosol Citocromo P450 Microsomi Diamino ossidasi Citosol Monoamino ossidasi Mitocondri Monoossigenasi flaviniche Microsomi Perossidasi Microsomi, lisosomi, saliva Xantina ossidasi Citosol Coniugazione Aminoacil trasferasi Citosol, microsomi, mitocondri Glutatione trasferasi Citosol, microsomi, sangue Metil trasferasi Mitocondri, citosol N-Acetil trasferasi Citosol Solfo trasferasi Microsomi UDP-glucuronosil trasferasi Mitocondri, microsomi da: Casarett & Doull - Tossicologia - EMSI ed.
CLASSIFICAZIONE DEI CYP450
superfamiglia CYP Famiglie (identità < 40%) CYP1 CYP2 CYP3 etc. Sottofamiglie (identità 40-50%) CYP1A CYP1B CYP1C etc. Membri (identità > 55%) CYP1A1 CYP1A2 CYP1A3 etc etc. Negli animali superiori il numero di P450 espressi è dell'ordine di 50-80. Nel genoma umano sono presenti 57 geni codificanti P450 e 19 pseudogeni La forma ridotta del citP450 lega monossido di carbonio (CO). Questa forma dà un massimo di assorbimento a 450 nm 2 = 450 nm max Absorbance 400 450 500 Wavelength (nm)
BIOTRASFORMAZIONE O METABOLISMO
SISTEMA MICROSOMIALE EPATICO
SISTEMA DI OSSIDASI A FUNZIONE MISTA (complesso del cit P450) (REAZIONI DELLA FASE I)
- citocromo P450 (proteina-eme che esiste in diverse isoforme)
- NADPH-citocromo P450-reduttasi NADP+ NADPH Flavoproteina (ridotta) Flavoproteina (ossidata) 2 e- AH. P450-Fe2+ 3 RH- P450-Fe3+ O2 RH P450-Fe2+ H2O 02 1 4 P450-Fe3+ R-H (farmaco originario) R-OH (prodotto ossidato) Figura 4-3. Cicio del citocromo P450 nella ossidazione dei far- maci (RH = farmaco originario; ROH = metabolita ossidato; e = elettrone). Lume Membrana R E 333 Citoplasma CYP NADPH × e NADPH-CYP- Reduttasi XOH O2 H2O Metabolita inattivo Metabolita reattivo Figura 3.4 - Localizzazione subcellulare eu attività del citocromo P-450; dei due atomi che costituiscono la molecola di O2, un atomo è inserito sullo xenobiotico (X), mentre l'altro viene ridotto a formare una molecola di H2O. da: Tossicologia - Galli - Corsini - Marinovich - Piccin Ed.
Citocromi P450 microsomiali
Adenine Ribose Phosphate Cytochrome P450 Reductase Phosphate Ribitol N N 1e NADPH H3C- HỌC N CNC N-FOND N N N O CNC N N c - N 0 N -- Fet-N C_N_C Cytochrome P450 Benzo[a]pyrene Benzo[a]pyrene-7,8-dihydrodiol-9,10-epoxide HO OH P450 P450 O2 epoxide hydrolase HO OH Benzo[a]pyrene-7,8-epoxide Benzo[a]pyrene-7,8-dihydrodiol Cytochrome b5 2e" O Phosphate Ribitol [FAD] H3C H3C 1e- C [FMN] O2 Esempio di reazione catalizzata da citocromi P450: Biotrasformazione del benzopirene
INDUZIONE ENZIMATICA
L'esposizione ripetuta ad alcuni farmaci ed inquinanti ambientali, è in grado di "indurre" il citocromo P450
Meccanismi di induzione enzimatica
- aumento trascrizione del DNA
- aumento traduzione mRNA a proteine
- stabilizzazione mRNA
- stabilizzazione delle proteine
INDUZIONE ENZIMATICA
INDUZIONE FARMACO-METABOLICA
PREVALENTEMENTE A CARICO DEL CIT P450 EPATICO
- STIMOLAZIONE DELLA SINTESI DEGLI ENZIMI DI BIOTRASFORMAZIONE
- PROLIFERAZIONE DEL RETICOLO ENDOPLASMATICO
- AUMENTO DEL PESO DEL FEGATO
L'induzione di enzimi di biotrasformazione è un processo adattativo recettore mediato (xenosensori), che consente di aumentare la velocità di eliminazione degli xenobiotici in momenti o situazioni in cui il livello di esposizione alla sostanza è particolarmente elevato . L'induzione produce un'accelerazione del metabolismo. L'induzione spesso non comporta alcun cambiamento nella velocità di biotrasformazione dello stesso induttore