Introducción a la Química: Estructura Atómica y Enlaces
Documento de Universidad sobre Introducción a la Química: Estructura Atómica y Enlaces. El Pdf explora la materia y los átomos, números cuánticos, tabla periódica y formación de enlaces químicos. Es un material de Química para estudiantes universitarios.
Ver más30 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Introducción a la Química
Conceptos Fundamentales del Átomo
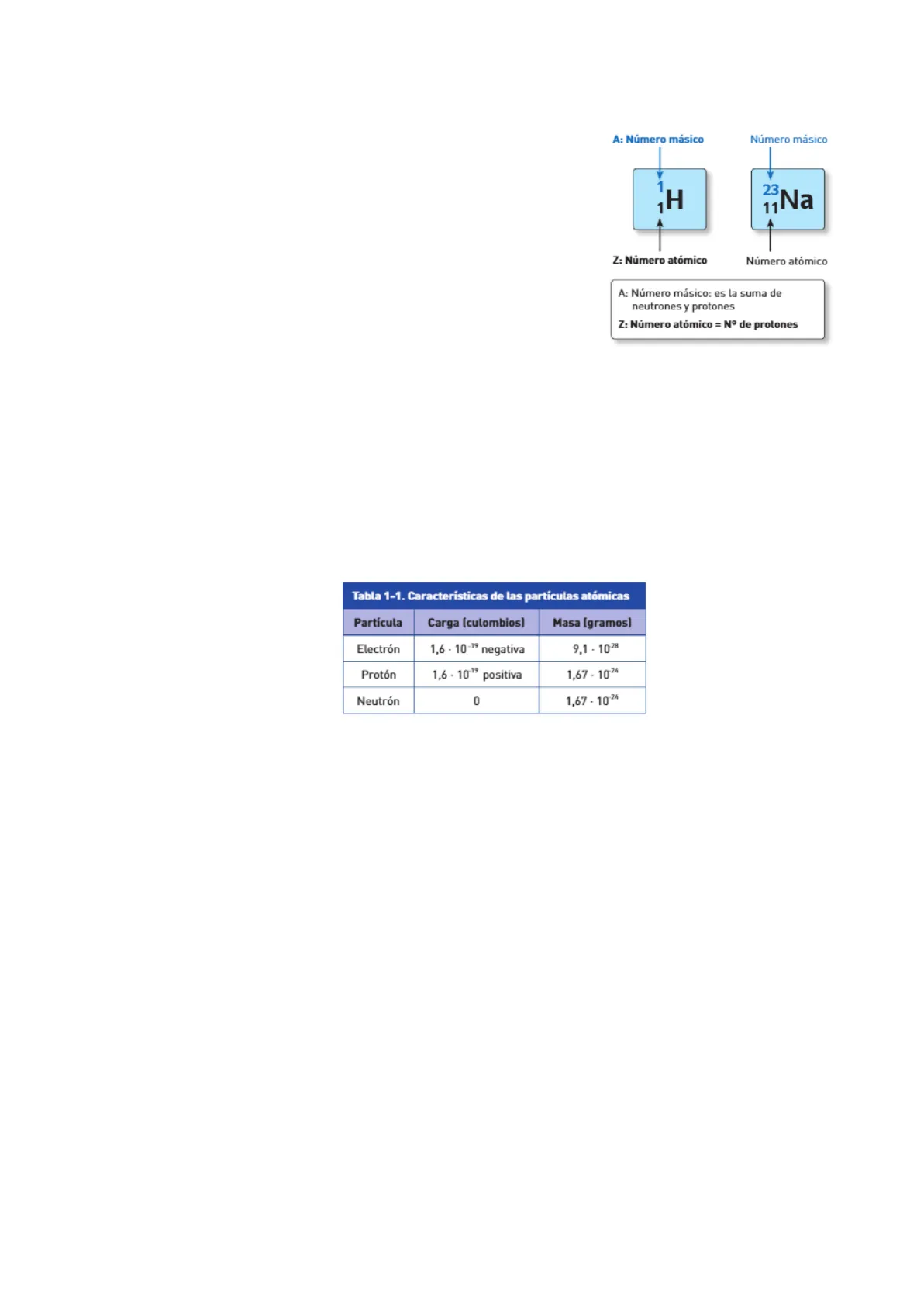
- Numero atomico: protones
- Numero masico: suma de protones y neutrones
- Isotopo:Un isótopo es una variante de un elemento químico que tiene el mismo número de protones (y por tanto el mismo número atómico) pero diferente número de neutrones en el núcleo. (tienen propiedades químicas muy similares, ya que el número de protones (que determina el comportamiento químico) no cambia, pero pueden tener diferentes propiedades físicas, como una masa atómica distinta.)
A: Número másico Número másico 1 ¡H 23 11 Na 4 Z: Numero atomico Número atómico A: Número másico: es la suma de neutrones y protones Z: Número atómico = Nº de protones
La Materia y los Átomos
- Los átomos son las unidades fundamentales de la materia y están compuestos por tres partículas subatómicas: protones, neutrones y electrones.
- En la tabla, se muestran las características de estas partículas: su carga (positiva para los protones, negativa para los electrones, y neutra para los neutrones) y sus masas.
Tabla 1-1. Características de las partículas atómicas
Partícula Carga (culombios) Masa (gramos) Electrón 1,6 - 10-19 negativa 9,1 - 1028 Proton 1,6 - 101 positiva 1,67 - 102 Neutron 0 1,67 - 10:24
- Normalmente, los átomos son neutros, ya que tienen el mismo número de protones y electrones. Sin embargo, si pierden o ganan electrones, se convierten en iones. Si pierden electrones, se vuelven cationes (positivos) y, si ganan electrones, se vuelven aniones (negativos).
Ubicación de las Partículas Atómicas
- Los protones y neutrones están en el núcleo, concentrando casi toda la masa del átomo.
- Los electrones se encuentran en los orbitales alrededor del núcleo, definidos por números cuánticos.
Número Atómico e Isótopos
- Cada elemento se identifica por su número atómico (Z), que es la cantidad de protones en el núcleo.
- Un mismo elemento puede tener diferentes cantidades de neutrones, lo que da lugar a isótopos, que son variantes del mismo elemento con diferentes masas.Órbitas y números cuánticos:
Órbitas y Números Cuánticos
- Los electrones se encuentran en áreas específicas llamadas orbitales atómicos, donde existe la mayor probabilidad de encontrarlos.
- Estos orbitales se definen por conjuntos de cuatro números
cuánticos, que determinan su energía y posición.
- numero cuantico principal: (N) tamaño y energia del orbital (se detomina 1,2 ,3 ... )
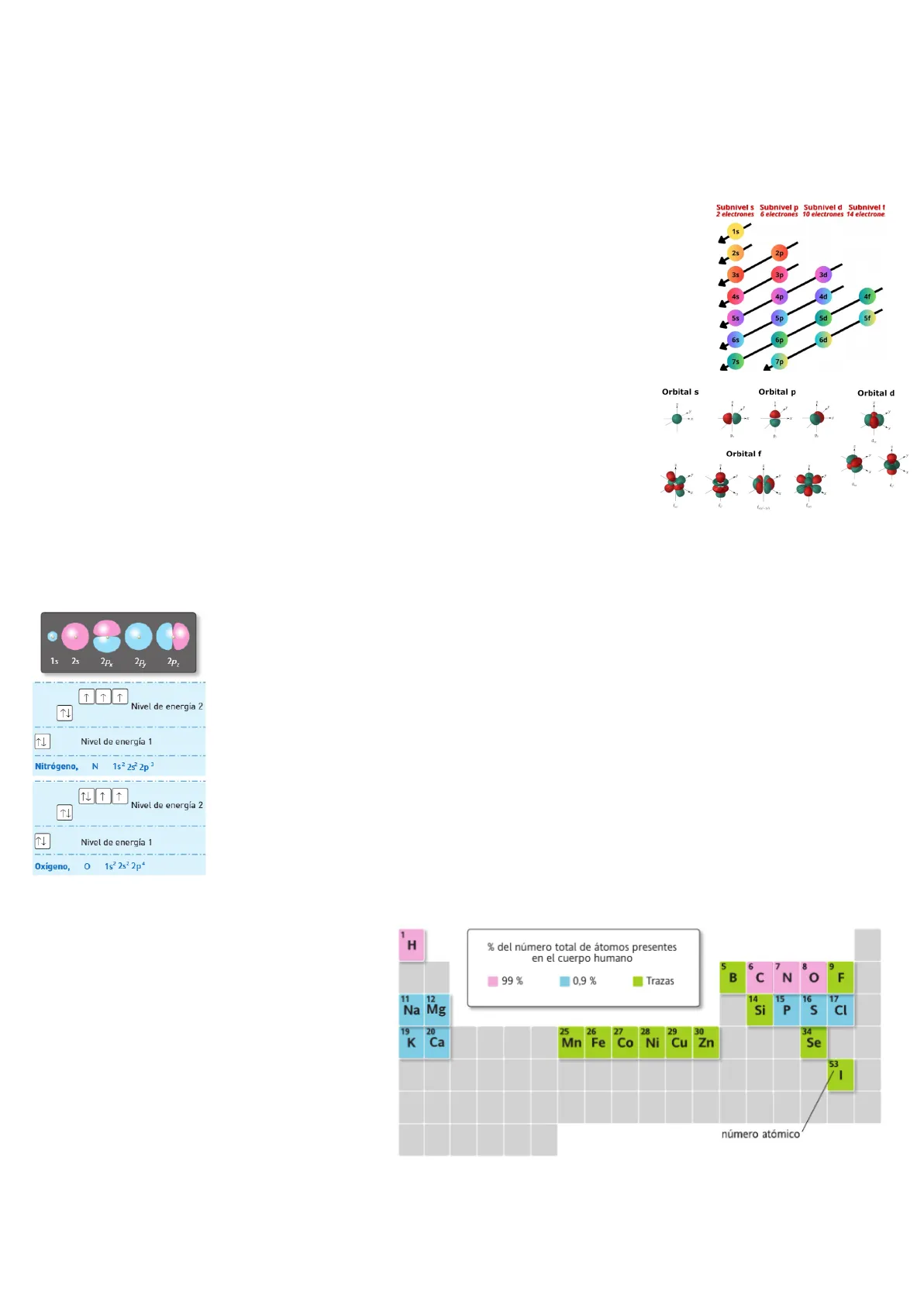
- Numero cuantico azimutal (L): Define la forma (se denominan s,p, d y f) S: esférico y capacidad de 2 electrones P: ovalada y capacidad de 6 electrones D: ovalado y capacidad de 10 electrones F: ovalado y capacidad de 14 electrones
- Numero cuantico magnetico (m)) : define la orientacion en el espacio (Se denominan x, y, z)
- Numero espin: (Ms): momento angular intrinseco del electron ( ayudan a diferenciar entre electrones que están en el mismo orbital. ) +2/1: espín "arriba" (1) -1/2: espín "abajo" (I)
Debido a la dificultad de dibujar los orbitales atomicos se usa la configuracion electronica que va de mayor numero de electrones a menor. Por ejemplo: N: 7 electrones. 1s2 2s2 2p3 1s2: El número "1" representa el nivel de energía (el más cercano al núcleo del átomo). La letra "s" representa el tipo de orbital (en este caso, "s" puede contener hasta 2 electrones), y el superíndice "2" indica que hay 2 electrones en este orbital. 2s2: Ahora estamos en el segundo nivel de energía (2), también en un orbital s, que tiene 2 electrones. 2p3: Seguimos en el segundo nivel de energía (2), pero ahora en un orbital tipo p. Los orbitales p pueden contener hasta 6 electrones en total, pero aquí solo hay 3 electrones (de ahí el "3").
Tabla Periódica
- En la tabla periódica se ordenan los elementos de izquierda a derecha según aumenta su numero de protones y por lo tanto también de electrones (si es un átomo neutro)
- C , Ny O: elementos fundamentales que constituyen las células
- H: 1 electron 1S1
- C: 6 electrones 1s2 2s2 2p2
- N: 7 electrones 1s2 2s2 2p3
- O: 8 electrones 1s2 2s2 2p4
1 H % del número total de átomos presentes en el cuerpo humano 5 6 7 8 9 B C N O F 99 % 0,9 % Trazas 11 12 14 15 16 17 Na Mg Si P S Cl 19 20 25 26 27 28 29 30 34 K Ca Mn Fe Co Ni Cu Zn Se 53 número atómico 1 1 Nivel de energía 2 Nivel de energía 1 Nitrógeno, N 1s2 23 2p 3 TL Nivel de energía 2 Nivel de energía 1 Oxígeno, 0 1s2 2s2 2p4 Subnivel s Subnivel p Subnivel d Subnivel f 2 electrones 6 electrones 10 electrones 14 electrone: 15 2s 2p 35 3p 3d 45 4p 4d 4f 55 5p 5d Sf 6s 6p 6d 7s 7p Orbital s Orbital p Orbital d Pr Orbital f d 1s 2s 2p 2P 2Pz3 Capitulo 1. Bases de la bioquímica. Video 1
Períodos y Grupos de la Tabla Periódica
- Los elementos están organizados en
- períodos (filas horizontales.Cada período representa un nuevo nivel de energía donde pueden ubicarse los electrones.)
- grupos (columnas verticales. Los elementos en el mismo grupo tienen propiedades químicas similares debido a que tienen el mismo número de electrones de valencia.).
Grupos de Elementos
- Grupo 1: Metales Alcalinos
- Elementos: Sodio (Na), Potasio (K)
- Características: Muy reactivos, especialmente con el agua; tienen un electrón de valencia.
- Grupo 2: Metales Alcalinoterreos
- Elementos Magnesio (Mg), Calcio (Ca)
- Características: Reactivos, aunque menos que los metales alcalinos; tienen dos electrones de valencia.
- Grupo 3-12: Metales de Transición
- Elementos: hierro (Fe), cobre (Cu), níquel (Ni), zinc (Zn), manganeso (Mn), cobalto (Co)
- Características: Tienen propiedades metálicas; son buenos conductores de electricidad; pueden formar compuestos de múltiples estados de oxidación. Tienen entre 1-2 electrones en su capa más externa.
- Grupo 13: Metales Térreos
- Elementos: Boro (B)
- Características: Contienen tres electrones de valencia; el aluminio es muy conocido por su uso en la industria.
- Grupo 14: Carbonoideos
- Elementos: Carbono (C), Silicio (Si)
- Características:tienen cuatro electrones de valencia.
- Grupo 15: Nitrogenos
- Elementos: Nitrógeno (N), Fósforo (P).
- Características: Tienen cinco electrones de valencia; el nitrógeno es un componente clave del aire.
- Grupo 16: Calcogenos
- Elementos: Oxígeno (O), Azufre (S), Selenio (Se),
- Características: Tienen seis electrones de valencia; el oxígeno es vital para la respiración.
- Grupo 17: Halógenos
- Elementos: Flúor (F), Cloro (CI), Yodo (I).
- Características: Muy reactivos; tienen siete electrones de valencia y forman sales cuando reaccionan con metales.
Distribución de Electrones
- Cada círculo alrededor del núcleo muestra el nivel de energía donde están ubicados los electrones.
- En el primer nivel (más cercano al núcleo), caben hasta 2 electrones; en el segundo nivel caben hasta 8.
- Por ejemplo, el carbono (C) tiene 2 electrones en el primer nivel y 4 en el segundo, mientras que el oxígeno (O) tiene 2 en el primer nivel y 6 en el segundo.
Número de Electrones de Valencia
- El último nivel de cada átomo contiene los electrones de valencia, que son importantes para las reacciones químicas y la formación de enlaces
- La valencia de un elemento químico es su capacidad de combinación, representada por un dígito que indica el número de enlaces que puede formar en un compuesto.
- A medida que te mueves hacia la derecha en un período, el número de electrones de valencia aumenta, lo que a su vez afecta la reactividad.
- Por ejemplo,: El carbono (C) tiene una valencia de cuatro, lo que significa que puede formar hasta cuatro enlaces con otros átomos ..
Formación de Moléculas
- Los átomos tienden a asociarse para formar moléculas o agregados atómicos.
- Ejemplos:
- Moléculas diatómicas: Dos átomos iguales, como la molécula de oxígeno (O2).
- Compuestos: Moléculas que contienen átomos de diferentes elementos, como el agua (H2O).Regla del Octeto:
Regla del Octeto
- Propuesta por Lewis, establece que los átomos son más estables cuando tienen ocho electrones en su capa de valencia. Por lo que para crear enlaces para tener 8 electrones de valencia (excepto el hidrógeno que solo necesitan 2)
VÍDEO 1-2 Átomo Número de electrones no apareados (en rojo] Número de electrones en la capa externa completa ¿Cómo se forman las moléculas? H· 1 2 H . + H. - H:H - H-H Dihidrógeno :0. 2 8 :0. + 2 H· H H IN- 3 8 + 3 H . H :N:H H - N-H Amoniaco H H 4 8 + 4 H. - Н:C:H H = H-C-H Metano H 2 8 :Š· + 2 H . :S:H H S-H Sulfuro de hidrógeno H :0: OH : P. 3 8 3 H. + :P. + 4 .0: - > =P:Q:H = = P-OH :0 OH O-H :O:H = Agua H H Ácido fosfórico
Electronegatividad y Formación de Enlaces
- Los átomos que tengan más números de electrones en su última capa son más electronegativos ( los de la izquierda de la tabla periódica)
- Los átomos con alta electronegatividad tienden a atraer electrones compartidos en un enlace.
ELECTRONEGATIVIDAD He B C N O E Ne 2,0 2,5 3,0 3,5 4.0 Si P CI Ar 1,5 1,8 2,1 2,5 3,0 Ge As Se Br Kr 0,8 1,0 1,3 1,5 1,6 1,6 1,5 1,8 1,9 1,9 1,6 1,6 1,8 2,0 2,4 2,8 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te Xe 0,8 1,0 1,2 1,4 1,6 1,8 1,9 2,2 2,2 2,2 1,9 1,7 1,7 1,8 1,9 2,1 2,5 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg TI Pb Bi Po At Rn 0,7 0,9 1,0 1,3 1,5 1,7 1,9 2,2 2,2 2,2 2,4 1,9 1,8 1,9 1,9 2,0 2,1 baja media alta Zn Ga Ca Sc Ti V Cr Mn Fe Co Ni Cu Be 1,0 1,6 Na Mg Al S 0,9 1,2 H 2,1 Li K 1,9 I
Configuración Electrónica y Reactividad
- La configuración electrónica de un elemento determina su reactividad. Los electrones de valencia (electrones en la última capa) son los que participan en reacciones químicas.
- La configuración electrónica es la forma en que están organizados los electrones
en una molécula.
- Estado Basal: Cuando los electrones tienen la mínima energía posible, se dice que la molécula está en su estado basal o fundamental.
- Estado Excitado: Si los electrones tienen más energía (por ejemplo, si absorben energía), la molécula se encuentra en un estado excitado.
Tipos de Enlace
- Los enlaces iónicos, como en la sal de mesa (NaCI), ocurren cuando hay una gran diferencia de electronegatividad, lo que provoca la transferencia completa de electrones y la formación de iones.
- Enlaces covalentes:Los enlaces covalentes son un tipo de enlace químico en el
cual dos átomos comparten uno o más pares de electrones para lograr una
configuración electrónica más estable, generalmente acercándose a completar sus
capas de electrones
- Apolar: Los electrones se comparten de manera igualitaria entre los átomos, porque sus electronegatividades son iguales o muy similares. Ejemplo: H2, O2.
- Polar: Los electrones se comparten de forma desigual debido a una diferencia en la electronegatividad de los átomos. Esto crea una distribución de carga parcial, donde un átomo tiene una carga parcial negativa (ō-) y el otro, una carga parcial positiva (ō+). Ejemplo: el agua (H2O), donde el oxígeno es más electronegativo que el hidrógeno.
Orbital Molecular: Cuando dos átomos se unen, sus orbitales atómicos (los lugares donde se encuentran los electrones) se combinan para formar un orbital molecular. Este orbital determina cómo se comportará la unión.
- Orbital Enlazante: Si el nuevo orbital tiene menor energía que los orbitales originales, la unión se fortalece y se dice que es un orbital enlazante.
- Orbital Antienlazante: Si el nuevo orbital tiene mayor energía, puede debilitar la unión y se llama orbital antienlazante. Este tipo de orbital no favorece la formación del enlace.
Enlace Covalente Coordinado (o Dativo)
- En un enlace covalente coordinado, un átomo aporta ambos electrones para formar el enlace, mientras que el otro átomo sólo proporciona un orbital vacío.
- Como resultado, el átomo que no aporta electrones puede tener una carga positiva porque tiene más protones que electrones, mientras que el otro átomo recibe los electrones para completar su unión.
Electrones forman enlace coordinado con el proton H I- + H-N :- >H+ H-N-H - H H ion amonio