Le Leggi Ponderali: teoria atomica e principio di Avogadro in Chimica
Slide di Scuola superiore sulle Leggi Ponderali. Il Pdf esplora le leggi ponderali, la teoria atomica e il principio di Avogadro, spiegando come gli atomi si combinano e come calcolare la massa atomica e molecolare, con definizioni chiave e tabelle di riferimento.
Mostra di più19 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
La materia è costituita da atomi
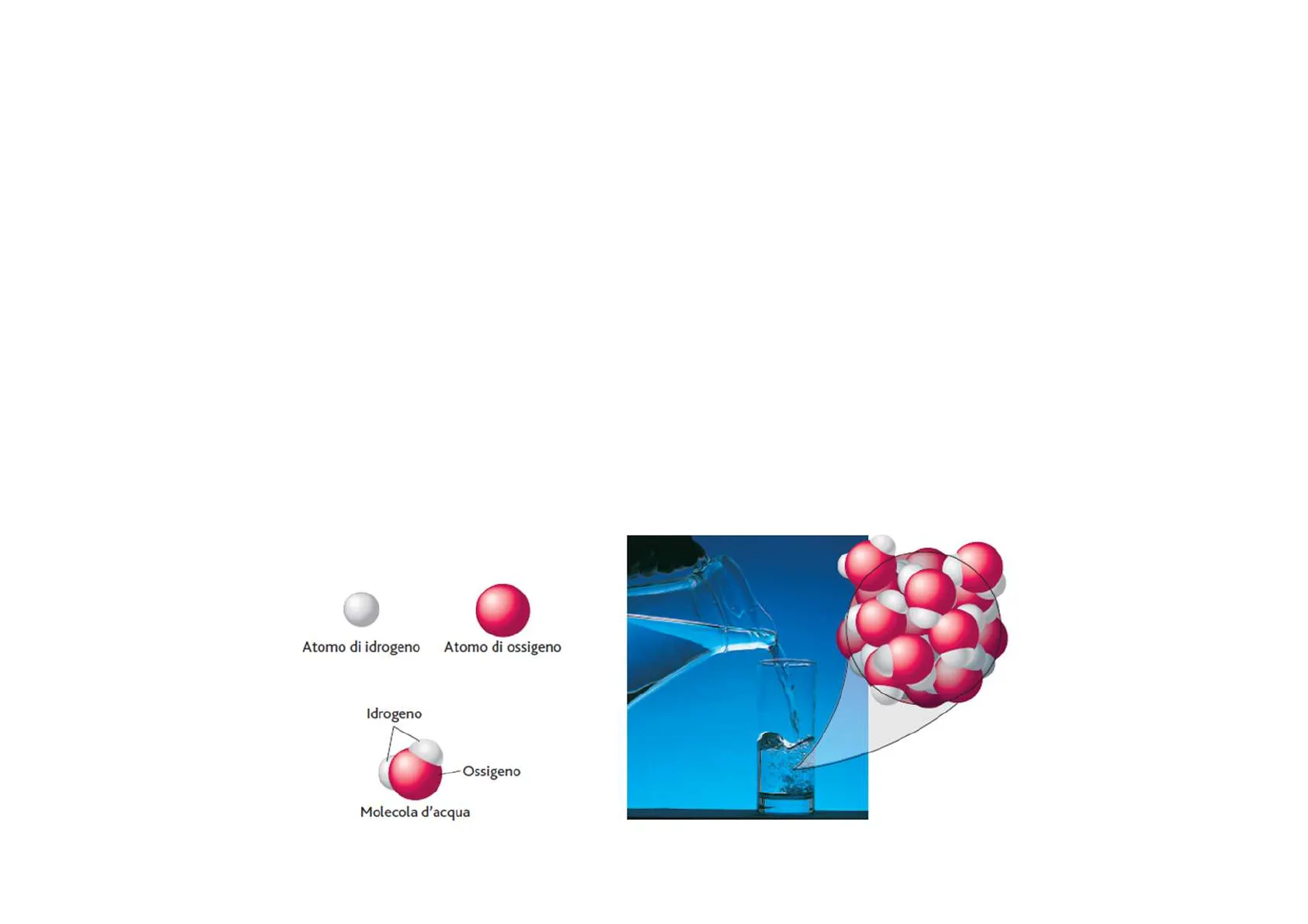
La teoria atomica sostiene che tutte le sostanze chimiche sono costituite da particelle minuscole chiamate atomi. I singoli atomi si combinano tra loro in vari modi per formare particelle più complesse, le molecole. Moltissime sostanze chimiche che troviamo nel nostro ambiente sono costituite da atomi di vario tipo, combinati in proporzioni specifiche.
Atomo di idrogeno e ossigeno
Atomo di idrogeno Atomo di ossigeno Idrogeno Ossigeno Molecola d'acqua
Le leggi ponderali: legge di Lavoisier
L'esistenza degli atomi fu dimostrata attraverso le leggi ponderali: Legge della conservazione della massa o legge di Lavoisier: in una reazione chimica, la massa dei reagenti è esattamente uguale a quella dei prodotti
Principio di conservazione della massa
In una reazione chimica, la massa si conserva perché il numero e la na- tura degli atomi restano inalterati: la somma delle masse del sodio e del cloro è uguale alla massa totale del cloruro di sodio che si forma. sodio cloro cloruro di sodio + 23 g + 35,4 g 58,4 g + 11,5 g + 17,7 g 29,2 g Antoine-Laurent Lavoisier (1743-1794).
Le leggi ponderali: legge di Proust
Legge delle proporzioni definite o legge di Proust: in un composto, il rapporto tra le masse degli elementi che lo costituiscono è definito costante.
Rapporto tra le masse di cloro e sodio
Il rapporto tra le masse di cloro e di sodio è definito e costan- te: un atomo di cloro si combina sempre con uno di sodio e ogni atomo di cloro ha una massa 1,54 volte maggiore di quella di ogni atomo di sodio. massa cloro massa sodio =1,54 Joseph Proust 1754-1826
La teoria atomica di Dalton
John Dalton (1766- 1844)
- La materia è costituita da minuscole particelle chiamate atomi.
- Gli atomi sono indivisibili. Nelle reazioni chimiche essi rimangono inalterati e non si «rompono» in frazioni più piccole.
- Tutti gli atomi di un elemento puro sono identici tra loro sia per la massa sia per le altre proprietà.
- Gli atomi di elementi diversi hanno massa e proprietà differenti.
- Quando gli atomi di elementi diversi si combinano per formare i composti, si formano particelle nuove e più complesse. Gli atomi che le costituiscono, tuttavia, sono sempre combinati in un rapporto numerico definito.
Le leggi ponderali: legge di Dalton
Legge delle proporzioni multiple o legge di Dalton: quando due elementi si combinano tra loro per formare composti diversi, le quantità di uno di essi che si combinano con una quantità fissa dell'altro, stanno fra loro in rapporti semplici esprimibili mediante numeri interi e piccoli.
Esempi di proporzioni multiple
1°caso + carbonio ossigeno ossido di carbonio CO: con 12 g di carbonio si legano 16 g di ossigeno 2ºcaso + carbonio anidride carbonica ossigeno CO2: con 12 g di carbonio si trovano legati 32 g di ossigeno Il rapporto tra le masse di O nei 2 composti è di 2:1 Rapporto tra le masse: 16g:12g=1,33 Rapporto tra le masse: 32g:12g=2,66 Rapporto tra le 2 masse 2,66:1,33=2
Atomi e molecole
Gli elementi sono costituiti da atomi che hanno identiche proprietà chimiche. La molecola è un raggruppamento di due o più atomi che possiede proprietà chimiche caratteristiche. Esistono molecole formate da atomi dello stesso tipo come le molecole diatomiche. Ha O2 N2 Cl2 12 Altre molecole sono formate anche da più di due atomi dello stesso tipo. S8 P4
Formule delle molecole
La formula di una molecola indica da quali elementi essa è costituita e quanti atomi di ciascun elemento essa contiene. CH4 NH3 CO2 molecola di metano molecola di ammoniaca molecola di diossido di carbonio La formula che utilizziamo per indicare quali e quanti atomi costituiscono la molecola di un composto è chiamata formula bruta o grezza.
Gli ioni
La materia non è costituita soltanto da atomi e da molecole, molte sostanze sono costituite da particelle cariche elettricamente : gli ioni.
- Gli ioni carichi positivamente (per esempio, Na+) si chiamano cationi.
- Gli ioni carichi negativamente (per esempio, CI-) si chiamano anioni.
Composti ionici
I composti ionici (come i sali) sono formati da cationi e anioni. catione Na+ + + I + + 1 + + + + anione CI-
La massa atomica
Dalton compilò la prima tabella delle masse atomiche degli elementi conosciuti, prendendo come riferimento l'atomo di H: la massa così espressa è detta massa atomica relativa. Le masse atomiche proposte da Dalton risultarono errate nella maggior parte dei casi perché Dalton partiva dal presupposto che la molecola d'acqua avesse formula HO, cioè che l'O fosse otto volte più pesante dell'H. Fu grazie alla distinzione fra atomi e molecole proposta da Stanislao Canizzaro (in base agli studi già compiuti nel 1811 da Amedeo Avogadro) che si arrivò alla corretta determinazione della massa degli atomi.
Il principio di Avogadro
Amedeo Avogadro intuì che gli elementi allo stato gassoso non sono costituiti da singoli atomi ma da molecole biatomiche e formulò la legge o principio di Avogadro: volumi uguali di gas diversi, nelle stesse condizioni di pressione e temperatura, contengono lo stesso numero di molecole (non di atomi). + = 1 volume di H2 1 volume di Cl2 2 volumi di HCl
La massa atomica: correzione di Cannizzaro
Cannizzaro utilizzò il principio di Avogadro per correggere le masse atomiche relative 1 litro O2 = 1,43 g 1 litro H2 = 0,089 g 1,43 massa O2 massa H2 = = 16 0,089 Il rapporto tra le masse di 1L di O2 e 1L di H2 è 16, quindi la massa di un atomo di O è 16 volte la massa di un atomo di H
La massa atomica: riferimento attuale
Oggi per misurare la massa atomica non si usa più come riferimento l'H, ma l'isotopo 12 del carbonio, indicato con 12C. L'unità di massa atomica (u) è la dodicesima parte (1/12) della massa dell'isotopo 12C. La massa atomica relativa, MA, di un elemento è la sua massa espressa in unità u, ed il valore di ogni elemento è riportato sulla tavola periodica. La MA è chiamata anche peso atomico.
Pesi atomici di alcuni elementi
Pesi atomici di alcuni elementi Elemento Peso atomico H idrogeno 1,008 Li litio 6,941 Na sodio 22,99 K potassio 39,10 Be berillio 9,012 Mg magnesio 24,31 Ca calcio 40,08 B boro 10,81 Al alluminio 26,98 C carbonio 12,01 Si silicio 28,09 N azoto 14,01 P fosforo 30,97
Massa molecolare relativa e peso formula
La massa molecolare relativa, MM o peso molecolare, è la somma delle masse atomiche che compaiono nella molecola. Per i composti ionici la massa molecolare relativa si calcola allo stesso modo ma prende il nome di peso formula. Es. MMCH4= MAc + 4MAH = 12,01u+4(1,008)u= 16,042 u
Contare per moli
Il valore dell'unità di massa atomica, 1 u = 1,661 · 10-24 g, è estremamente piccolo per essere misurato con gli strumenti. È stato perciò necessario trovare una grandezza che mettesse in relazione gli atomi e le molecole con le grandezze misurabili con le bilance: la mole (mol). Una mole è la quantità di sostanza che contiene un numero di particelle elementari uguali al numero di atomi contenuti in 12 g di 12C. La massa di una mole di un elemento (o di una molecola) è uguale alla sua massa atomica (o molecolare) espressa in grammi/mole. La massa molare M che si misura in g/mol, è la massa di una mole. grafite (C) mercurio (Hg) zolfo (S) rame (Cu) zinco (Zn) etanolo (CH3CH2OH) 00 : 1 acqua (H2O) 194 dicromato di potassio (K2Cr2O7) 40 solfato di rame pentaidrato (CuSO4 . 5 H2O) 20 0 cloruro di sodio (NaCl)
Numero di Avogadro
Avogadro si pose il problema di quante particelle elementari fossero contenute in una mole e lo risolse tramite il rapporto: massa molare/massa atomica = 6,022 . 1023 particelle/mol Il risultato di questo rapporto è noto come numero o costante di Avogadro. Una mole di sostanza contiene sempre 6,022 · 1023 particelle (atomi, molecole o ioni). C + 02 - CO2 MONDO MICROSCOPICO 1 atomo MA =12 u 1 molecola MM=32 u 1 molecola MM=44 u xN = 6,02 × 1023 x N = 6,02 × 1023 x N = 6,02 × 1023 MONDO MACROSCOPICO 1 mole di atomi 12 g 1 mole di molecole 1 mole di molecole 44 g 32 g
Calcoli con le moli
In pratica, per calcolare il numero di moli di una sostanza si usa la formula: massa del campione (g) m numero di moli n = M massa molare (g/mol) massa molare (g/mol) massa del campione (g) m = n . M numero di moli (mol) numero di particelle N numero di moli (mol) n =- NA costante di Avogadro (particelle/mol)
Esempio di calcolo delle moli
Esempio: Calcola il numero di moli contenute in 38,2 g di glucosio, C6H1206. SOLUZIONE Innanzitutto occorre calcolare la massa molare del glucosio. Siccome la massa molecolare vale: MMC6H1206 = 6 · 12,01 u + 12 · 1,008 u + 6 · 16,00 u = 180,16 u la sua massa molare equivale a MCGH1206 = 180,16 g/mol A questo punto è possibile calcolare il numero di moli: 38,2 g n = 180,16 g/mol = 0,212 mol
Composizione percentuale
La composizione percentuale è utile per determinare la massa effettiva di un elemento presente in una data massa di composto.
Esempio di calcolo della composizione percentuale
Esempio: Calcola la composizione percentuale degli elementi nel fluoruro di calcio, CaFz- SOLUZIONE Dopo aver calcolato il peso formula del fluoruro di calcio, un composto ionico, MMcaf2 = 40,08 u + 2 - 19,00 u = 78,08 u si imposta la seguente proporzione per determinare le percentuali di composizione dei singoli ele- menti: MAca : MM Caf2 = X: 100 40,08 u : 78,08 u = x : 100 % Ca = 78,08 u 40,08 u - 100 = 51,33% di calcio La percentuale di fluoro può essere calcolata come differenza al 100%: % F = 100% - % Ca = 100 - 51,33 = 48,67% di fluoro
La formula minima
La formula minima indica il rapporto di combinazione minimo con cui gli atomi si legano per formare la molecola.
Passaggi per determinare la formula minima
I passaggi per determinare la formula minima sono i seguenti:
- si scrive la massa m in grammi di ciascun elemento presente in 100 g di composto, cioè la sua percentuale in massa;
- si calcola il numero di moli n di ciascun elemento dividendo la massa m (g) per la sua massa molare M (g/mol);
- si divide il numero di moli di ciascun elemento per il più piccolo numero di moli calcolato: i numeri interi che si ottengono sono gli indici numerici della formula;
- si scrivono gli elementi e in basso a destra di ciascuno il rispettivo indice.
Esempio di calcolo della formula minima
COMPOSTO 37,5% C C H 50,0% 12,5% Elementi Massa in 100 g di composto Numero di moli Rapporto tra le moli Formula minima H 12,5% 12,5 g = 12,4 mol =4 1,008 g/mol 3,12 mol C 37,5% 37,5 g = 3,12 mol = 1 CH4O 12,01 g/mol 3,12 mol O 50,0% 50,0 g 50,0 g 16,00 g/mol = 3,13 mol 3,13 mol =1 3,12 mol 12,4 mol 12,5 g 3,12 mol 37,5 g