Reacciones Químicas: Fundamentos y Disoluciones, Ies Mutxamel
Diapositivas de Ies Mutxamel sobre Reacciones Químicas: Fundamentos y Disoluciones. El Pdf es una presentación didáctica de Bachillerato de Química que aborda los fundamentos teóricos y las disoluciones, incluyendo definiciones, esquemas y problemas resueltos para el estudio autónomo.
Ver más24 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Fundamentos Teóricos de Reacciones Químicas
Reacciones y Ecuaciones Químicas
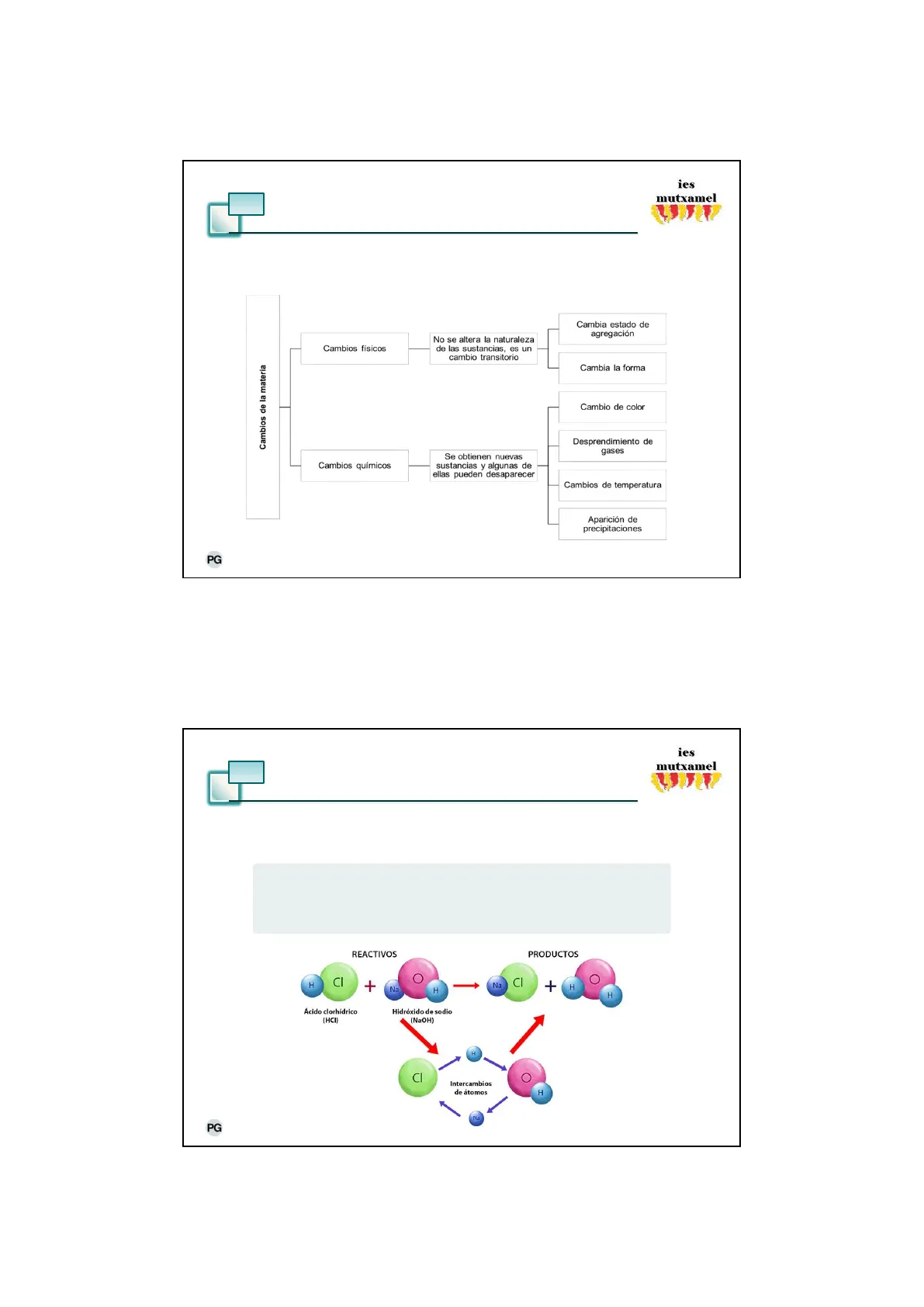
Reacciones Químicas: Cambios Físicos y Químicos
02/02/2025 TEMA 5.1. REACCIONES QUÍMICAS FUNDAMENTOS Y DISOLUCIONES Química Patricia Gisbert de Ves ies mutxamel Curso 2024/2025 GENERALITAT VALENCIANA Conselleris d'Educació, Investigació, Cultura i Esport Cofinanciado por el programa Erasmus+ de la Union Europea Unión Europea A. FUNDAMENTOS TEÓRICOS 102/02/2025 ies mutxamel 1. Reacciones y ecuaciones químicas 1.1. Reacciones químicas Cambia estado de agregación Cambios físicos No se altera la naturaleza de las sustancias, es un cambio transitorio Cambia la forma Cambios de la materia Cambio de color Desprendimiento de gases Cambios químicos Se obtienen nuevas sustancias y algunas de ellas pueden desaparecer Cambios de temperatura Aparición de precipitaciones 3 PG TEMA 5.1. Reacciones químicas
Definición de Reacción Química
ies mutxamel 1. Reacciones y ecuaciones químicas 1.1. Reacciones químicas Una reacción química, es todo proceso termodinámico en el cual dos o más especies químicas o sustancias (reactivos), se transforman, cambiando su estructura molecular y sus enlaces, en otras sustancias llamadas productos. REACTIVOS PRODUCTOS CI + Na H H Ácido clorhídrico (HCI) Hidróxido de sodio (NaOH) H CI Intercambios de átomos H Na PG TEMA 5.1. Reacciones quimicas 4 Na CI H + H
Mecanismo de una Reacción Química: Colisiones
202/02/2025 ies mutxamel 1. Reacciones y ecuaciones químicas 1.1. Reacciones químicas - Mecanismo de una reacción química CHOQUE NO EFICAZ I I I CHOQUE EFICAZ H I Las reacciones tienen lugar por las colisiones entre moléculas (en gas o en disolución). Se define la frecuencia de colisiones, como (n.º colisiones / t): v œc (n.º colisiones / s) Para que la colisión entre reactivos, sea efectiva y de lugar a la formación de productos, debe tener la orientación adecuada y energía suficiente. PG TEMA 5.1. Reacciones químicas 5
Ecuación Química
Representación y Contenido de una Ecuación Química
ies mutxamel 1. Reacciones y ecuaciones químicas 1.2. Ecuación química ¿Qué son? Representación de una reacción química y debe contener: Todos los reactivos y productos Las condiciones de la reacción El estado físico de las sustancias CO + 3H, CH4 + H,0 En reactivos En los productos PG TEMA 5.1. Reacciones químicas 6
Símbolos Utilizados en Ecuaciones Químicas
302/02/2025 ies mutxamel 1. Reacciones y ecuaciones químicas 1.2. Ecuación química Símbolos utilizados en las ecuaciones Símbolo Significado (s) Indica el estado sólido (1) Indica el estado líquido (g) Indica el estado gaseoso (ac) Identifica disuelto en agua. + Reacciona con Separa reactivos de productos -> Reacción reversible Desprendimiento de Gas Precipitación de solido Agregar calor 7 PG TEMA 5.1. Reacciones químicas
Información de la Ecuación Química: Combustión del Metano
ies mutxamel 1. Reacciones y ecuaciones químicas 1.2. Ecuación química Combustión del metano: + + CH4 + 202 - CO2 + 2H2O ¿Qué información obtenemos de la ecuación química? Cada molécula de metano (CH4) requiere 2 moléculas de oxígeno (O2) para reaccionar Cada molécula de metano (CH4) genera 1 molécula de dióxido de carbono (CO2) y 2 moléculas de agua (H2O) PG TEMA 5.1. Reacciones químicas 8
Mecanismo de una Reacción Química: Teoría de Colisiones
402/02/2025 ies mutxamel 1. Reacciones y ecuaciones químicas 1.2. Ecuación química - Mecanismo de una reacción química CHOQUE NO EFICAZ I 1 I CHOQUE EFICAZ 1 Explicamos la reacción mediante la Teoría de Colisiones Las reacciones tienen lugar por las colisiones entre moléculas (en gas o en disolución). Se define la frecuencia de colisiones, como (n.º colisiones / t): v œc (n.º colisiones / s) Para que la colisión entre reactivos, sea efectiva y de lugar a la formación de productos, debe tener la orientación adecuada y energía suficiente. PG TEMA 5.1. Reacciones químicas 9
Nivel Molecular y Energía de Activación
1. Reacciones y ecuaciones químicas 1.2. Ecuación química - Mecanismo de una reacción química ¿QUÉ OCURRE A NIVEL MOLECULAR? Para que un choque sea eficaz y se formen los productos debe cumplirse: -La energía ha de ser suficiente para que se rompan los enlaces. A la energía mínima para que ocurra la reacción se la conoce como Energía de Activación (Ea) 4 aA + bB + C + dD energia de activación Estado de tramición Energía de Activación Entalpía Reactivos Calor de Reacción diferencia de energia entre reactivos y productos Productos Coordenada de reacción Si las moléculas no alcanzan la energía de activación la reacción no tiene lugar PG TEMA 5.1. Reacciones químicas 10
Ajuste de Ecuaciones Químicas
Método de Tanteo y Conservación de la Masa
5 ies mutxamel A02/02/2025 ies mutxamel 1. Reacciones y ecuaciones químicas 1.3. Ajuste de ecuaciones química Método de tanteo + + CH4 + 202 CO2 + 2H20 Las ecuaciones químicas deben estar ajustadas, de forma que se cumpla la ley de conservación de la masa. Debe haber el mismo número de átomos de cada elemento a ambos lados de la ecuación, en los reactivos y en los productos. PG TEMA 5.1. Reacciones químicas 11
Ejemplo de Ecuación Ajustada
ies mutxamel 1. Reacciones y ecuaciones químicas 1.3. Ajuste de ecuaciones química CH3CH2OH + O2 -CO2 + H2O No ajustada + + 8 + + Ajustada CH3CH2OH + 3O2 2CO2 + 3H2O PG TEMA 5.1. Reacciones químicas 12
Ejercicios de Ajuste de Reacciones Químicas
602/02/2025 ies mutxamel 1. Reacciones y ecuaciones químicas 1.3. Ajuste de ecuaciones química Ejemplo: Ajusta las siguientes reacciones químicas a) H2 + Cl2 -> HCI b) H2SO4 + KOH -> K2SO4 + H2O c) K2CrO4 + AgNO3 -> Ag2CrO4 + KNO3 d) H2 + O2 -> H2O2 PG TEMA 5.1. Reacciones químicas 13
Leyes Fundamentales de Química
Ley de Conservación de la Masa
Principio de Lavoisier
ies mutxamel 2. Leyes fundamentales de química 2.1. Ley de conservación de la masa En una reacción química, la suma de las masas de todas las sustancias que intervienen se mantiene constante. En cualquier reacción química, la masa total se conserva Ley de Lavoisier "la masa ni se crea ni se destruye, solo se transforma" PG TEMA 5.1. Reacciones químicas 14
Experimento del Globo Inflado
702/02/2025 ies mutxamel 2. Leyes fundamentales de química 2.1. Ley de conservación de la masa El globo que se infla "solo" En una botella de plastico se añade vinagre hasta aproximadamente un dedo de altura. A continuación, se llena el globo con una cucharada de bicarbonato de sodio y se coloca en la boca de la botella. Se da la vuelta al globo y se observa lo ocurrido. Además, tanto previamente como una vez finalizo el experimento, se pesa la botella de plástico para saber el incremento de masa. Preguntas: -¿ Qué ha ocurrido? Bicarbonato Vinagre -¿ Qué compuesto se ha formado? -¿ Por qué ha cambiado o no ha cambiado la masa de la botella? PG TEMA 5.1. Reacciones químicas 15
Tipos de Reacciones Químicas
Clasificación General de Reacciones Químicas
3. Tipos de reacciones químicas 3.1. Clasificación de las reacciones químicas Tipos de reacciones químicas Según partículas Según mecanismo Precipitación Síntesis Ácido-Base - neutralización Descomposición Oxidación-reducción (redox) Desplazamiento Doble desplazamiento PG TEMA 5.1. Reacciones químicas ies mutxamel 16
Reacciones Ácido-Base: Neutralización
Características de Ácidos y Bases
802/02/2025 ies mutxamel 3. Tipos de reacciones químicas 3.2. Reacciones ácido-base: neutralización ÁCIDOS BASES Sabor Ácido Amargo Sensación a la piel Punzante o picante Suaves al tacto Colorantes vegetales (tornasol) Rojo Azul Corrosivos Disuelven grasas. Al tratar grasas Disuelven sustancias Atacan a los metales desprendiendo Precipitan sustancias disueltas por hidrógeno En disolución conducen la corriente En disolución conducen la corriente eléctrica eléctrica Neutralización Pierden sus propiedades al reaccionar con bases Pierden sus propiedades al reaccionar con ácidos Ejemplo de ácido Ejemplo de Base Jugo de limón Sosa Caustica 17 PG TEMA 5.1. Reacciones químicas
Reacción entre Ácidos y Bases
ies mutxamel 3. Tipos de reacciones químicas 3.2. Reacciones ácido-base: neutralización Ácidos y bases fuertes: si tienen mucha tendencia a ceder o aceptar protones, respectivamente. Acidos y bases debiles: si tienen POCA tendencia a ceder o aceptar protones, respectivamente. Reacción entre ácidos y bases HCI NaOH NaCl H,O CI OH CI 0 + + H Na Na H2 Ácido Base Sal Agua Reacción de neutralización PG TEMA 5.1. Reacciones químicas 18 9 Corrosivos animales con álcalis se obtiene el jabón Reactividad ácidos
Escala de pH
Medida de Acidez o Basicidad
02/02/2025 ies mutxamel 3. Tipos de reacciones químicas 3.2. Reacciones ácido-base - Escala de pH El pH es una medida de la acidez o basicidad de una disolución 0 1 2 3 4 5 6 7 8 9 10 11 1213 14 Ácido Neutro Base PG TEMA 5.1. Reacciones químicas 19
Rangos de pH y Disoluciones
ies mutxamel 3. Tipos de reacciones químicas 3.2. Reacciones ácido-base - Escala de pH El pH es una medida de la acidez o basicidad de una disolución Aumenta [H'] y la acidez Aumenta [OH'] y la basicidad 0 1 2 3 4 5 6 7 8 9 10 11 1 12 13 14 Disoluciones ácidas PH < 7 [H'] > 107 mol/L Disolución neutra PH = 7 [H'] = [OH] = 107 mol/L Disoluciones básicas PH > 7 [OH] > 10-7 mol/L Indicadores: sustancias que cambian de color según sea el pH de la disolución a la que se añaden PG TEMA 5.1. Reacciones químicas 20
Reacciones de Combustión
Definición y Componentes
1002/02/2025 ies mutxamel 3. Tipos de reacciones químicas 3.2. Reacciones de combustión La combustión es una reacción redox en la que una sustancia llamada combustible reacciona con oxígeno, denominado comburente, y genera dióxido de carbono y vapor de agua CO2 H20 C.H, + 02 - CO2 + H20 -02 C.H, PG TEMA 5.1. Reacciones químicas 21
Velocidad y Energía de las Reacciones
Factores que Modifican la Velocidad de una Reacción
Rapidez de Reacción
ies mutxamel 4. Velocidad y energía de las reacciones 4.1. Factores que modifican la velocidad de una reacción La velocidad de una reacción es la rapidez con la que se combinan los reactivos o la rapidez con la que se forman los productos + + NO O3 Ineffective collision NO O3 + + NO O3 Effective collision NO2 O2 PG TEMA 5.1. Reacciones químicas 22
Concentración de los Reactivos
1102/02/2025 ies mutxamel 4. Velocidad y energía de las reacciones 4.1. Factores que modifican la velocidad de una reacción Concentracion de los reactivos Un aumento de la concentración de los reactivos implica un aumento de la velocidad de reacción menor concentración mayor concentración menor frecuencia de choques mayorfrecuencia de choques menor velocidad de reacción mayor velocidad de reacción 23 PG TEMA 5.1. Reacciones químicas
Temperatura de la Reacción
ies mutxamel 4. Velocidad y energía de las reacciones 4.1. Factores que modifican la velocidad de una reacción Temperatura de la reacción Experimentalmente, se observa que, en términos generales, la velocidad de la reacción de una reacción química aumenta con la temperatura Aumento de temperatura C Aumento de velocidad de las moléculas 24 PG TEMA 5.1. Reacciones químicas
Grado de División de Reactivos Sólidos
1202/02/2025 ies mutxamel 4. Velocidad y energía de las reacciones 4.1. Factores que modifican la velocidad de una reacción Grado de división de los reactivos sólidos Al aumentar el grado de división de los reactivos sólidos, se facilita el contacto entre los reactivos y, por tanto, el número de choques eficaces Lento Rápido 8 PG TEMA 5.1. Reacciones químicas 25
Presencia de un Catalizador
ies mutxamel 4. Velocidad y energía de las reacciones 4.1. Factores que modifican la velocidad de una reacción Presencia de un catalizador La presencia de un catalizador aumenta la velocidad de la reacción. En cambio, cuando un catalizador disminuye la velocidad de una reacción química se denomina inhibidor O En pequeñas cantidades, aumenta notablemente la velocidad de una reacción. No se consume en la reacción química global recuperándose completamente al final de esta. Energia potencial A+ B A + B sin catalizador C + D catalizador C +D Avance de la reacción Avance de la reacción velocidadcon catalizador > velocidadsin catalizador PG TEMA 5.1. Reacciones químicas E E: Energia potencial 26