Derivados Halogenados y Alcoholes: Clasificación y Reacciones en Química
Documento de Universidad sobre Derivados Halogenados y Alcoholes. El Pdf, de Química, detalla la clasificación, nomenclatura y propiedades físicas de estos compuestos, incluyendo mecanismos de reacción SN1, E1 y SN2, así como reacciones de esterificación y oxidación.
Ver más12 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
DERIVADOS HALOGENADOS
Son compuestos orgánicos en los que uno o más átomos de hidrógeno han sido reemplazados por átomos de halógeno (flúor, cloro, bromo o yodo). Según el tipo de cadena de la que derivan, pueden clasificarse como: Alifáticos, si provienen de alcanos Insaturados, si derivan de alquenos o alquinos
- Aromáticos, si el halógeno está unido a un anillo bencénico
En el caso de los alifáticos, se conocen como haluros de alquilo o haloalcanos. Además, pueden clasificarse según el tipo de carbono al que está unido el halógeno:
- Primarios, si el carbono unido al halógeno está enlazado a un solo grupo alquilo (R)
- Secundarios, si está unido a dos grupos alquilo
- Terciarios, si se une a tres grupos alquilo
POLARIZACIÓN DEL ENLACE C-X
En los grupos funcionales de los derivados halogenados y los alcoholes, aparece un carbono unido a un halógeno (en los primeros) o a un oxígeno (en los segundos). En ambos casos, el enlace covalente entre el carbono y el heteroatomo está polarizado, ya que el halógeno o el oxígeno tienen una electronegatividad mayor que la del carbono. Esta diferencia de electronegatividad provoca que los electrones compartidos se desplacen hacia el átomo más electronegativo, generando una distribución desigual de cargas: el heteroátomo queda con un exceso de densidad electrónica (o) y el carbono con una deficiencia (o+). Esto da lugar a un momento dipolar, cuyo valor depende directamente de la diferencia de electronegatividad entre ambos átomos. Un heteroátomo es cualquier átomo distinto de carbono e hidrógeno que forma parte de una estructura orgánica. En este tema, los heteroátomos más relevantes son los halógenos y el oxígeno. Todos los halógenos comunes (F, Cl, Br, I) son más electronegativos que el carbono, por lo que, al formar enlaces con él, generan un dipolo eléctrico
NOMENCLATURA Y CLASIFICACIÓN
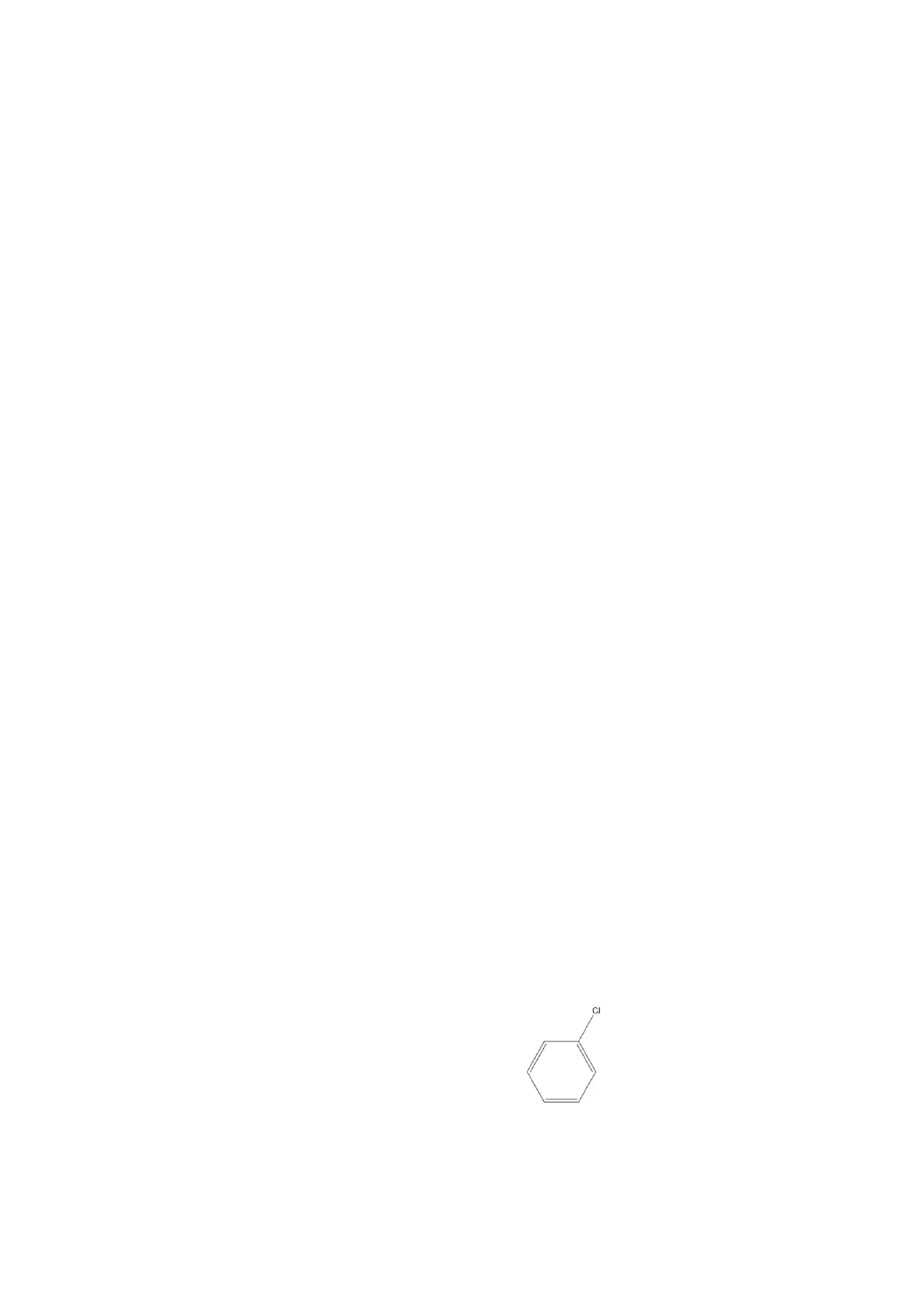
Similar a la de los alcanos, considerando el halógeno un sustituyente de la cadena principal. Se comienza la numeración por el lado más próximo al halógeno y su número de posición de indica delante. CH3-CH3-CH3-Cl 1-Cloropropano CI Clorobenceno CH3-CH3Cl-CH3 2-Cloropropano
PROPIEDADES FÍSICAS DE LOS HALOGENUROS DE ALQUILO
- Son poco solubles en agua, debido a su baja capacidad para formar enlaces de hidrógeno. Presentan un comportamiento bastante apolar, especialmente los que tienen cadenas largas o halógenos grandes. Son solubles en disolventes orgánicos apolares o ligeramente polares, como los disolventes alifáticos (por ejemplo, hexano o éter). Se utilizan frecuentemente como disolventes en química orgánica debido a su capacidad para disolver compuestos orgánicos sin reaccionar con ellos.
- Tienen puntos de fusión y ebullición más altos que los alcanos correspondientes, debido a: o La polarización del enlace C-X (que permite interacciones dipolo-dipolo) o Su mayor masa molecular, que intensifica las fuerzas de dispersión (fuerzas de Van der Waals)
- Cuando el halógeno es el mismo, los puntos de fusión y ebullición aumentan con el número de carbonos en la cadena, por el incremento de las fuerzas de Van der Waals.
- Si se mantiene la misma cadena, los puntos de fusión y ebullición aumentan desde el flúor hasta el yodo, ya que los halógenos más pesados son más polarizables y generan fuerzas intermoleculares más fuertes.
- Los compuestos ramificados presentan puntos de ebullición más bajos que sus isómeros lineales, ya que sus moléculas no se pueden apilar eficientemente y generan menos interacción intermolecular.
- Los halogenuros más ligeros (con pocos átomos de carbono y halógenos pequeños) suelen ser gases a temperatura ambiente. A medida que aumenta el número y tamaño de los átomos de halógeno, los compuestos se vuelven líquidos o sólidos, debido al aumento en la masa y las fuerzas intermoleculares.
ALCOHOLES
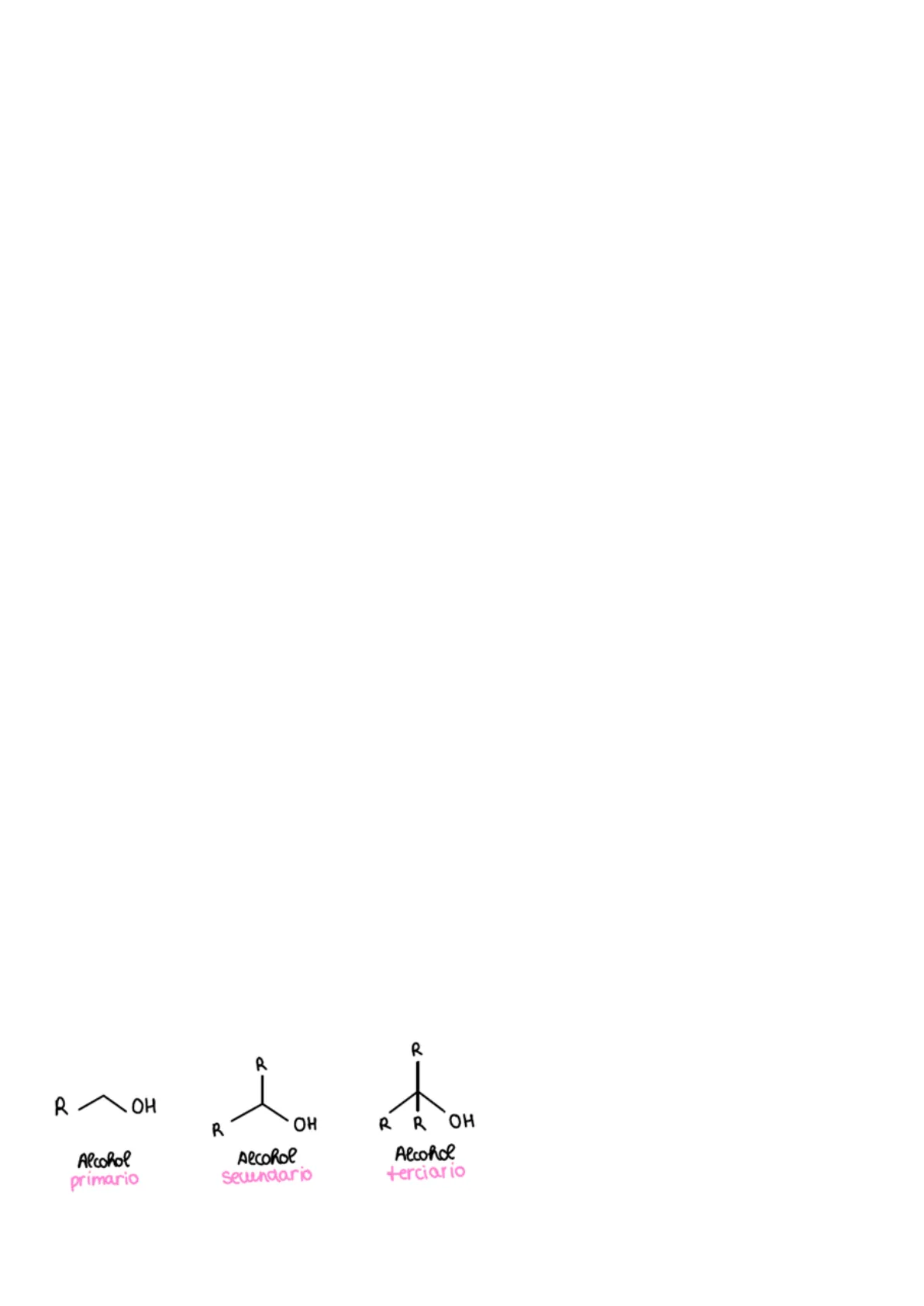
Compuestos en los que se sustituye un hidrógeno por un grupo OH (hidroxilo) y también se clasifican en primarios secundarios y terciarios. R R ~OH R OH R R OH Alcohol primario Alcohol secundario R Alcohol terciario
NOMENCLATURA DE LOS ALCOHOLES
Se utiliza el sufijo -ol para indicar el grupo hidroxilo. Como los alcanos, sustituyendo -o del alcano por -ol.
PROPIEDADES DE LOS ALCOHOLES
Los alcoholes tienen puntos de ebullición más altos que los alcanos y los halogenuros de alquilo porque el grupo hidroxilo -OH permite formar puentes de hidrógeno. Esto ocurre porque: El oxígeno, al ser muy electronegativo, atrae hacia si los electrones del enlace O-H y queda con carga parcial negativa (6-), pudiendo atraer al hidrogeno de otra molécula.
- El hidrógeno, al quedarse con menos electrones, queda con carga parcial positiva (5+), pudiendo atraer al oxigeno de otra molécula.
Así, se forman puentes de hidrógeno, que son mucho más fuertes que las fuerzas de Van der Waals (en los alcanos) o los dipolos permanentes (en los halogenuros). Y cómo esas atracciones son más fuertes, se necesita más energía (temperatura) para separarlas y que hiervan.
ISOMERIA OPTICA
Isomería óptica es un tipo de isomería en la que dos moléculas tienen la misma fórmula molecular y estructura general, pero no son superponibles, como una mano derecha y una izquierda. Esto ocurre cuando la molécula tiene un átomo de carbono quiral o asimétrico, es decir, un carbono unido a cuatro grupos sustituyentes diferentes. Estas moléculas se llaman enantiómeros, y se diferencian en cómo desvían la luz polarizada: uno la desvía a la derecha (dextrógiro +) y el otro a la izquierda (levógiro -). Su disposición espacial viene dada pro las configuraciones R o S. Emil Fisher:
- R/S: Describe la configuración espacial de los átomos alrededor de un carbono quiral.
- D/L: Describe la forma en que una molécula desvía la luz polarizada, aunque no está directamente relacionada con la configuración R/S
Una proyección de Fischer es una forma de representar moléculas orgánicas, especialmente moléculas con carbonos quirales, en dos dimensiones. Representa un centro asimétrico (carbono quiral) como la intersección de dos líneas perpendiculares. Las líneas horizontales representan los enlaces que salen del plano (hacia delante), y las verticales, los que entran (hacia atrás)
Configuración R o S
- Ordenar/numerar los sustituyentes del carbono quiral en función del número atómico. En caso de tener por ejemplo 2 alcanos, irá primero el que tiene mayor Mm. Ej: Cl (1) >C2H5 (2) >CH3 (3) >H (4)
- Situar de forma que el sustituyente de menor prioridad (Normalmente H) quede hacia atrás 3 3 R S Om 4 4 m 2 1 1 2 R
REACTIVIDAD
Reacciones de sustitución nucleófila
RCH2CH2X + Y- à RCH2CH2Y + X-
- Reacción de eliminación RCH2CH2X + Y- à RCH=CH2 + HY + X- X -> Grupo saliente
GRUPOS SALIENTES
El grupo saliente es el átomo o grupo de átomos que abandona la molécula cuando entra el nucleófilo en una reacción de sustitución. Normalmente, se trata de una especie que se desprende con carga negativa, es decir, actúa como la base conjugada del ácido del que proviene. La calidad de un grupo saliente está directamente relacionada con la estabilidad de esa base conjugada. Cuanto más débil sea esa base (es decir, cuanto más estable sea por sí sola), mejor grupo saliente será. Esto se puede predecir con el pKa del ácido del que proviene: Ácidos fuertes tienen pKa bajos y generan bases conjugadas débiles.
- Por tanto, un buen grupo saliente proviene de un ácido fuerte, ya que al separarse queda como una base débil, estable y poco reactiva, lo cual favorece que la reacción avance.
Un ejemplo claro es el agua (H2O), que proviene del ácido fuerte H3O+. Al actuar como grupo saliente, forma una molécula neutra y estable, ideal para reacciones de sustitución. Cuando el grupo saliente se va, se queda solo en solución como una base conjugada. Si esa base es débil, quiere decir que: Es estable por sí sola, no va a querer volver a reaccionar y no complica la reacción ni la revierte.
REACCIONES DE SUSTITUCIÓN NUCLEÓFILA
Mecanismo en dos etapas: SN1 (unimolecular)
1. Formación del carbocation:
El enlace entre el carbono y el grupo saliente (C-X) se rompe. El par de electrones del enlace se queda con el grupo saliente, y se forma un carbocatión como intermediario. Esta es la etapa lenta y determina la velocidad de la reacción, que sigue una cinética de primer orden: V = k [R-X] Es decir, la velocidad depende solo de la concentración del sustrato (la molécula que pierde el grupo saliente), no del nucleófilo.
2. Ataque del nucleófilo:
El nucleófilo ataca al carbocatión para formar el producto. Dado que el carbocatión es plano (hibridación sp2), el nucleófilo puede atacar desde ambos lados, lo que puede dar lugar a una mezcla racémica si el centro reaccionante es quiral (mezcla de los dos enantiómeros). En muchas reacciones SN1, el disolvente actúa como nucleófilo. Cuando esto ocurre, el proceso se denomina solvólisis.
Factores que afectan la reacción SN1:
Calidad del grupo saliente:
Cuanto mejor sea el grupo saliente (es decir, más estable como especie independiente), más fácil será que se disocie y más favorable será la reacción.
Estabilidad del carbocation intermedio:
Cuanto más estable sea el carbocation, más probable y rápida será la reacción. Por eso, los carbocationes terciarios (estabilizados por efecto inductivo y resonancia) reaccionan más fácilmente que los secundarios, y estos más que los primarios.
MECANISMO EN 1 ETAPA: SN2 (bimolecular)
En la reacción SN2, el ataque del nucleófilo y la salida del grupo saliente ocurren de forma simultánea, en una sola etapa. A medida que se forma el enlace entre el nucleófilo y el carbono, el enlace entre el carbono y el grupo saliente se va rompiendo al mismo tiempo. El nucleófilo ataca al carbono desde el lado opuesto al grupo saliente, es decir, por detrás del carbono, lo que genera una inversión de la configuración en ese carbono (efecto conocido como "inversión de Walden"). Durante el proceso, el carbono en el estado de transición se encuentra con una hibridación sp2 (ya que está parcialmente unido al nucleófilo y al grupo saliente), y los tres sustituyentes (el nucleófilo, el grupo saliente y el átomo de carbono) se disponen en un plano. Esto significa que en el estado de transición, el carbono está parcialmente involucrado en los enlaces con el nucleófilo y el grupo saliente, pero aún no está completamente formado ni uno ni otro. Es concertada: ambas reacciones ocurren en una sola etapa
- Es bimolecular: la velocidad de la reacción depende de la concentración de ambas sustancias, no solo de una Mismo plano + + Nucleófilo G. Saliente Inversión de Walden G. Saliente
El volumen de los sustituyentes es muy importante en las reacciones Sn2: el nucleófilo necesita espacio suficiente para acceder al centro electrófilo.
Factores que afectan a Sn2:
Grupo saliente: Cuanto mejor sea (más débil como base), mayor facilidad tendrá para abandonar la molécula y favorecer la reacción. Nucleófilo: Un buen nucleófilo acelera la SN2. Si los átomos son del mismo tamaño, las bases más fuertes suelen ser mejores nucleófilos. Volumen del nucleófilo: Nucleófilos voluminosos reaccionan más lentamente, aunque sean bases fuertes, debido al impedimento estérico.