Appunti di Chimica: stati di aggregazione della materia e passaggi di stato
Documento di Chimica sul Modulo I, che esplora gli stati di aggregazione della materia e i relativi passaggi di stato. Il Pdf, utile per la scuola superiore, approfondisce i fenomeni fisici e chimici, e il concetto di massa, con schemi e grafici esplicativi.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
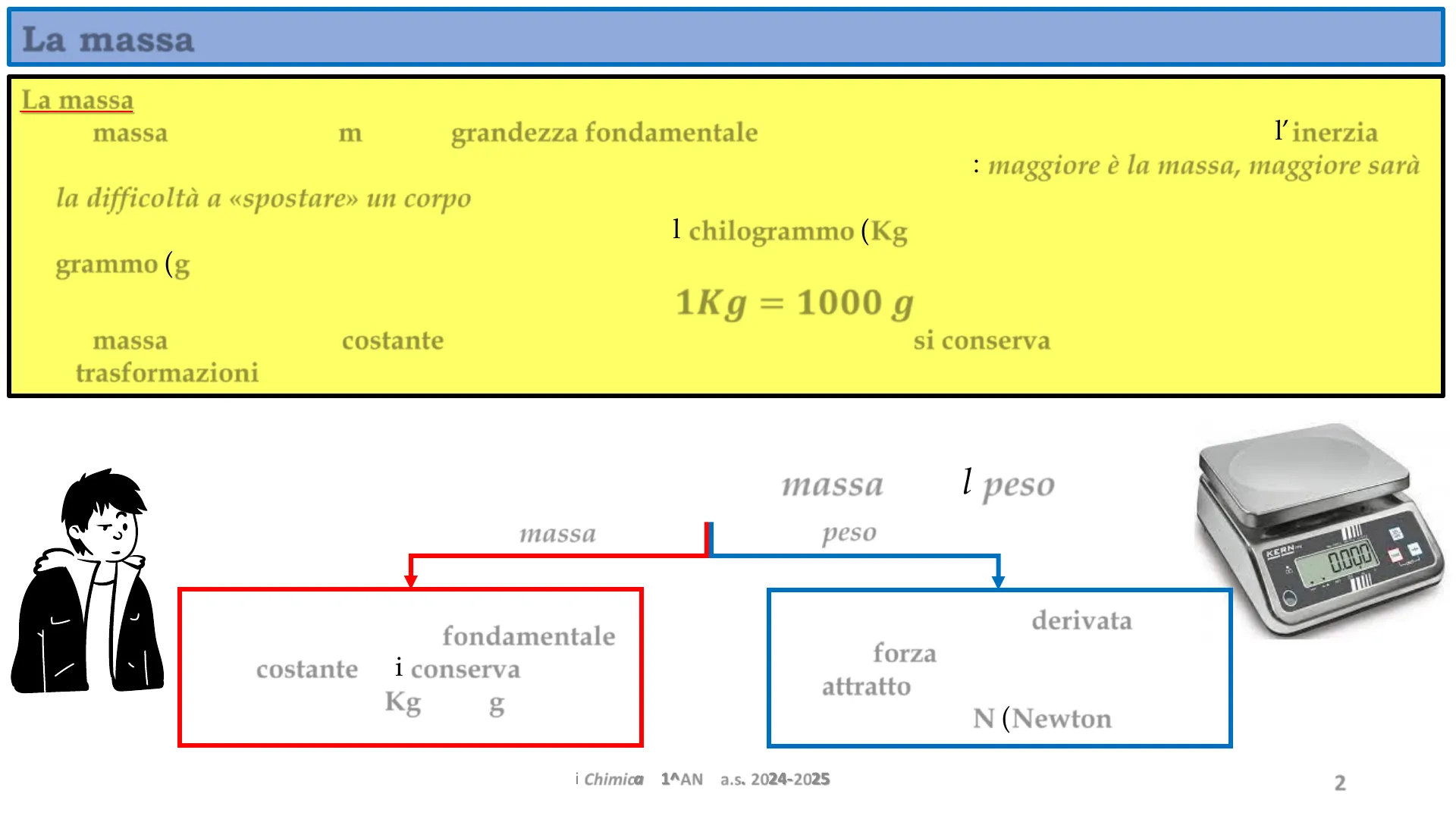
La massa
La massa (indicata con m) è una grandezza fondamentale. È caratteristica di tutti i corpi e ne misura l'inerzia, cioè la resistenza che oppongono alla variazione dello stato di moto o quiete: maggiore è la massa, maggiore sarà la difficoltà a «spostare» un corpo. L'unità di misura nel Sistema Internazionale (SI) è il chilogrammo (Kg), ma in Chimica sperimentalmente si usa il grammo (g). Ricorda: 1Kg = 1000 g. La massa di un corpo è costante in ogni punto dell'universo. La massa si conserva, anche se il corpo è sottoposto a trasformazioni. Non bisogna confondere la massa con il peso.
Massa vs Peso
- È una grandezza fondamentale;
- È costante e si conserva;
- Si misura in Kg (o in g);
- È una grandezza derivata;
- È la forza con cui il corpo è attratto dalla Terra;
- Si misura in N (Newton);
Il volume
Il volume (indicato con V) è una grandezza derivata dalla lunghezza: ha le dimensioni di una lunghezza al cubo. È la porzione di spazio che un corpo occupa. L'unità di misura nel Sistema Internazionale (SI) è il metro cubo (m3), ma in Chimica sperimentalmente per i liquidi si usano delle grandezze correlate. Ricorda: 1 dm3 = 1 L = 1000 cm3 = 1000 ml dove: dm3 (decimetrocubo); L (litro); mL (millilitro) 11= 1 dm3 = 1000 cm3 1 cm3 = 1 ml
La densità
La densità (indicata con d) è una grandezza derivata. È il rapporto tra la massa e il volume di un corpo. m d= = V nel caso dell'acqua: 1000kg/m3 = 1 kg / dm3 = 19/cm3
Esempio di densità: acqua e olio
L'olio è meno denso dell'acqua. Un litro Uguali volumi di olio e acqua hanno massa diversa.Il calore e la temperatura La temperatura La temperatura è la proprietà della materia che esprime il livello termico (agitazione termica delle particelle) di un corpo, ossia quanto questo corpo è «caldo» (alta temperatura) o «freddo» (bassa temperatura). Il calore Il calore è la forma di energia che passa spontaneamente (fluisce) dai corpi caldi (a temperatura maggiore) a quelli freddi (a temperatura minore). Questo trasferimento di energia cessa quando i corpi raggiungono la stessa temperatura. Calore e temperatura sono quindi grandezze correlate tra loro: fornendo calore ad un corpo la sua temperatura aumenta; se sottraiamo calore allora la temperatura del corpo si abbasserà.
Scale termometriche
T(K) =t(ºC) + 273 t(C) = T(K) - 273 Esempi: · se t (℃)= 20 ℃, allora T (K) = 20 + 273 = 293 K · se T (K)= 250 K, allora t (°℃) = 250 - 273 = - 23 ℃
La materia e le sostanze
La materia è tutto ciò che possiede massa e occupa un volume. La realtà che ci circonda si presenta in molteplici forme che, sebbene differenti tra loro, hanno in comune queste due proprietà essenziali. I diversi tipi di materia che possiedono caratteristiche anche molto diverse prendono il nome di materiali. Sostanza Una sostanza è un particolare tipo di materia che possiede proprietà caratteristiche e ben determinate. Le proprietà si dividono in intensive ed estensive.
Proprietà intensive ed estensive
Sono proprietà indipendenti dalle dimensioni del corpo e quindi sono identiche (non variano) per qualsiasi corpo o campione. Sono proprietà che dipendono dalle dimensioni del corpo e quindi assumeranno valore diverso (variano) a seconda del campione.
Esempi di proprietà intensive e proprietà estensive
Ecco alcuni esempi di proprietà intensive e proprietà estensive.
Proprietà intensive
A. La densità. La densità dell'olio è minore di quella dell'acqua, indipendentemente dall'estensione dei due liquidi: perciò l'olio galleggia sull'acqua, indipendentemente dalle quantità dei due liquidi. B. Il colore. Il rame è sempre di colore rosso, a prescindere D. La temperatura di ebollizione. La temperatura di ebollizione dell'acqua (100°℃ alla pressione di 1 atm) non dipende dal volume del liquido.
Proprietà estensive
La lunghezza dei corpi La massa dei corpi Il volume dei corpi
Gli stati di aggregazione della materia
La materia si presenta sotto forma di 3 stati fisici di aggregazione
Stato solido
Le particelle che lo compongono sono a stretto contatto e occupano posizioni reciproche fisse Ha VOLUME proprio Ha FORMA propria
Stato liquido
Le particelle che lo compongono sono a stretto contatto ma non occupano posizioni reciproche fisse Ha VOLUME proprio Prende la forma del recipiente che lo contiene
Stato gassoso
Le particelle che lo compongono sono distanti tra loro e sono in perenne movimento. NON ha VOLUME proprio Occupa tutto lo spazio che ha a disposizione
Come avvengono i cambiamenti di stato
La maggior parte delle sostanze può trovarsi allo stato solido, liquido e gassoso e passare da uno stato all'altro, ossia subire i diversi passaggi di stato.
Assorbimento di calore
sublimazione fusione vaporizzazione solido liquido aeriforme
Cessione di calore
solidificazione condensazione brinamento Per fare ciò è necessario assorbire o cedere calore (a seconda della direzione in cui si procede). Osserviamo quindi che gli stati fisici di aggregazione, come accennato, si differenziano per il diverso grado di agitazione termica delle particelle del sistema.
Le curve di riscaldamento
La curva di riscaldamento descrive il modo in cui la temperatura di una sostanza, inizialmente solida, varia in funzione del tempo, mentre viene fornito calore a velocità costante.
Variazione di temperatura durante i passaggi di stato
Durante i passaggi di stato la temperatura non varia perché il calore fornito non aumenta l'agitazione termica, ma viene usato per vincere la forza di interazione tra le particelle.
Fasi della curva di riscaldamento
A una data pressione (in genere quella atmosferica), (a) fornendo calore a una sostanza allo stato solido, questa aumenta di temperatura finché, (b) raggiunta una temperatura ben determinata, fonde, ossia passa allo stato liquido. Durante la fusione, pur continuando a fornire calore, la temperatura rimane costante, fino a quando tutta la massa della sostanza non si è trasformata in liquido. Terminata la fusione, (c) l'ulteriore somministrazione di calore provoca l'aumento di temperatura del liquido; poi, (d) a una temperatura specifica, il liquido raggiunge l'ebollizione, vale a dire passa a vapore nell'intera sua massa in modo tumultuoso. Nel corso dell'ebollizione, la temperatura si stabilizza di nuovo; infine, (e) quando tutto il liquido è diventato vapore, se si fornisce ancora calore, la temperatura del vapore aumenta.
I passaggi di stato nei solidi
Cambiamenti di stato in riscaldamento
Fusione Si definisce fusione il passaggio di una sostanza dallo stato solido a quello liquido. Sublimazione Si chiama sublimazione il passaggio diretto dallo stato solido a quello di vapore.
Cambiamenti di stato in raffreddamento
Solidificazione Prende il nome di solidificazione il passaggio di una sostanza dallo stato liquido a quello solido. Brinamento Si intende per brinamento il passaggio diretto da vapore allo stato solido.
Esempio: sublimazione e brinamento dello iodio
Il punto di solidificazione (o temperatura di solidificazione) coincide con quello di fusione. Per esempio, la fusione del ghiaccio e il congelamento dell'ac- qua avvengono entrambi alla temperatura di 0 °C. Questo vale per qualsiasi coppia di passaggi di stato in riscaldamento / raffreddamento.
Liquidi, aeriformi e passaggi di stato
La vaporizzazione e la condensazione
Il passaggio di stato da liquido a vapore prende il nome di vaporizzazione. Viceversa si ha la condensazione.
Tipi di vaporizzazione
evaporazione ebollizione L'evaporazione avviene a qualsiasi temperatura nel campo di esistenza del liquido. Si tratta di un fenomeno superficiale. Prende il nome di ebollizione la vaporizzazione che interessa ogni punto di un liquido. Avviene ad una determinata temperatura.
Dipendenza dalla pressione
A una determinata pressione, l'ebollizione di ogni liquido avviene a una temperatura caratteristica e costante, detta punto di ebollizione (o temperatura di ebollizione). Il punto di ebollizione, dipende notevolmente dalla pressione esterna: per esempio, sulla vetta del Monte Everest la pressione dell'aria è talmente bassa che l'acqua bolle a 76°C.
Le trasformazioni della materia
Trasformazioni fisiche
Le trasformazioni fisiche non danno origine a nuove sostanze. La natura della sostanza coinvolta non varia, cioè le particelle che la costituiscono non subiscono modificazioni.
Trasformazioni chimiche
Le trasformazioni chimiche o reazioni chimiche sono processi in cui le sostanze iniziali si trasformano in nuove sostanze. È un processo attraverso il quale le sostanze modificano la loro identità chimica, si trasformano cioè in sostanze differenti. Le sostanze iniziali di una reazione chimica sono dette reagenti, quelle finali prodotti.
Esempi di comuni trasformazioni fisiche
- La fusione dei ghiacci polari
- La dilatazione termica dei binari esposti al sole
- La dissoluzione del sale da cucina in acqua
Esempi di comuni trasformazioni chimiche
- Arrugginimento di una catena di ferro
- L'imbrunimento di una fetta di mela lasciata all'aria
- La combustione del metano nei fornelli di casa
NOTA: abbiamo analizzato in dettaglio i tre stati fisici della materia e i possibili passaggi di stato. Tutti i passaggi di stato sono trasformazioni fisiche, perché non alterano la composizione delle sostanze coinvolte.