Il Carbonio: Ibridazione, Isomeria e Metabolismo in Chimica Organica
Documento dall'Università sul Carbonio, Ibridazione e Isomeria. Il Pdf, di Chimica per l'Università, esplora l'ibridazione del carbonio, l'isomeria, il metabolismo dei lipidi e delle proteine, la fase oscura della fotosintesi e la genetica dei virus, con un focus schematico sugli orbitali e i legami.
Mostra di più29 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
IL CARBONIO
Presentazione del Carbonio
- IVA
- valenza: II, IV in chimica organica solo 4
- configurazione elettronica: 1s2 2s2 2p2
- z= 6
A = 12
Gli orbitali
Gli orbitali: bilobati(p), sferici(s)
L'ibridazione del carbonio
Ibridazione sp3
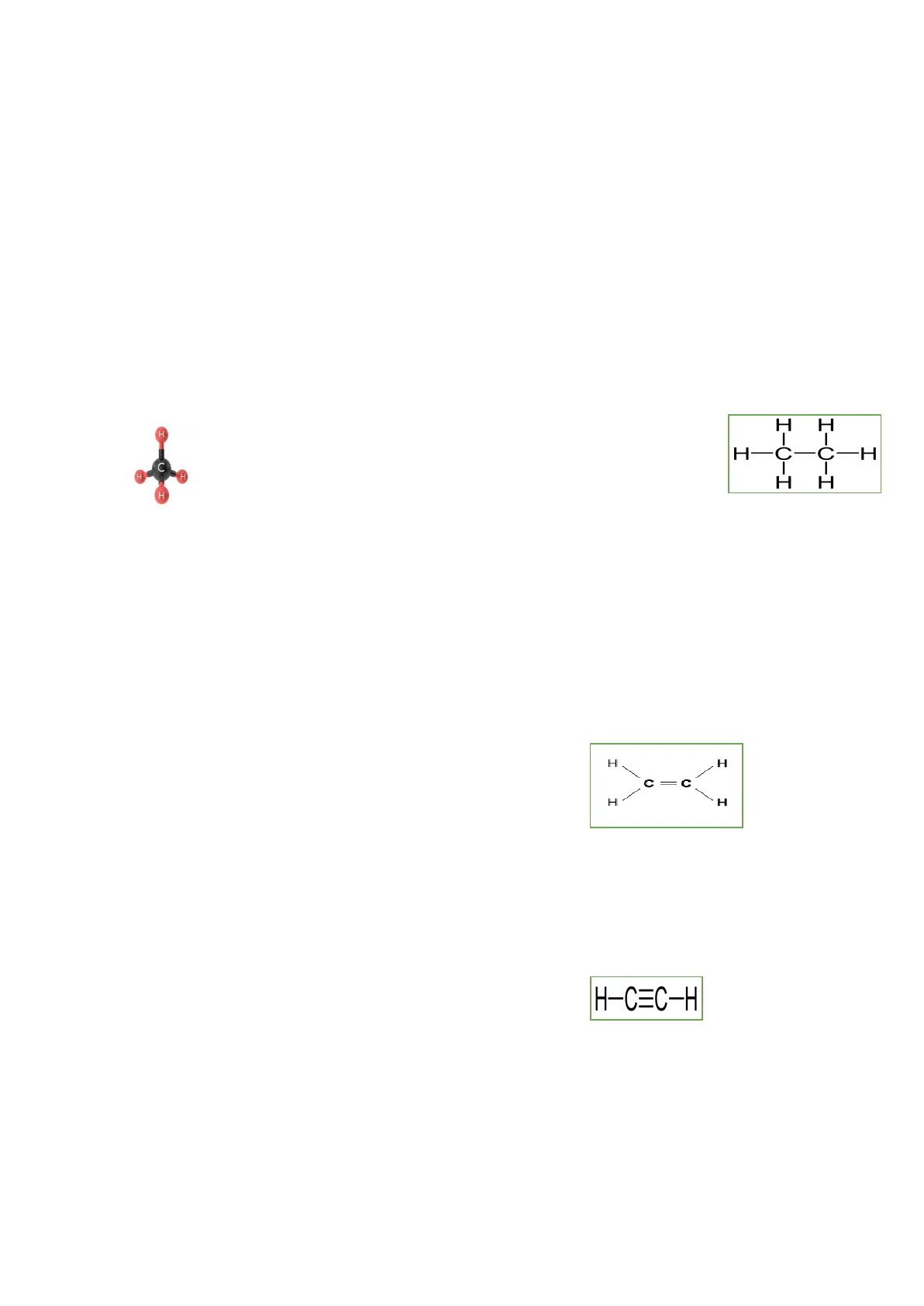
H C H un orbitale s si ibrida con 3 orbitali p quindi il 75% sarà bilobato e il 25% sarà sferico viene utilizzata dal carbonio in tutti i suoi composti in cui forma 4 legami singoli con altri 4 atomi (es. etano C2H6, metano CH4) geometria: tetraedrica natura del legame: 4 sigma 0 TT numero orbitali p PURI: 0
Ibridazione sp2
un orbitale s si ibrida con 2 orbitali p quindi il 66% sarà bilobato e il 33% sarà sferico utilizzata quando il carbonio è legato ad altri 3 atomi(es. etene C2H4) geometria: triangolare planare natura dei legami: 3 sigma 1 TT numero orbitali p PURI: 1 H H C=C H H
Ibridazione sp
un orbitale s si ibrida con un orbitale p quindi il 50% sarà bilobato e il 50% sarà sferico utilizzata quando il carbonio si lega a 2 atomi con geometría planare (es. etino C2H2) geometria: lineare H-C=C-H natura dei legami:1 sigma, 2 TT numero orbitali p PURI: 2
Legami sigma
- più forte dal punto di vista energetico
- è il primo che si forma, posizionandosi in modo tale che gli elettroni siano al centro
- si ha con un orbitale sferico più uno bilobato sull'asse di legame H-C-C-H H I-O-I H H H
- esempi: H2 -> legame covalente o puro H2O -> legame covalente o polare F2 -> legame covalente o puro
Legami TT
- si forma dopo ed è perpendicolare;
- non include l'asse di legame
- si forma per sovrapposizione laterale di orbitali p non ibridati (PURI) In generale
- un legame doppio consiste sempre in un legame o e in uno TT;
- un legame triplo consiste in 2 sono legami TT e uno o ;
- se è presente un legame multiplo gli atomi coinvolti avranno ibridazione sp2 o sp.
L'isomeria
Sono detti isomeri quei composti che hanno stessa formula molecolare ma con differente formula di struttura e diverse proprietà fisiche e chimiche.
Isomeria di struttura
Isomeria di struttura: due o più composti che hanno la stessa formula molecolare ma presentano una diversa sequenza degli atomi di carbonio o una diversa posizione dei legami multipli
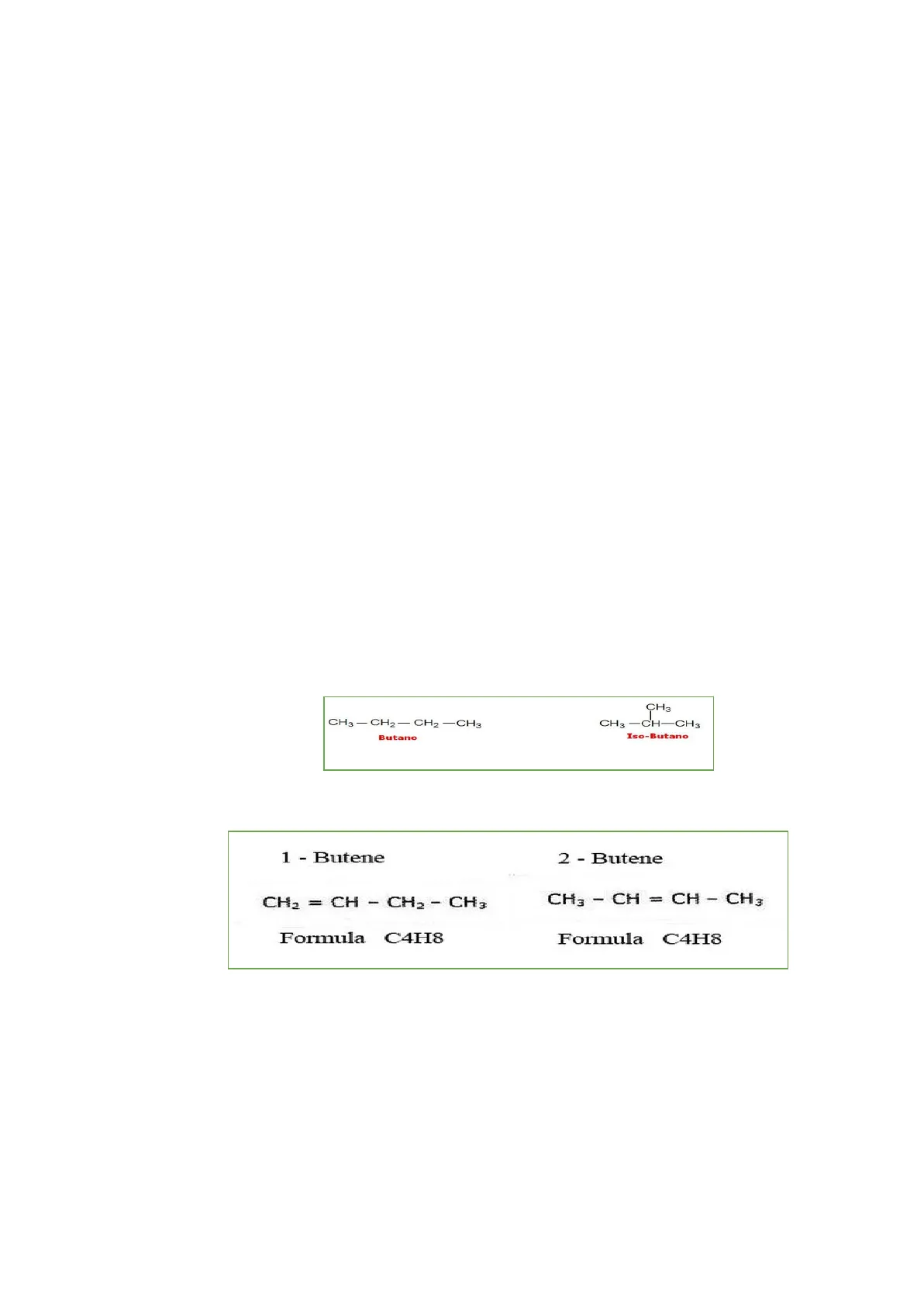
- Isomeri di catena: sono composti che differiscono per il diverso modo con cui gli atomi di carbonio sono legati nella catena carboniosa. es: C4H10 CH3 CH3 - CH2- CH2 -CH3 CH3 -CH-CH3 Iso-Butano Butano
- isomeri di posizione: sono composti con la stessa catena carboniosa ma differiscono per la posizione di un legame multiplo(doppio legame o triplo) 1 - Butene 2 - Butene CH2 = CH - CH2 - CH3 CH3 - CH = CH - CH3 Formula C4H8 Formula C4H8
- Isomeri di gruppo funzionale: sono composti che presentano gruppi funzionali diversi nella catena carboniosa quando un composto ha gruppo funzionale ossidrilico è chiamato alcol; quando un composto ha gruppo funzionale un atomo di ossigeno è un etere;
La stereoisomeria
La stereoisomeria: fenomeno in cui atomi o gruppi atomici di due o più composti sono legati tra loro nella stessa sequenza ma con differente disposizione spaziale.
- isomeri geometrici: sono due composti che differiscono per la disposizione spaziale di atomi o gruppi atomici legati a due atomi di carbonio uniti da: legami semplici cicloalcani doppio legame alcheni
- isomeri ottici (enantiomeri): sono due molecole con diversa disposizione spaziale che sono l'una l'immagine speculare dell'altra ma NON sovrapponibili. Deve essere presente uno stereocentro, un atomo di carbonio legato a 4 atomi o gruppi atomici diversi. I due enantiomeri hanno proprietà chimiche e fisiche diverse (glucosio acido lattico, aminoacidi) : proprietà chimiche: in una molecola il substrato reagisce con il sito attivo dell'enzima quando c'è una conformazione sterica mentre nell altra non c'è una conformazione quindi non reagisce proprietà fisiche: i due enantiomeri fanno ruotare il piano della luce polarizzata di due angoli uguali ma con direzioni opposte levogiro fa deviare la luce a sinistra destrogiro fa deviare la luce a destra Se si ha una miscela 50% e 50% si ha un racemo, quindi la luce non devia.
Gli idrocarburi
Gli idrocarburi sono composti organici costituiti esclusivamente da carbonio e idrogeno. origine fossile non polari. aromatici(chiusi) e alifatici(chiusi e aperti)
Gli Alcani
Proprietà fisiche degli Alcani
- proprietà fisiche: 1. Hanno basso punto di ebollizione che aumenta all'aumentare della lunghezza e della ramificazione della catena carboniosa; 2. A temperatura ambiente sono aeriformi; 3. La loro densità è minore di quella dell acqua; 4. Sono apolari a causa della minima differenza di elettronegatività tra H e C; 5. Insolubili in acqua ma solubili in solventi apolari; 6. Hanno una forma tetraedrica
Proprietà chimiche degli Alcani
- proprietà chimiche : 1. Sono ibridati sp3 quindi hanno 4 legami semplici carbonio-carbonio e per questo sono saturi. 888 4 sp3 orbitals 2 p hybridize E 1111 2 . 88.88 4 orbitals mixed - 4 orbitals formed 2. Sono idrofobici. 3. Tra idrocarburi si ha una miscela omogenea. 4. Tra un idrocarburo e l'altro ci sono le forze di London che sono forze deboli a cui basta poca energia per essere spezzate. 5. CnH2n+2 a. prefissi: met, et, prop, but, pent, es, ept; suffisso: ano;
Isomeria degli Alcani
- Isomeria: Di catena
Reattività degli Alcani
- Reattività: reazione di ossidazione (combustione): è una reazione di ossidoriduzione fortemente esotermica che avviene in eccesso di O2 e porta alla formazione di CO2 e acqua. CH4 + 2 02 - CO2 + 2 H2O C3Hg + 5 02 - 3 CO2 + 4 H20 (3n + 1) /2 = coefficiente stechiometrico dell'O2 ΔΗ<0
- reazione di alogenazione ( sostituzione elettrofila ): è una reazione che avviene tra un alcano e un alogeno Xz, che avviene con la presenza raggi ultravioletti (UV) o fornendo calore(A) e non spontanea. A sostituirsi è l'atomo di H con l' X2. I prodotti sono un alogenuro alchilico e un acido alogenidrico. Qui avviene una rottura omolitica (ciascun atomo trattiene uno dei due elettroni di legame, avendo la formazione di radicali liberi).
I cicloalcani
- Def: sono idrocarburi alifatici a catena chiusa, saturi per la presenza di legami semplici carbonio-carbonio
- CnH2n n>=3;
- le proprietà chimiche e fisiche e la reattività è uguale a quella degli alcani.
- Nomenclatura: prefisso ciclo e dal dell'alcano Viene utilizzata principalmente la formula topologica.
Isomeria dei cicloalcani
- Isomeria: Isomeria di posizione: con i sostituenti uguali il nome del composto è preceduto dai prefissi -di, -tri, -tetra. con i sostituenti diversi i nomi sono indicati in ordine alfabetico.
- isomeria geometrica: i due sostituenti possono trovarsi nella stessa parte (cis) o da parti opposte(trans) rispetto al piano
Reattività dei cicloalcani
- Reattività: reazione di ossidazione; reazione di alogenazione; reazione di addizione: avviene solo con il ciclopropano e il ciclobutano che reagiscono con H2 in presenza del catalizzatore Pt, o con Br2 in presenza di luce
Gli alcheni
- Gli alcheni sono idrocarburi alifatici a catena aperta, insaturi per presenza di un doppio legame carbonio-carbonio.
Caratteristiche degli Alcheni
- Caratteristiche: 1. ibridati sp2 2. il doppio legame implica a. non si ha una libera rotazione intorno al legame perché comporterebbe la rottura del legame pigreco che richiede energia non disponibile a temperatura ambiente; b. lunghezza doppio legame < lunghezza legame semplice; c. la molecola è più instabile e quindi più reattiva per la presenza di un legame sigma e pigreco. 3. CnH2n n>=2 4. suffisso -ene.
Isomeria degli Alcheni
- Isomeria: isomeria di posizione isomeria di catena isomeria geometrica
Reattività degli Alcheni
- Reattività: reazione di idrogenazione: è l'addizione di un alchene e H2 in presenza di un catalizzatore metallico (Pt) avendo come prodotto un alcano. è una reazione di riduzione in cui gli atomi di C formano nuovi legami con l'H e in cui il n.o. del C diminuisce mentre il n.o dell'H aumenta. C=C / 1 + H2 ->-C-C- + Calore H H
- addizione elettrofila alogenazione: si aggiunge ad un alchene un alogeno e si avrà come prodotto un alcano con i due atomi dell'alogeno, chiamato alcano disostituito. (avviene in un solvente inerte CCl4 ) idroalogenazione: avviene tra un alchene e un acido alogenidrico. Regola di Markovnikov dice che il meccanismo di reazione avviene in due stadi in cui l'H (elettrofilo) si lega all'atomodi carbonio del doppio legame con legato al maggior numero di atomi di idrogeno 1. Nel primo stadio si ha l'addizione dello ione H+ elettrofilo al doppio legame con formazione di un carbocatione 2. Nel secondo stadio si ha l' addizione dello ione dell'alogeno al carbocatione più stabile. idratazione: avviene tra un alchene e H2O in presenza di un catalizzatore acido H+ e il prodotto sarà un alcol. HO H H+ R-C=C-H + H2O - R-C-C- H R' H 1. 1 R' H
Gli alchini
Gli alchini sono idrocarburi alifatici a catena aperta, insaturi per presenza di un triplo legame carbonio-carbonio.
Caratteristiche degli Alchini
Caratteristiche: 1. ibridazione sp 2. il triplo legame implica: a. lunghezza triplo legame < lunghezza doppio legame; b. energia triplo legame > energia del doppio legame; c. molecola più instabile e più reattiva per la presenza di due legami pigreco e uno sigma. 3. CnH2n-2 n>=2 4. suffisso -ino.
Isomeria degli Alchini
- Isomeria: isomeria di posizione
- isomeria di catena
Reattività degli Alchini
- Reattività reazione di idrogenazione reazione di addizione elettrofila alogenazione idroalogenazione idratazione
Gli idrocarburi aromatici
Sono composti organici costituiti da uno o più anelli (catena chiusa) a sei atomi di carbonio. Gli atomi di carbonio nell'anello sono uniti da legami covalenti semplici e da un particolare tipo di legame nel quale gli elettroni sono delocalizzati. Il termine aromatico viene usato in chimica per indicare un composto dotato di un'elevata stabilità.
IL BENZENE
Caratteristiche del Benzene
- Caratteristiche C6H6 Sp2
- A temperatura ambiente è liquido incolore e volatile (maria volatile significa che vaporizza facilmente non che il benzene vola ingnorante)
- è apolare e insolubile in acqua
- è saturo e poco reattivo infatti è molto stabile e non dà reazioni di addizioni con l'H e con gli X2
- tutti i legami hanno la stessa lunghezza = 1,39 Å 1. Kekulè, al fine di giustificare che il benzene non dà reazioni di addizione, ipotizzò che il benzene esistesse sotto forma di un anello esatomico rappresentato da due formule di struttura in equilibrio tra loro. Qui i legami semplici e doppi carbonio-carbonio sono alternati. 2. Questa teoria viene smentita con la fisica moderna e la misurazione della lunghezza e dell'energia di legame. 3. Si capisce così che il benzene è ibridato sp2 ed ha una forma ciclica ed esatomico, capendo che ci sono 6 elettroni delocalizzati KEKULÉ MODEL DELOCALISED MODEL 4. Il cerchio rappresenta la nube elettronica formata dai 6 elettroni delocalizzati, questi si trovano in p di conseguenza la nube si trova sotto e sopra il piano della molecola.
Reazioni del Benzene
- Il benzene da reazioni di sostituzione elettrofila
Derivati monosostituiti del Benzene
- Derivati monosostituiti: sostituzione con un alogeno (es: clorobenzene)
- sostituzione con un CH3 = toluene / metilbenzene
- sostituzione con un gruppo ossidrile OH = fenolo / idrossibenzene
- sostituzione con NH2 = anilina / amminobenzene
- sostituzione con NO2 = nitrobenzene
Derivati bisostituiti del Benzene
- Derivati bisostituiti: sostituzione con 2 gruppi CH3 = xilene CH CH CH, CH, CH, CH, o-xilene m-xilene p-xilene 1,2-dimetilbenze 1,3-dimetilbenzene 1,4-dimetilbenzene