Stati di aggregazione della materia, proprietà dei fluidi e termoregolazione
Documento di Università su Stati di aggregazione della materia. Il Pdf, un appunto di Chimica, esplora gli stati solido, liquido e gassoso, le proprietà dei fluidi come pressione e capillarità, e la termoregolazione, offrendo una panoramica completa per lo studio.
Mostra di più30 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Stati di Aggregazione della Materia
Gli stati di aggregazione della materia possono essere: solido, liquido e aeriforme.
I differenti stati di aggregazione sono caratterizzati da moti molecolari e interazioni intermolecolari molto diversi.
Negli stati di aggregazione si differenziano per 2 diverse caratteristiche: l'energia cinetica delle particelle della materia e le forze di attrazione che si sviluppano tra le diverse particelle. L'energia cinetica delle particelle è dovuta al movimento delle particelle stesse e possono essere 3 diversi movimenti:
- Traslazionale: le particelle si spostano rispetto al baricentro del sistema macroscopico;
- Vibrazionale: spostamento delle particelle rispetto al punto di equilibrio della particella;
- Rotazionale: movimento attorno al suo asse molecolare;
moto di vibrazione
Stato Solido
- Si ha il minimo valore di energia cinetica, le forze di attrazione tra le particelle sono molto intense, generando una grande quantità di energia potenziale.
- Sono presenti diversi tipi legami, come ad esempio: covalenti, ionici, a idrogeno o forze di Van der Waals.
- Si forma una struttura molto ordinata e stabile dove le particelle sono ferme nel tempo.
- La struttura di un solido è rigida e indeformabile.
· Na Do Rappresentazione di un cristallo di cloruro di sodio; si può vedere come gli ioni siano fissi in determinate posizioni
Stato Liquido
- L'energia cinetica delle particelle è media, ci sono interazioni più deboli rispetto ai solidi, ma non nulle.
- Le forze di attrazione si sviluppano soprattutto tra particelle che si trovano sullo stesso strato.
- Possono essere considerati come strati molecolari che scorrono l'uno rispetto all'altro, senza interazioni particolarmente forti tra loro.
- E' incomprimibile, ma non ha forma propria.
Stato Gassoso
- E' presente la massima quantità di energia cinetica, perché sono presenti tutti e 3 i tipi di movimento (cfr. vedi sopra).
- Sono assenti le forze di attrazione intermolecolari, quindi le particelle sono indipendenti tra loro-> tendono ad occupare tutto il volume a loro disposizione.
- Non hanno una forma e non hanno volume proprio.
LIQUIDI GAS Deformabili e diffusibili Deformabili e diffusibili Incomprimibili (a causa di particelle molto impaccate) Comprimibili moto di traslazione moto di rotazione
Proprietà dei Fluidi
- I liquidi e gas sono solitamente considerati come fluidi e hanno 2 proprietà principali:
- Deformabilità-> possono essere deformati;
- Diffusibilità-> la graduale dispersione di una sostanza attraverso un'altra sostanza; si tratta di un processo in cui 2 liquidi miscibili si mescolano, dovuto da un diverso gradiente di concentrazione;
- Solo i gas possono compiere l'effusione, in particolare passano da zone di pressione maggiore a zone di pressione minore, attraverso fori molto sottili.
- Nella tavola periodica, sono presenti 11 elementi allo stato gassoso, in particolare sono gli elementi:
- Del gruppo 18 (gas nobili), in forma monoatomica;
- O, H, Cl, Na e F, in forma di molecole biatomiche;
- Che costituiscono le molecole poliatomiche a basso peso molecolare (es. CO2);
Volume e Pressione dei Gas
- Allo stato gassoso, la materia può essere descritta da 4 proprietà: 2 estensive (volume e massa) e 2 intensive (pressione e temperatura).
- Volume: viene misurato in m3 o litri (1L=1dm3=1000cm3, 1mL=1cm3) e dipende da variabili come temperatura e pressione.
- Temperatura: misura del livello termico delle sostanze in K o *C ed è un indicatore del flusso di calore.
Pressione
- Definita come la forza esercitata su una superficie e può essere espressa in Pa, Bar, mmHg o atm.
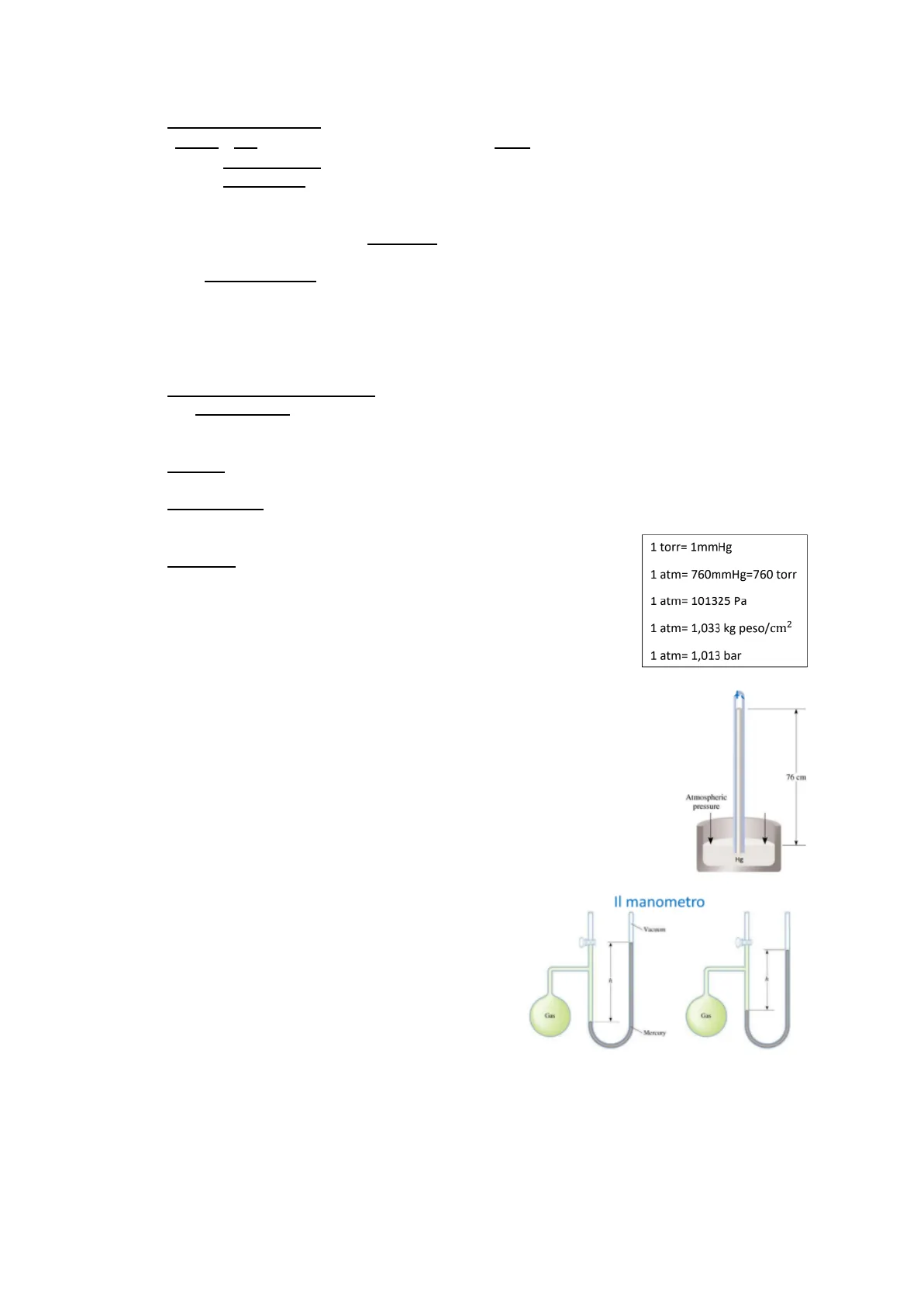
- Torricelli inventò il barometro (serve a misurare la pressione), in cui viene utilizzato un tubo chiuso, pieno di mercurio, che viene capovolto e messo in equilibrio con del mercurio in una vaschetta. A pressione atmosferica, l'altezza della colonnina di mercurio corrisponde a 76cm = 1mmHg. La forza peso esercitata da questi 76cm di mercurio corrisponde a 1,033kg peso/cm2.
1 torr= 1mmHg 1 atm= 760mmHg=760 torr 1 atm= 101325 Pa 1 atm= 1,033 kg peso/cm2 1 atm= 1,013 bar 76 cm Atmospheric pressure Hg
Il Manometro
Per misurare la pressione di un gas si usa uno strumento chiamato manometro, composto da un tubo ad U nel quale si trova del mercurio. Il manometro può essere formato da un braccio aperto, in contatto con l'atmosfera o un braccio chiuso, contenente generalmente il vuoto e raramente un altro gas. L'altro braccio sarà in contatto con il sistema preso in considerazione, il gas che si vuole misurare. Il mercurio nelle braccia avrà un livello diverso. Questo dislivello: · è proporzionale alla pressione assoluta del gas nel caso di un braccio chiuso · indica la differenza tra la pressione atmosferica e la pressione del gas, ovvero una pressione relativa, nel caso in cui il tubo sia aperto Volume, temperatura e pressione sono grandezze correlate da una relazione matematica chiamata equazione di stato. Solo nel caso dei gas esiste un'equazione di stato universale che vale per qualunque tipo di gas. Un'equazione generale non esiste per i liquidi e i solidi, se non per famiglie di liquidi/solidi accomunate da caratteristiche chimiche ben precise. Questo comportamento peculiare è dovuto al fatto che nei gas non esistono forze di interazione tra le particelle, esulando il gas dalla natura chimica delle particelle che lo compongono. L'equazione è applicabile solo quando il gas è considerato un gas ideale, ovvero quando: · le molecole che lo costituiscono possono essere considerate puntiformi, il volume delle particelle è irrilevante rispetto al volume del gasnon ci sono interazioni tra le particelle ● Queste due condizioni si verificano quando il gas è a bassa pressione. L'equazione di stato dei gas è stata derivata dalla fusione di alcune leggi sperimentali, ossia: · La legge di Boyle, che mette in correlazione pressione e volume del gas · La legge di Charles, che mette in correlazione il volume e la temperatura · La legge di Gay- Lussac, che mette in correlazione pressione e temperatura · Principio di Avogadro, che mette in relazione il volume di un gas con la massa del gas stesso, cioè con il numero di moli
cuum Gas Gas Mercury
Legge di Boyle: Legge Isoterma (1862)
La legge di Boyle mette in relazione pressione e volume del gas. Boyle utilizzò un tubo a forma di J in cui posizionò del mercurio, con del gas all'estremità chiusa. Questa legge regola una trasformazione a temperatura costante, per questo motivo è detta isoterma. Aumentando la pressione esercitata sul gas, grazie all'aumento della quantità di mercurio, si ha una diminuzione del volume proporzionale all'aumento di pressione. Da questa osservazione Boyle enunciò che: Il volume occupato da un gas a temperatura costante è inversamente proporzionale alla pressione esercitata su di esso. Sperimentalmente, quindi, pressione e volume sono inversamente proporzionali. P . V= k NB: questa è l'equazione che descrive una iperbole equilatera, che descrive il variare di due grandezze misurate a temperatura costante. Realizzando l'esperimento di Boyle a diverse temperature, si ottengono diverse iperboli, dette isoterme: con questo termine si intende il diagramma che illustra la variazione di una proprietà misurata a temperatura costante. Questo principio è applicabile anche alla respirazione: al momento dell'inspirazione il diaframma si contrae, aumentando il volume della cassa toracica, diminuendo quindi la pressione alveolare. Grazie alle proprietà dei fluidi, l'aria tende a diffondere negli alveoli, dove la pressione è più bassa. Nell'espirazione il processo avviene in maniera opposta.
Volume (L) 8 200 mmHg 6 8L 400 mmHg 4 4L 2 2L 0 0 100 200 300 400 1 1 P &c oppure V & V P Questa è l'equazione di una iperbole P (kPa) Ogni curva rappresenta una ISOTERMA 4 T (K) PV=k 3 500 2 300 100 1 1 1 (a) Espirazione: Inspirazione: la cavità toracica si espande la cavità toracica si contrae Cavia toracica 271 Polmone Polmone Cuore Cavità pleurica Diaframma
1^ Legge di Charles Gay-Lussac: Legge Isobarica
La legge di Charles e Gay-Lussac mette in relazione volume e temperatura e si basa su studi avvenuti alla fine del 700, circa 100 anni dopo Boyle. Il loro assetto sperimentale era costituito da un contenitore cilindrico contenente gas, dotato di un pistone mobile a tenuta stagna. Per mantenere la pressione costante il pistone si muoveva in modo da accomodare le variazioni di volume del gas causate dal variare della temperatura. Osservarono che il volume del gas aumentava all'aumentare della temperatura.
PRIMA LEGGE DI CHARLES E GAY LUSSAC 1787 To> T1 v. V2 > V1 T. Raddoppiando la temperatura as- soluta, il volume raddoppia. P P2= P1 PV = k, 100 mmHgSi può osservare il fenomeno su un grafico con T(x) e V(y), dove si crea una retta isobara in cui il volume è direttamente proporzionale alla temperatura in ℃. La pendenza delle rette, invece, dipende dalla massa dei gas. L'intercetta con l'asse delle ordinate rappresenta il volume occupato dal gas a T=0℃. Abbassando la temperatura a livelli estremi non è più possibile giungere in modo sperimentale ad una conclusione poiché il gas diviene liquido. Dalle osservazioni, però, si notò che tutte le isobare cadevano in un unico punto sull'asse > delle ascisse, corrispondente a -273,15℃. Questo portò alla formulazione di una scala della temperatura assoluta, ossia una scala in cui esiste una temperatura corrispondente alla Vo temperatura più bassa a cui la materia V=Vo (1+at) 273,15 TºC esiste e quindi dove un gas ha volume nullo (è la temperatura più bassa in assoluto perché -273,15℃ non si può pensare che la materia possa raggiungere una temperatura nella quale il volume è inferiore a zero). La legge quindi si esprime nel seguente modo: La variazione di volume che subisce un gas a pressione costante, in seguito alla variazione di temperatura di 1ºC, è uguale a 1/273 del volume che il gas occupa a 0°C. V = Vo(1 + a t) a =coefficiente di espansione termica, uguale per tutti i gas, 1/273,15 ℃-1 Sviluppando questa relazione si ottiene che V = kT, dove k = - TO Temperatura assoluta V=Vo (1+1 t)_ V=Vo (273,15+ t) 273,15 273,15 - V=VOT To V=k T k= Va T. 0 To= temperatura assolut corrispondente a 0℃
2ª Legge di Charles e Gay-Lussac: Legge Isocora
SECONDA LEGGE DI CHARLES E GAY LUSSAC In questo caso il pistone NON deve essere mobile. La velocità delle particelle aumenta T. V2 = V1 Raddoppiando la temperatura as- soluta, la pressio- ne raddoppia P Pz > P1 P=Po (1+ßt) P=kT k= Po To retta isocora, in cui la pendenza dipende dalla massa del gas. L'intercetta con le ordinate corrisponde alla pressione che quella massa di gas esercita ad una temperatura di 0°C. Anche in questo caso, l'intercetta con l'asse delle ascisse cade a -273,15℃. Allo zero assoluto la pressione sulle pareti è nulla. P = Po(1 + ßt), ß=coefficiente di espansione termica del gas, uguale per tutti i gas, 1/273,15 ℃ Anche P = kT, dove k = P0
P m1 Masse diverse dello stesso gas m1>m2>m3 m2 m3 PO -273,15℃ TºC Mantiene lo stesso assetto sperimentale, questa volta però il volume viene mantenuto costante e viene valutato il cambiamento di pressione all'aumentare della temperatura. Si osservò che l'aumento della temperatura del gas era direttamente proporzionale all'aumento di pressione. Graficamente (Figura 1), con T(x) e P(y) si crea una VO