Xilene e benzilalcol-deidrogenasi: caratteristiche, usi ed effetti sulla salute
Slide da De Bei - Miotto 5^aba A.s. 24/25 su Xilene. Il Pdf illustra le caratteristiche, gli usi e gli effetti sulla salute dello xilene, un composto aromatico, e descrive la benzilalcol-deidrogenasi, un enzima coinvolto nel suo metabolismo, con dettagli sulla struttura e il meccanismo catalitico, utile per lo studio della Chimica a livello universitario.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Introduzione allo Xilene
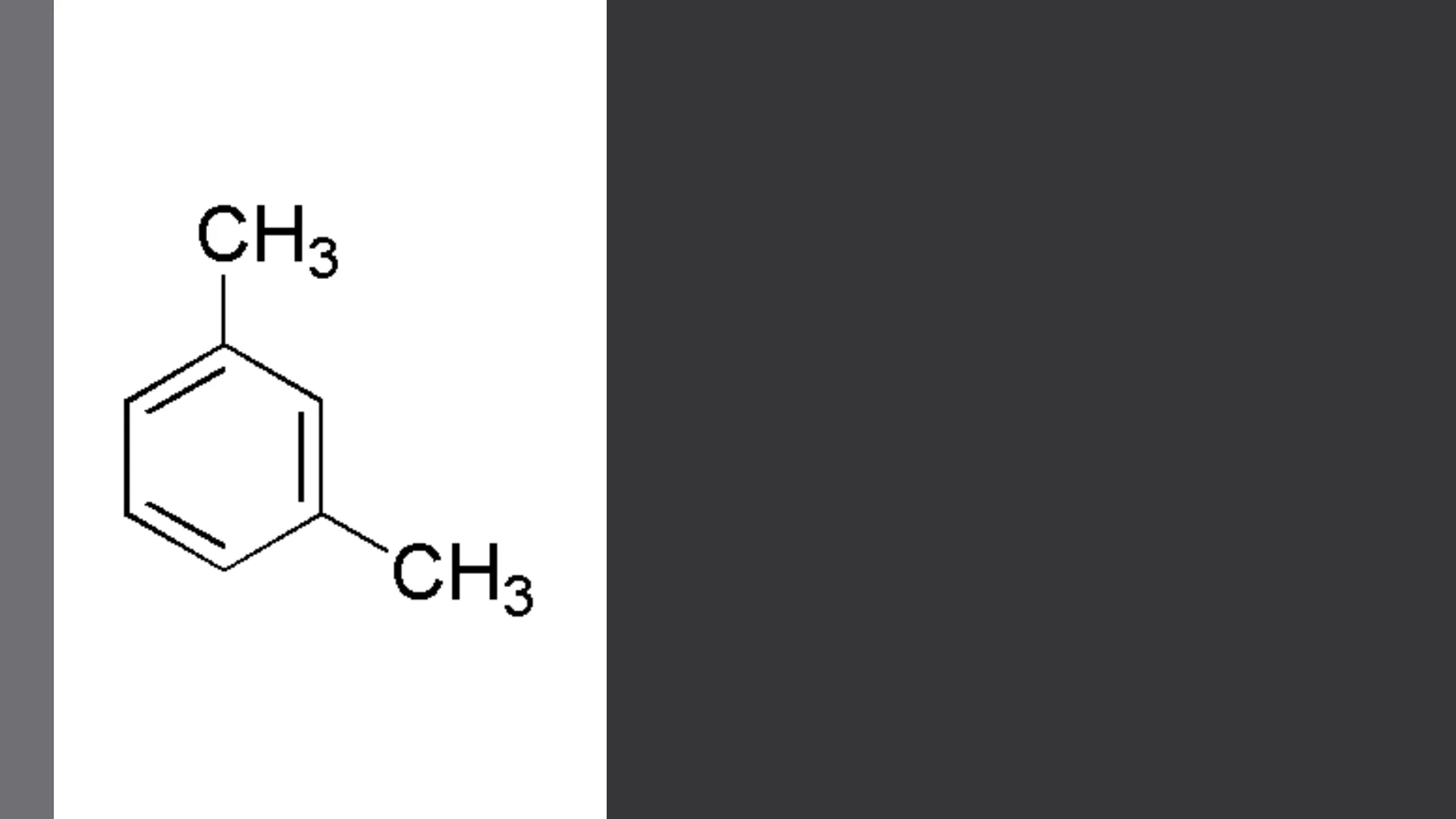
CH3 CH3 3 XILENE De Bei - Miotto 5^ABA A.s. 24/25INTRODUZIONE
- Lo xilene è un composto aromatico.
- Si trova in natura nel petrolio e nel catrame.
- Viene utilizzato nei pennarelli indelebili, come solvente nella stampa, per la lavorazione di gomme e cuoio e come diluente per le vernici.
- L'effetto principale dell'inalazione dei vapori di xilene è la depressione del sistema nervoso centrale, con sintomi quali mal di testa, vertigini, nausea e vomito arrivando a causare tumori e perdita dell'udito nei casi più gravi.
£
-
Il meccanismo di tossicità non è noto, sebbene uno studio in vitro che utilizzava membrane di cellule umane e di ratto ha dimostrato che gli xileni e altri solventi con proprietà anestetiche potrebbero legarsi alle proteine transmembrana, alterando così le loro attività.
-
La IARC ha classificato la mistura di xileni come non cancerogena per l'uomo poiché non ci sono evidenze scientifiche che suggeriscano la sua cancerogenicità.
! IRRITANTE INFIAMMABILE TOSSICO A LUNGO TERMINE
Le Tre Forme dello Xilene
Lo xilene può essere definito un aromatico bisostituito da due gruppi metilici. In quanto aromatico è presente in 3 forme: CH3 CH3 CH CH3 CH, CH3 o-xilene m-xilene 1,2-dimetilbenze 1,3-dimetilbenzene p-xilene 1,4-dimetilbenzene
Xilene Pathways
Lo xilene può percorrere differenti vie per le sue 3 diverse forme, le principali sono:
- Per l'orto-xilene la via di Bulkholdeira cepacia e del Rhodococcus
- Per il meta-xilene la via di Pseudomonas Putida
- Per il para-xilene la via di Pseudomonas Putida e del Rhodococcus
Mappa delle Vie Metaboliche
CH3 m-Xylene o-Xylene o-Xylene CH3 xylene monooxygenase p-xylene dioxygenase OH xylene monooxygenase 3-Methylbenzyl alcohol CH3 1 benzylalcohol dehydrogenase CH3 OH CH3 3,4-Dimethylcatechol 4,5-Dimethylcatechol benzyl alcohol dehydrogenase catechol 2,3-dioxygenas e 4,5-dimethylcatechol 2,3-dioxygenase OH OH 2-Methylbenzaldehyde OH --- H 4-Methylcyclohexa-3,5-dicne 1.2-ci-diol-1-carboxylate 1 benzaldehyde dehydrogenase HO O benzaldehyde dehydrogenase 2-Hydroxy-5-methyl- 6-oxohepta-2,4-dienoate 2-Hydroxy-4,5-dimethyl- 6-oxohexa-2,4-dienoate catechol 1,2-dioxygenase 4-Methylcatechol COO coo 3-Methyl-cis,cis- hexadiene dio ate HO. catechol 2,3-dioxygenase muconate cycloisomerase CH3 CH3 CO2 CO2 roxy-5-methyl-cis,cis- sonic semialdehyde OH HO O 2-hydroxymuconic emialdehyde hydrolase OH 2-Oxohex- trans-4-enoate Coo 3-Methylmucono- lactone muconate cycloisomerase CH methylmuconolactone isomerase CH3 CH3 0 COO 4-Methyl-3-oxoadipate enol-lactone 1.2-dihydroxy-3-methyl- cyclohexa-3,5-diene- carboxylate dehydrogenase -hydroxy-2-oxovalerate aldolase OH A OH 3-Methylcatechol OH CH3 p-Xylene p-Xylene CH3 CH3 CH3 -xylene 3,4-dioxygen ase o-xylene 4,5-dioxygenase xylene monooxygenase OH OH OH 2-Methylbenzyl alcohol H3C OH H3C CH3 benzaldehyde dehydrogenase HO 2-Hydroxy-3-methyl- 6-oxohepta-2,4-dienoate 0 p-Toluate C benzoate 1,2-dioxygenase CO. Carbon dioxide 4-methylcyclohexa-3,5-diene- 1,2-c8-diol-1-carboxylate dehydrogenase m-Methylbenzoate E o-Methylbenzoate CHO 4-Methylmuconolactone toluate dioxygenase toluate dioxygenase Carbon dioxide Carbon dioxide 4-methylmuconolactone methylisomerase OH 12-Dihydroxy-6-methyl- cyclohexa-3,5-diene carboxylate OH 2-oxopent-4-enoate hydratase Coo 4-Hydroxy-2- oxohexanoate CH HO OH 4-methyl-3-oxoadipate enol-lactone hydrolase OF + Pyruvate Coo OHC Propanal 4-Methyl- 3-oxoa dip ate CO. Carbon dioxide CH3 3-Methylcatechol CH3 p-Methylbenzylalcohol OH HO 3.6- Dimethylcatechol benzyl alcohol dehydrogenase 3,6-dimethylcatechol 2,3-dioxygenase p-Tolualdehyde O 3-Methylbenzaldehyde CHa .OH ₣ CH- OH Coo 1.2-Dihydroxy-3-methyl- cyclohexa-3,5-diene- carboxylate 1,2-dihydroxy-6-methyl- cyclohexa-3,5-dienecarboxylate dehydrogenase coo
Xilene Monossigenasi
XILENE MONOSSIGENASI La xilene monoossigenasi è una monoossigenasi contenente un gruppo diferro (simile alla toluene/o- xilene monoossigenasi). La proteina è formata da 500 amminoacidi, fa parte del metabolismo di Pseudomonas putida e Burkholderia cepacia ed è in comune tra i pathways di m-xilene e di o-xilene.
Sito Catalitico della Xilene Monossigenasi
La sua struttura catalitica della proteina è formata da un sito attivo ferro(II)-ferro(II) a ponte carbossilato. Gli amminoacidi che formano il sito catalitico sono glutammati e istidine che contengono gli atomi di ferro e attivano l'ossigeno per l'idrossilazione del substrato. La xilene monoossigenasi può spesso catalizzare idrossilazioni successive sui suoi substrati. Idrossilazione: reazione chimica che porta all'introduzione di gruppi idrossile (OH-) in una molecola 2
Reazione della Xilene Monossigenasi
Questo enzima catalizza l'idrossilazione di alchilbenzeni dipendente da NADH e ferredossina (Il centro attivo Fe(II)-Fe(II) coordinato da Glu/Asp e His) genera con O2 un intermedio (Fe2+-O-O-Fe2+) che ossida il gruppo metilico dello xilene, formando alcool benzilico corrispondente. Toluene + O2 + 2 ferredossine ridotte + 2 H+ -> alcol benzilico + 2 ferredossine ossidate + H2O
Dimetilcatecolo-Diossigenasi
DIMETILCATECOLO- DIOSSIGENASI La dimetilcatecolo-2,3-diossigenasi (una catecolo diossigenasi) scinde i catecoli metilati nel pathway dello xilene. È tipicamente un omotetramero (struttura formata da 4 monomeri uguali) con un singolo Fe2+ per subunità. La proteina è composta da 307 amminoacidi e fa parte del metabolismo di Rhodococcus sp. catecolo OH OH
Sito Catalitico e Reazione della Dimetilcatecolo-Diossigenasi
SITI CATALITICO E REAZIONE Il sito attivo contiene un Fe(II) legato da due istidine e un glutammato (triade 2-His-1-Glu). Sono presenti 4 siti catalitici ognuno per monomero. La catalisi della proteina porta entrambi gli atomi di ossigeni dell'O2 a reagire con il Fe(II), provocando la rottura del legame C-C tra le posizioni 2 e 3 dell'anello aromatico. L'enzima catalizza l'apertura diossigenolitica dell'anello dei catecoli: catecolo + O2 -> 2-idrossimuconato semialdeide
Benzilalcol-Deidrogenasi
BENZILALCOL- DEIDROGENASI L'alcol benzilico deidrogenasi è Appartiene alla famiglia delle alcol deidrogenasi contenenti zinco e ed in grado di convertire gli alcoli aromatici in aldeidi. Possiede due atomi di Zinco2+ e due gruppi solfati (non coinvolti nella catalisi). La benzilalcoldeidrogenasi è una deidrogenasi composta principalmente da strutture secondarie a elica, ß foglietto e frammenti random coil.
Sito Catalitico della Benzilalcol-Deidrogenasi
SITO CATALITICO Nel metabolismo dello xilene, l'alcol benzilico viene ossidato a benzaldeide da questo enzima NAD+ dipendente. Il sito attivo contiene un Zn2+ catalitico coordinato da due cisteine, una serina (o treonina) e un'istidina che facilitano il trasferimento del protone.
Reazione della Benzilalcol-Deidrogenasi
REAZIONE Durante la catalisi, l'ossigeno dell'alcol lega lo Zn, una His (o Ser) conservata rimuove un protone e un idruro viene trasferito al NAD+, producendo benzaldeide e NADH. alcol aromatico + NAD+ -> aldeide aromatica + NADH + H+
Benzaldeide Deidrogenasi
BENZALDEIDE DEIDROGENASI La benzaldeide deidrogenasi è una deidrogenasi NAD+/NADP+ dipendente che ossida le aldeidi aromatiche ad acidi. La proteina è formata da 457 amminoacidi e fa parte del metabolismo di Burkholderia cepacia.
Sito Catalitico e Reazione della Benzaldeide Deidrogenasi
SITO CATALITICO E REAZIONE Il sito catalitico è formato da una cisteina, un'asparagina e due glutammati. Nella catalisi la Cys attacca l'aldeide, NAD(P)+ riceve l'idruro, e infine Glu215 deprotona il gruppo tioestere per liberare il benzoato. benzaldeide + NAD+ + H2O -> benzoato + NADH + 2 H+ O ONa Glu337 (333) Glu337 (333) Glu337 (333) Esempio di benzoato, benzoato di sodio Cys249 (243) Cys249 (243) Cys249 (243) Asn120 (114) Asn120 (114) Asn120 (114) Glu215 (209) Glu215 (209) Glu215 (209)