Corso di Chimica per Ingegneria Biomedica, Università degli Studi Firenze
Slide dall'Università degli Studi Firenze su Corso di Chimica per Ingegneria Biomedica. Il Pdf, adatto per lo studio universitario di Chimica, illustra concetti fondamentali come la classificazione della materia e le formule chimiche, con diagrammi e modelli molecolari 3D.
Mostra di più48 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Corso di Chimica - Laurea Triennale in Ingegneria Biomedica
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE CORSO DI CHIMICA Laura triennale in Ingegneria Biomedica Giulia Serrano Dipartimento di Ingegneria Industriale Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
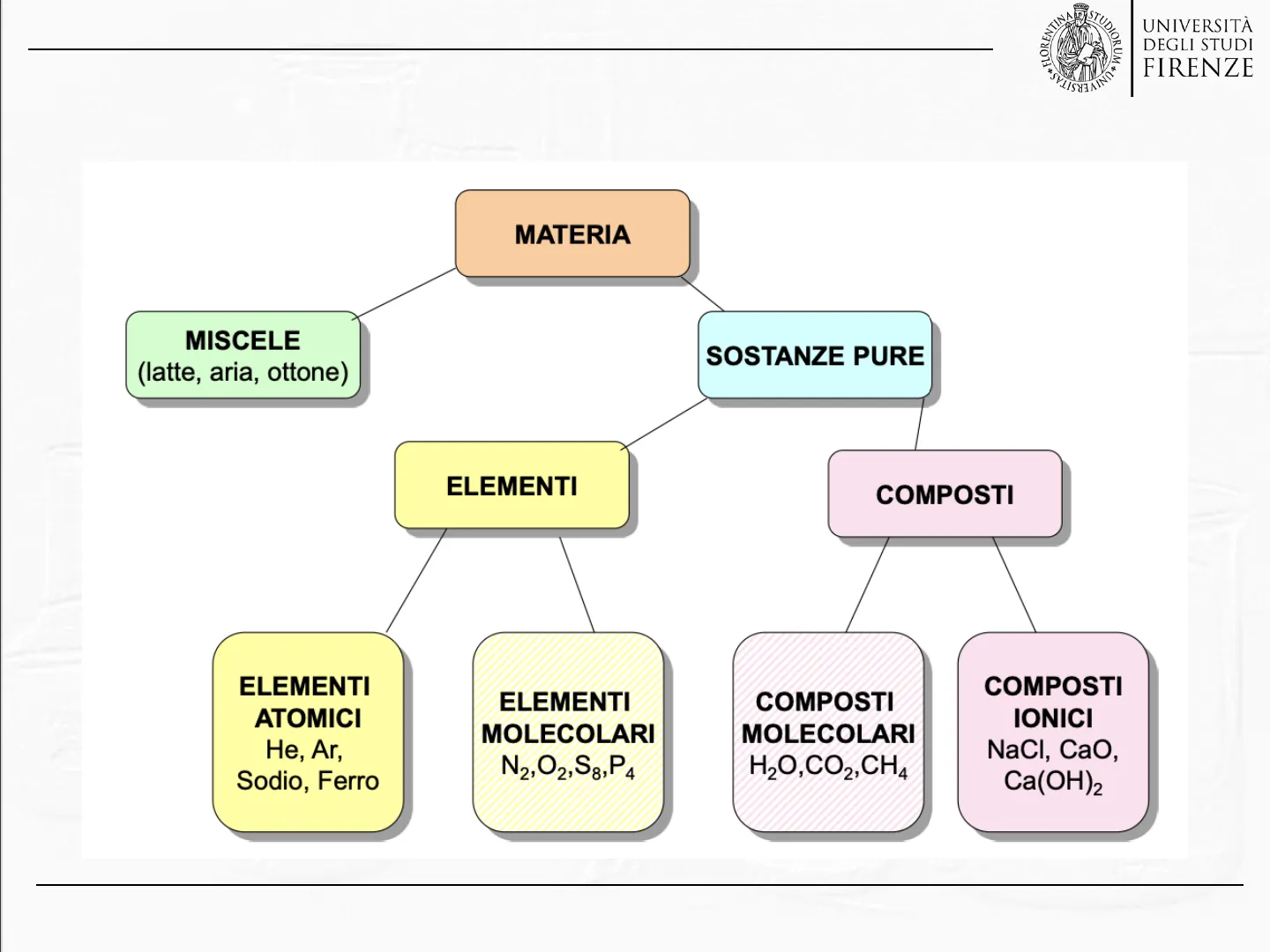
La Materia e le sue Classificazioni
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE La materia MATERIA
Miscele e Sostanze Pure
MISCELE (latte, aria, ottone) SOSTANZE PURE
Elementi e Composti
ELEMENTI COMPOSTI
Classificazione degli Elementi
ELEMENTI ATOMICI He, Ar, Sodio, Ferro ELEMENTI MOLECOLARI N2,O2,S8,P4
Classificazione dei Composti
COMPOSTI MOLECOLARI H2O,CO2,CH4 COMPOSTI IONICI NaCI, CaO, Ca(OH)2 Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Il Sistema Internazionale di Unità di Misura
STUI M + UNIVERSITAS& UNIVERSITÀ DEGLI STUDI FIRENZE Il Sistema Internazionale_prevede 7 grandezze fondamentali e ne definisce le unità di misura:
Grandezze Fondamentali e Unità di Misura
| Grandezza | Unità di misura | Simbolo |
|---|---|---|
| Intervallo di tempo | secondo | S |
| Lunghezza | metro | m |
| Massa | chilogrammo | kg |
| Temperatura | kelvin | K |
| Quantità di sostanza | mole | mol |
| Intensità di corrente elettrica | ampere | A |
| Intensità luminosa | candela | cd |
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Prefissi Moltiplicativi del SI
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE SI - PREFISSI MOLTIPLICATIVI
| Fattore | Prefisso | Simbolo | Fattore | Prefisso | Simbolo |
|---|---|---|---|---|---|
| 1024 | yotta- | Y- | 10-24 | yocto- | y- |
| 1021 | zetta- | Z- | 10-21 | zepto- | Z- |
| 1018 | exa- | E- | 10-18 | atto- | a- |
| 1015 | peta- | P- | 10-15 | femto- | f- |
| 1012 | tera- | T- | 10-12 | pico- | p- |
| 109 | giga- | G- | 10-9 | nano- | n- |
| 106 | mega- | M- | 10-6 | micro- | μ- |
| 103 | chilo- | k- | 10-3 | milli- | m- |
| 102 | etto- | h- | 10-2 | centi- | c- |
| 10 | deca- | da- | 10-1 | deci- | d- |
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Struttura Atomica della Materia
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Struttura atomica della materia
Origini della Teoria Atomica
Le origini della teoria atomica Democrito (468-370 a.c.) Epicuro (341-270 a.c.) Lucrezio (96-11 a.c.) La materia é costituita da atomi Atomos = indivisibile Lavoisier (1785) enuncia la legge di conservazione della massa Proust (1799) enuncia la legge delle proporzioni definite Dalton (1807) enuncia la legge delle proporzioni multiple Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Robert Boyle e la Chimica Moderna
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Robert Boyle (1627 - 1691) THE SCEPTICAL CHYMIST: OR CHYMICO-PHYSICAL Doubts & Paradoxes, Touching the SPAGYRIST'S PRINCIPLES Commonly call'd HYPOSTATICAL, As they are wont to be Propos'd and Defended by the Generality of ALCHYMISTS. Whereunto is præmis'd Part of another Difcourfe relating to the same Subject. BY The Honourable ROBERT BOYLE, Efq; LONDON, Printed by J. Cadwell for J. Croke, and are to be Sold at the Ship in St. Paul's Church-Yard. MDCLAI.
Contributi di Boyle alla Chimica
- Fondatore della chimica moderna.
- L'ipotesi di Boyle sosteneva che la materia è formata da atomi e raggruppamenti di atomi in movimento e che ogni fenomeno fosse il risultato della collisione di queste particelle. Boyle fece appello ai chimici affinché sperimentassero e affermò che gli esperimenti negavano il fatto che gli elementi chimici si limitassero ai soli quattro classici: terra, fuoco, aria e acqua. Boyle inoltre sostenne la necessità di separare la chimica dalla medicina e dall'alchimia, elevando questa al rango di una scienza. Soprattutto sostenne l'approccio rigoroso alla sperimentazione scientifica: egli riteneva che tutte le teorie dovessero essere dimostrate sperimentalmente prima di essere considerate vere.
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Antoine-Laurent de Lavoisier
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Antoine-Laurent de Lavoisier (1743-1794)
Principi Fondamentali di Lavoisier
- Metodo di Nomenclatura Chimica, 1787
- Legge di conservazione della massa: in una reazione chimica la massa dei reagenti è uguale alla massa dei prodotti.
- Elemento: sostanza semplice che non può essere scomposta da nessun metodo conosciuto e che è la base per la formazione dei composti chimici.
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Gli Elementi di Dalton
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE ELEMENTS. Simple Plate 5 2 4 5 G 7 G P S 10 18 0 N T L Z B 19 20 21 2º 23 24 25 96 27 28 99 30 32 33 3.4 35 36 Compound Coger with Hydrogen 37 38 39 000 Origen with Azote 41 48 43 45 € D Oxygen with Carbone and Sulphur 46 47 48 19 50 Oxygen with phosph. 57 52 53 54 55 Hyd. with Sulphe. & phosph 56 57 58 Sulphur with phosph 59 60 Gli Elementi di Dalton Lezione 01 - Introduzione 13 15 16 17 3 Hydrogen with azete & CarboneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Le Leggi Ponderali della Chimica
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Le Leggi ponderali
Legge della Conservazione della Massa (Lavoisier)
- Legge della conservazione della massa (Lavoisier) La massa totale di un sistema reagente non varia
Legge delle Proporzioni Definite (Proust)
- Legge delle proporzioni definite (Proust) In qualunque composto il rapporto fra le quantità in peso degli elementi costituenti è definito e costante
Legge delle Proporzioni Multiple (Dalton)
- Legge delle proporzioni multiple (Dalton) Quando due elementi possono combinarsi insieme in rapporti ponderali diversi per dare diversi composti, le quantità di uno di essi che nei vari casi si combina con la medesima quantità dell'altro stanno fra loro in rapporti espressi da numeri interi, generalmente piccoli
1785 1799 1807 Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Esempio: Legge di Conservazione della Massa
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Legge di conservazione della massa ioduro di potassio + nitrato di piombo Si preparano le due polveri Si mischiano le due polveri nel mortaio (avviene una reazione) S 3047 Si uniscono le polveri nel mortaio e si misura la massa. ĐÁP ĐÔNG 3047 ÉEL La massa resta la stessa Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Esempio: Legge delle Proporzioni Definite
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Legge delle proporzioni definite Esempio: Riscaldando un campione di carbonato di rame del peso di 12,4 g CO2 CuCO3 si ottengono 8 g di ossido di rame e 4,4 g di anidride carbonica calore CuO Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Esempio: Legge delle Proporzioni Multiple
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Legge delle proporzioni multiple
| g di azoto | g di ossigeno | |
|---|---|---|
| N2O | 28 | 16 |
| N2O2 | 28 | 32 |
| N2O3 | 28 | 48 |
| N2O4 | 28 | 64 |
| N2O5 | 28 | 80 |
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Teoria Atomica di Dalton
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Teoria atomica di Dalton
- Tutta la materia è costituita da particelle piccolissime, indistruttibili e indivisibili, chiamate atomi.
- Tutti gli atomi di uno stesso elemento sono identici tra loro, avendo dunque, dimensioni, massa e proprieta chimiche identiche.
- Gli atomi di un elemento non possono essere trasformati in atomi di altri elementi.
- Gli atomi di un elemento si combinano, quando formano un composto, sempre e solo con numeri interi di atomi di altri elementi.
- Gli atomi si trasferiscono sempre interamente passando da un composto ad un altro.
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Scoperta della Radioattività
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Antoine Henri Becquerel (1852 - 1908) Maria Skłodowska Curie (1867 - 1934)
Contributi di Becquerel e Curie
- Becquerel, nel corso di studi sui raggi X scoprì che Sali di Uranio emettevano raggi capaci di impressionare lastre fotografiche non esposte alla luce.
- Maria Curie prosegue questi studi e scopre che anche altri elementi presentavano la stessa capacità e coniò il nome di Radioattività.
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Le Radiazioni
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Le Radiazioni
Materiale radioattivo N Blocco di piombo S Magnete Rıggi beta Raggi gamma Lastra fotografica Raggi alfa Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
La Scoperta dell'Elettrone
STUI FI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE La scoperta dell'elettrone
Tubo di Crookes e Raggi Catodici
Tubo di Crookes 1897 Tubo in vetro contenente gas rarefatto e sottoposto ad elevate differenze di potenziale tramite due elettrodi collegati al polo positivo (anodo) e negativo (catodo) del generatore. A basse pressioni (10-6 atm) dall'elettrodo negativo (catodo) vengono emessi dei raggi detti «raggi catodici» resi visibili usando degli schermi fluorescenti, sempre identici indipendentemente dalla natura del gas e di carica negativa. A queste particelle venne dato il nome di elettroni. L'atomo e' neutro quindi devono esistere anche delle cariche positive, i protoni. Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Particelle Elementari e Radioattività
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Particelle Elementari
| Carica SI (C) | Atomico | Massa SI (kg) | Atomico | |
|---|---|---|---|---|
| Protone | 1.602x10-19 | +1 | 1.673×10-27 | 1.0073 |
| Neutrone | 0 | 0 | 1.675x10-27 | 1.0087 |
| Elettrone | -1.602x10-19 | -1 | 9.109x10-31 | 0.0005 |
Tipi di Radiazione
Radioattività
- Raggi alfa == > 2 protoni + 2 neutroni ( carica 2 +)
- Raggi beta == > Elettroni (carica 1 -)
- Raggi gamma == > Radiazioni elettromagnetiche
Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Modello Atomico di Thomson (1904)
N STUI NIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE Modello atomico di Thomson (1904)
Descrizione del Modello di Thomson
Atomo rappresentabile come una massa sferica con cariche elettriche positive uniformemente distribuite e contenente immersi nel suo interno un ugual numero di elettroni, in modo che il tutto risultasse elettricamente neutro. I + + I I + + + + I + + I Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
L'Esperimento di Rutherford
STUI UNIVERSITAS UNIVERSITÀ DEGLI STUDI FIRENZE L'Esperimento di Rutherford
Gold foil Source of alpha particles Beam of alpha particles Fluorescent screen Lead shield Nucleus Alpha particles Atoms of gold foil Ernest Rutherford (1871 - 1937) Rutherford commentò: "Era l'evento piu incredibile che fosse mai capitato nella mia vita. Era come se una granata di 15 pollici, sparata contro un pezzo di carta velina, fosse tornata indietro colpendo chi l'aveva sparata». Lezione 01 - IntroduzioneCorso di Chimica - Laurea Triennale in Ingegneria Biomedica
Modello Atomico di Rutherford (1908)
STUI ERSITAS IN UNIVERSITÀ DEGLI STUDI FIRENZE Modello atomico di Rutherford (1908)
Caratteristiche del Modello di Rutherford
Modello atomico di Rutherford Nucleo contenente particelle cariche positivamente (protoni) ed altre particelle (neutroni) Elettroni, che ruotano intorno al nucleo Modello planetario con un nucleo contenente i protoni e gli elettroni che ruotano intorno al nucleo come i pianeti intorno al sole (nuvola elettronica). Ipotizzata esistenza dei neutroni. Lezione 01 - Introduzione