Chimica Organica: Alcoli, nomenclatura e proprietà acido-base
Slide dal Politecnico Milano 1863 su Chimica Organica. Il Pdf esplora gli alcoli, la loro nomenclatura e le proprietà acido-base, con tabelle comparative di acidità e basicità, utile per lo studio universitario di Chimica.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Alcoli: Introduzione e Struttura
POLITECNICO
MILANO 1863
CMIC
dipartimento di chimica,
materiali e ingegneria chimica
"Giulio Natta"
CHIMICA ORGANICA
prof. Carlo Punta
alcoliGli alcoli
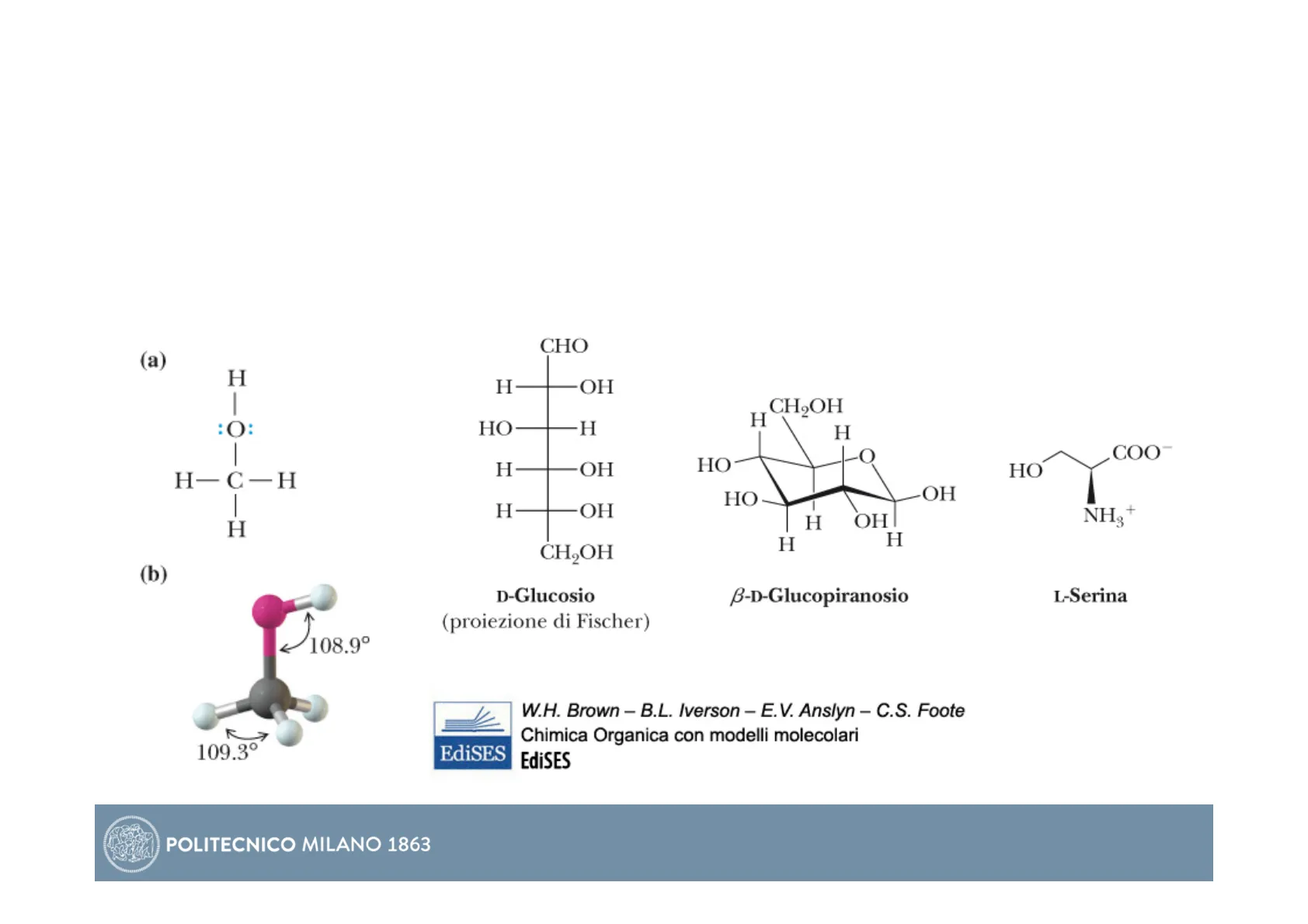
Il gruppo funzionale degli alcoli è il gruppo -OH (ossidrile) legato ad un atomo di
carbonio ibridato sp3. Anche l'ossigeno dell'alcol è ibridato sp3. Due orbitali ibridi sp3
dell'ossigeno formano legami o con il carbonio e l'idrogeno, mentre i restanti due orbitali
ibridi sp3 contengono ciascuno una coppia di elettroni non condivisa.
CHO
(a)
H
H-
-OH
:O:
HO-
-H
1
H-
-OH
H-C-H
1
H
CH2OH
(b)
D-Glucosio
(proiezione di Fischer)
-D-Glucopiranosio
L-Serina
4
108.9º
109.3º
EdiSES
W.H. Brown - B.L. Iverson - E.V. Anslyn - C.S. Foote
Chimica Organica con modelli molecolari
EdiSES
POLITECNICO MILANO 1863
Chimica Organica
2
HO
HO
OH
H -- OH
H
OH
NH3+
H
H
CHQOH
H
COO-
HO
Nomenclatura e Classificazione degli Alcoli
Nomenclatura degli Alcoli
Nomenclatura
OH
1-Propanolo
(Alcol propilico)
2-Propanolo
(Alcol isopropilico)
1-Butanolo
(Alcol butilico)
OH
-OH
OH
(S)-2-Butanolo
(Alcol (S)-sec-butilico)
2-Metil-1-propanolo
(Alcol isobutilico)
2-Metil-2-propanolo
(Alcol terz-butilico)
Classificazione degli Alcoli
Gli alcoli sono classificati come primari (1º), secondari (2°) o terziari (3º) a seconda che
il gruppo -OH sia legato ad un carbonio primario, secondario o terziario.
R-C-OH
Primario (1º)
R'
R-C-OH
H
Secondario (2°)
R'
R-C-OH
I
R"
Terziario (3º)
POLITECNICO MILANO 1863
Chimica Organica
3
H
1
I
H
OH
OH
Polioli e Composti Correlati
Dioli e Trioli
Polioli
· Dioli e trioli
OH
OH
OH
OH
HO
OH
HO
OH
HO
1,2-Etandiolo
(Glicole etilenico)
1,2-Propandiolo
(Glicole propilenico)
1,3-Propandiolo
1,2,3-Propantriolo
(Glicerolo, glicerina)
Composti con Gruppo Ossidrilico su Carbonio sp2
· composti che hanno un gruppo ossidrilico legato a un atomo di carbonio ibridato sp2
sp2 hybridized C
OH
OH
enol
phenol
POLITECNICO MILANO 1863
Chimica Organica
4
Acidità e Basicità degli Alcoli
Comportamento Acido degli Alcoli
Acidità e basicità degli alcoli
Gli alcoli possono comportarsi sia come acidi deboli (donatori di protoni)
CH3O-H +:0-H :CHO: + H-O-H
1
H
H
+
K =
[CHRO~][H3O+]
[CH3OH]
= 10-15.5
pK2 =15.5
Comportamento Basico degli Alcoli
che come basi deboli (accettori di protoni).
CH3CH2-0-H + H-OCH
H
Etanolo
Ione idrossonio
pKa-1.7
(acido più debole)
H2SO4
CH3CH2-0-H+:0-H
I
H
+
H
Ione etilossonio
pKa-2.4
(acido più forte)
Tabella Comparativa di pKa
Composto
Formula di struttura
pKa
Acido cloridrico
HCI
-7
Acido acetico
CH3COOH
4.8
Acido
più forte
Metanolo
CH3OH
15.5
Acqua
H2O
15.7
Etanolo
CH3CH2OH
15.9
2-Propanolo
(CH3)2CHOH
17
Acido
più debole
2-Metil-2-propanolo
(CH3)3COH
18
POLITECNICO MILANO 1863
Chimica Organica
5
Reazioni degli Alcoli
Formazione di Alcossidi con Metalli
Reazione degli alcoli con metalli: formazione di alcossidi
Gli alcoli reagiscono con Li, Na, K ed altri metalli liberando idrogeno, con formazione di
alcossidi. In questa reazione di ossido-riduzione, Na è ossidato a Na+ e H+ è ridotto a H2.
2 CH3OH + 2 Na -
> 2 CHO Na+ + H2
CH3CH2O"Na+
CH3
CH3CO-K+
CH3
Metossido di sodio
(MeO Na+)
Etossido di sodio
(EtO Na+)
terz-Butossido di potassio
(t-BuO"K+)
Gli alcoli possono essere convertiti in sali per reazione con basi più forti degli alcossidi.
Una di queste basi è l'idruro di sodio, NaH. Lo ione idruro, H:, la base coniugata dell'H2, è
una base estremamente forte.
CH3CH2OH
+ Na+H- - >
CHgCHQO"Na+ + H2
Etanolo
Idruro di sodio
Etossido di sodio
POLITECNICO MILANO 1863
Chimica Organica
6
Conversione in Alogenuri Alchilici
Gruppo Uscente -OH
Conversione degli alcoli in alogenuri alchilici
. Ricordare che, a differenza degli alogenuri alchilici in cui l'alogeno si comporta come buon
gruppo uscente, il gruppo OH negli alcoli è un cattivo gruppo uscente.
R-X
+
:Nu"
R-Nu +
X-
R-OH +
:Nu-
R-Nu +
-OH
. Perchè un alcol possa dare una reazione di sostituzione nucleofila, è necessario che l'OH
venga convertito in un miglior gruppo uscente. Quando un alcol è trattato con un acido, l'
"OH può essere convertito in H2O, un buon gruppo uscente.
R-OH
+
Ì-CI +
+
R-OH2
+ CI
POLITECNICO MILANO 1863
Chimica Organica
7
Reazione con Acidi Alogenidrici
Conversione degli alcoli in alogenuri alchilici: reazione con HCl, HBr e HI
. Gli alcoli terziari reagiscono rapidamente con HCI, HBr e HI.
OH +
HCI
25°C
CI
+
H2O
2-Metil-2-propanolo
2-Cloro-2-metilpropano
. Gli alcoli primari e secondari insolubili in acqua reagiscono molto lentamente con HCI.
. Gli alcoli primari e secondari possono essere trasformati in bromoalcani e iodoalcani
per trattamento con HBr e HI.
· Gli alcoli secondari danno una certa percentuale di prodotti di trasposizione, prova
della formazione di intermedi carbocationici durante la reazione.
OH
Br
+ HBr
->
+
+ H2O
calore
Br
Br
OH
+
HBr
a
2,2-Dimetil-1-propanolo
2-Bromo-2-metilbutano
(un prodotto di trasposizione)
POLITECNICO MILANO 1863
Chimica Organica
8
+
H2O
B
Reazione SN1 di Alcoli Terziari con HBr
Reazione di un alcol terziario con HBr - Una reazione SN1
1. Protonazione
H-0:+H-Br :- >H-O-H+:Br:
1
H
CH3
H
6
-
CH3-C-O:
+ :0-H
+
H
I
H
CH3
Uno ione ossonio
2. Formazione del
carbocatione
CH3
I
I
CH3
/
CH3-C-OF
+
/
SN1
1
I
CH3
CH3
H
CH3-C+ + :0:
H
Un carbocatione 3°
intermedio
CH3
1
..
CH3-C-Br:
1
CH3
2-Bromo-2-metilpropano
(Bromuro di terz-butile)
POLITECNICO MILANO 1863
Chimica Organica
9
H
CH3
rapido e
reversibile
CH3-C-O-H + H-O-H
-
CH3
H
2-Metil-2-propanolo
(Alcol terz-butilico)
lento,
cineticamente
determinante
H
H
3. Formazione del legame
con l'alogenuro
CH3-C+ + : Br:
..
I
1
..
CH3
CH3
veloce
Reazione SN2 di Alcoli Primari con HBr
Reazione di un alcol primario con HBr - Una reazione SN2
1. Protonazione
rapido e
reversibile
H
.. +
O-H +H-O-H
O
+ :0-H
I
I
H
H
Uno ione ossonio
2. Sostituzione nucleofila bimolecolare
H
lento,
cineticamente
determinante
: Br :
H
.
+ :0
I
I
H
H
POLITECNICO MILANO 1863
Chimica Organica
10
..
+
: Br: +
..
O
SN2
Trasposizione nelle Reazioni di Sostituzione
Trasposizione
Gli alcoli secondari reagiscono secondo entrambe i meccanismi dando luogo a miscele.
Nel caso della formazione di carbocationi è possibile la trasposizione.
Gli alcoli primari ramificati in posizione ß reagiscono secondo un meccanismo che
comporta la formazione di un carbocatione 3º, generato per perdita di una molecola di
acqua e contemporanea migrazione di un gruppo alchilico.
H
lento,
cineticamente
determinante
+
H
(concertato)
1
H
H
Un carbocatione 3º
intermedio
..
: CI
+
..
veloce
:C1: +
2-Cloro-2-metilbutano
POLITECNICO MILANO 1863
Chimica Organica
11
+ :0:
Disidratazione Catalizzata da Acidi: Sintesi di Alcheni
Condizioni e Facilità di Disidratazione
Disidratazione catalizzata da acidi degli alcoli: sintesi di alcheni
Un alcol può essere convertito in un alchene per disidratazione (cioè eliminazione di una
molecola d'acqua da due atomi di carbonio adiacenti).
· Si riscalda un alcol in presenza di acido fosforico all'85% o di acido solforico concentrato.
· Gli alcoli primari sono i più difficili da disidratare (180℃).
· Gli alcoli secondari subiscono la disidratazione catalizzata da acidi a temperature inferiori
(100-150℃)
. Gli alcoli terziari reagiscono a temperature appena superiori a quella ambiente.
alcol 1° <
alcol 2° <
alcol 3º
Facilità di disidratazione degli alcoli
CH3CH2OH
H2SO
180°℃
CH2=CH2 + H2O
CH3COH
CH3
1
CH3
H2SO4
50°℃
CH3
CH3C=CH2 + H2O
OH
H2SO4
140°C
+ H2O
Cicloesanolo
Cicloesene
2-Metil-2-propanolo
(Alcol terz-butilico)
2-Metilpropene
(Isobutilene)
POLITECNICO MILANO 1863
Chimica Organica
12
Regioselettività della Disidratazione
Disidratazione catalizzata da acidi degli alcoli: regioselettività
In generale prevale la formazione dell'alchene che ha il maggior numero di sostituenti
sul doppio legame, cioè l'alchene più stabile (regola di Zaitsev).
1
8
4
2
H2SO4
+
+ H2O
OH
3-Metil-2-butanolo
(racemo)
2-Metil-2-butene
(prodotto principale)
3-Metil-1-butene
H2SO4
+
2-Metilciclopentanolo
(racemo)
1-Metilciclopentene
(prodotto principale)
3-Metilciclopentene
(racemo)
Possibilità di trasposizione ...
H2SO4
140°-170℃
+
OH
3,3-Dimetil-2-butanolo
(racemo)
2,3-Dimetil-2-butene
(80%)
2,3-Dimetil-1-butene
(20%)
POLITECNICO MILANO 1863
Chimica Organica
13
Meccanismo E1 della Disidratazione
Disidratazione catalizzata da acidi - Una reazione E1
H
H
H
0:
O
rapido e
reversibile
+
+
HO-H
+ :0-H
H
1
H
H
O
lento,
cineticamente
determinante
+
+ H20:
Un carbocatione 2°
intermedio
3. Eliminazione di un protone
+
rapido e
reversibile
H-O: +
+
+
.. +
H-O-H
1
H
>H H
H
NB H+ è un catalizzatore ...
POLITECNICO MILANO 1863
Chimica Organica
14
1. Protonazione
2. Formazione del carbocatione
C
Trasposizione nella Disidratazione Acido-Catalizzata
Disidratazione catalizzata da acidi - trasposizione
H2O
+ H3O+
H+
-H2O
+
-
2,3-Dimetil-
2-butene
OH
3,3-Dimetil-2-
butanolo
(racemo)
Un carbocatione 2º
intermedio
Un carbocatione 3º
intermedio
+
H3O+
H2O
2,3-Dimetil-
1-butene
POLITECNICO MILANO 1863
Chimica Organica
15
Disidratazione di Alcoli Primari
Disidratazione catalizzata da acidi di alcoli primari
Gli alcoli primari aventi poche o nessuna ramificazione in posizione ß danno origine, per
disidratazione acido-catalizzata, a un alchene terminale e ad alcheni trasposti.
OH
H2SO4
140°-170℃
+
+
1-Butanolo
trans-2-Butene
(56%)
cis-2-Butene
(32%)
1-Butene
(12%)
La formazione di questi prodotti è il risultato di una combinazione dei meccanismi E1 ed E2.
.. +
E2
H-0:+
1->H-O-H+
..
+
+ : 0-H
H H
H
H
1-Butene
H
H
E1
.. +
E1
H-O: +
+
+
+ H-O-H
H
trans-2-Butene
cis-2-Butene
shift-1,2 di uno
ione idruro
+
+ :0-H
H H
H
H
Un carbocatione 2°
POLITECNICO MILANO 1863
Chimica Organica
16
.. +
GO-H
-
trasposizione
2
Ossidazione degli Alcoli
Ossidazione di Alcoli Primari
Ossidazione degli Alcoli
Gli alcoli sono ossidati a una varietà di composti carbonilici. Nell'ossidazione un legame C-H
viene sostituito con un legame C-O
1. Un alcol primario dà aldeidi o acidi carbossilici
H
[O]
R
H
C=O
or
C=O
-
HO
2 C-H bonds
1º alcohol
aldehyde
carboxylic acid
Ossidazione di Alcoli Secondari
2. Un alcol secondario dà chetoni
R
R
[O]
R-C-OH
C=0
1 C-H bond
H
2° alcohol
R
ketone
Ossidazione di Alcoli Terziari
3. Gli alcoli terziari non vengono ossidati.
[O]
no C-H bonds
R-C-OH
R
R
NO REACTION
3º alcohol
POLITECNICO MILANO 1863
Chimica Organica
17
R
R/C-OH
H