Miscele e soluzioni in chimica: tipologie, soluto, solvente e molarità
Slide sulle miscele e soluzioni in chimica. Il Pdf, adatto per la scuola superiore, esplora le diverse tipologie di miscele, i concetti di soluto, solvente e molarità, con esempi pratici per il calcolo, rendendo il materiale utile per l'apprendimento.
Mostra di più67 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Miscele e Soluzioni
I composti possono trovarsi in natura o allo stato puro o in miscele con altri Le miscele biologicamente più importanti sono quelle liquide Le miscele di liquidi possono essere di 4 tipi: soluzioni, sospensioni, colloidi ed emulsioni
Putzig Nitrato di Nichel (solido) in acqua si scioglie formando una soluzione omogenea
Birra: liquido (alcol), solido (malto), gas (CO2) sciolti in acqua
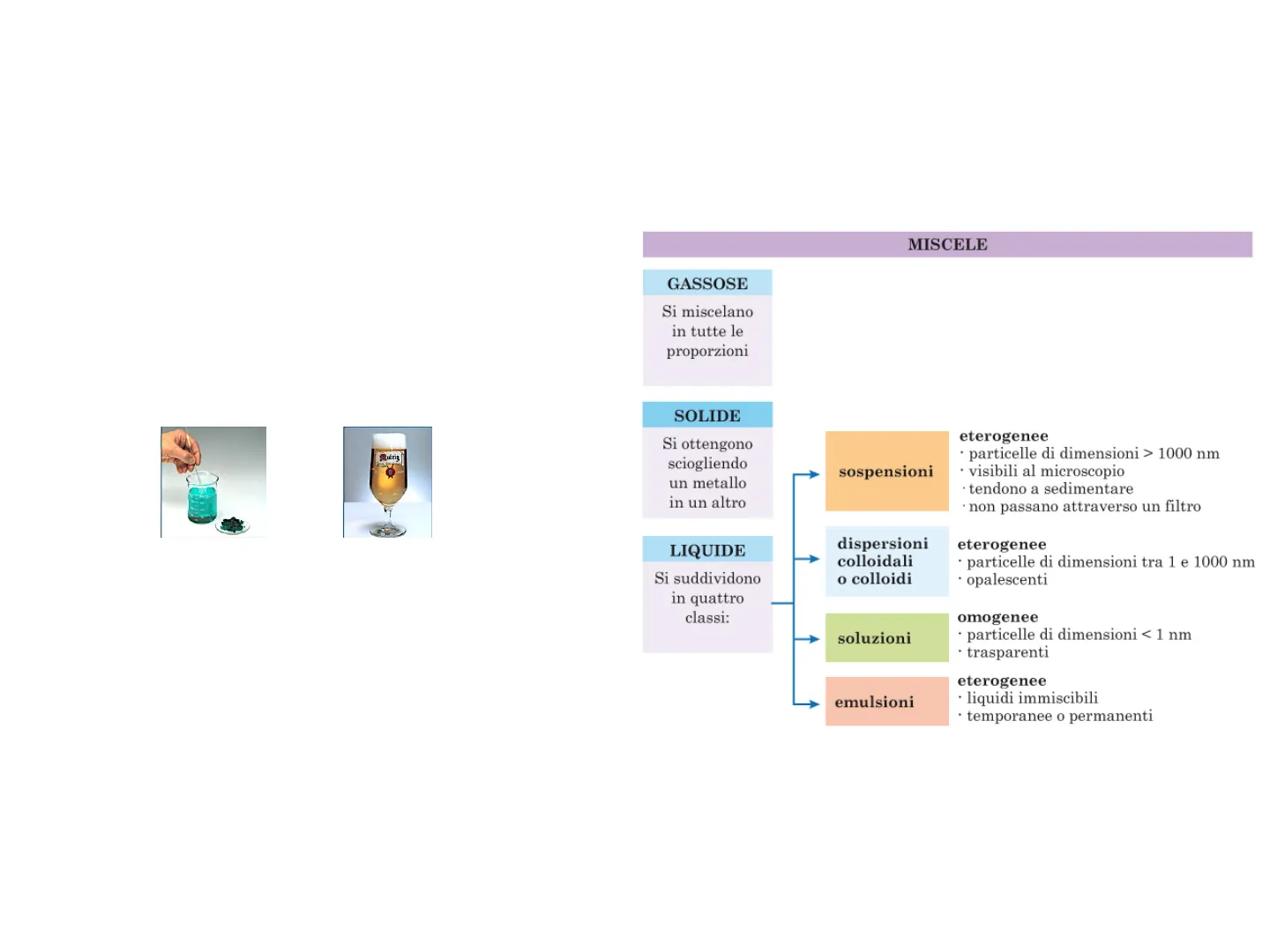
Tipi di Miscele
Miscele Gassose
Si miscelano in tutte le proporzioni
Miscele Solide
eterogenee Si ottengono sciogliendo un metallo in un altro
Miscele Liquide
Sospensioni
- particelle di dimensioni > 1000 nm
- visibili al microscopio
- tendono a sedimentare
- non passano attraverso un filtro
Dispersioni Colloidali o Colloidi
eterogenee
- particelle di dimensioni tra 1 e 1000 nm
- opalescenti
Soluzioni
omogenee
- particelle di dimensioni < 1 nm
- trasparenti
Emulsioni
eterogenee
- liquidi immiscibili
- temporanee o permanenti
Si suddividono in quattro classi:Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole.
Differenza con i colloidi che differiscono in quanto le particelle sono più grandi delle molecole normali ma non ancora visibili al microscopio (1 - 1000 nm).
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
Il solvente è il componente presente in quantità maggiore o che determina lo stato della materia in cui la soluzione esiste.
Il soluto è un componente presente in quantità minore.Il caso più comune è quello di soluzioni liquide (soluzioni di gas, solidi o liquidi sciolti in un liquido).
Si possono però avere:
- Soluzioni gassose: in genere i gas possono mescolarsi in tutte le proporzioni per dare soluzioni gassose.
- Soluzioni liquide: sono le più comuni e sono ottenute nella maggior parte dei casi sciogliendo un gas o un solido in un liquido. Sono comuni anche le soluzioni liquido-liquido (possono non essere miscibili in tutte le proporzioni).
- Soluzioni solide: sono principalmente leghe di due o più metalli. Le leghe di mercurio (l'unico metallo liquido) con altri metalli sono chiamate amalgame e possono essere sia liquide che solide).
Soluzioni Liquide
Le soluzioni liquide più presenti nei sistemi biologici sono soluzioni omogenee
Soluzione: miscela omogenea di due o più sostanze distribuite uniformemente l'una nell'altra
Una soluzione liquida consiste di 2 componenti:
- soluto: può essere una sostanza solida, liquida o gassosa
- solvente: in genere è una sostanza liquida nella quale si scioglie il soluto
Aggiungendo sale all'acqua questo si scioglie pur se aggiunto più volte, formando soluzioni a diversa concentrazione di sale Dunque le soluzioni, pur se formate dagli stessi elementi, hanno composizione variabile (soluzioni di acqua salata a diverse concentrazioni di sale).
Concetto analogo vale per altri soluti solubili in acqua (zucchero, solfato di Rame, nitrato di Nichel, etc.). Il risultato sarà sempre una soluzione limpida, solo che mentre con sale e zucchero sarà anche incolore, con altri composti come il CuSO4 ed il Ni(NO3)2 risulteranno limpide e colorate (limpido = trasparente alla luce).
Lasciando le soluzioni così formate a riposo per un certo periodo di tempo, più o meno lungo, il soluto resta disciolto e non precipita nuovamente sotto forma di Sali, ossia non sedimenta (a meno che il solvente non evapori).
Perché le Sostanze si Sciolgono?
Le soluzioni sono miscugli omogenei di due o più sostanze e possono essere solide, liquide o gassose.
Si formano a causa dell'agitazione termica delle particelle.
200 Linava 150 50 100 ImDay 50 A B C Valitutti, Falasca, Amadio Lineamenti di chimica @ Zanichelli editore 2019
La Concentrazione delle Soluzioni
Satura
Soprasatura
germe cristallino
FIGURA 11.23 Le soluzioni soprasature tendono ad essere sensibili. Raffreddandole troppo rapidamente o agitando il recipiente, si causa la formazione di solido. Anche l'aggiunta di un piccolo cristallo (o un granello di polvere) che funge da germe di cristallizzazione può far sì che una soluzione soprasatura omogenea si porti allo stato di soluzione satura con solido presente in eccesso.
Proprietà delle Soluzioni Liquide
Le proprietà fondamentali delle soluzioni possono essere così riassunte:
- Sono costituite da una o più sostanze solubili (soluto) disciolte in una sostanza liquida (solvente)
- Hanno composizione variabile
- Sono trasparenti alla luce
- Sono omogenee
- Non presentano sedimentazione
- Possono essere separate nei loro componenti mediante metodi fisici
- Passano attraverso la carta da filtro senza separarsi nei loro componenti
Solubilità
In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con un eventuale solido in eccesso.
Equilibrio dinamico (a) (b) (c)
La concentrazione del soluto nella soluzione satura è detta solubilità. Ad esempio la solubilità di NaCl in acqua è di 36 g per 100 ml di acqua a 20° C.
Dipendenza dalla Polarità
La solubilizzazione di un soluto in un solvente dipende dalla loro polarità o apolarità
La solubilità (s) è la quantità massima di un soluto che a una data temperatura si scioglie in una determinata quantità di solvente.
Una soluzione che a una data temperatura contiene:
- una quantità di soluto inferiore a s, si dice insatura;
- una quantità di soluto uguale a s, si dice satura.
Un solido è solubile in un solvente se ha un valore alto di solubilità; è insolubile se il valore è molto piccolo.
Posca, Fiorani Chimica più.verde @ Zanichelli editore 2020
Influenza del Legame e Solvatazione
La solubilità è influenzata dal tipo di legame che unisce le sostanze coinvolte.
Nella formazione di una soluzione, le molecole di solvente (componente in proporzione maggiore) circondano le molecole di soluto (componente in proporzione minore).
Tale fenomeno è chiamato solvatazione.
Quando il solvente è l'acqua, la solvatazione prende il nome di idratazione.
L'Acqua
L'acqua (H2O) quando è pura (bidistillata) non conduce elettricità Questo indica che l'acqua è formata da molecole con atomi legati fra loro solo mediante legami covalenti Gli atomi che formano la molecola dell'acqua non sono disposti in maniera lineare, ma formano un angolo di legame di circa 105° (con esattezza 104,45°)
x = elettroni dell'idrogeno (H) H &O X - H · = elettroni dell'ossigeno (O) 8 0 1 8+ H 104.45° 8+H. .. XO: H H H H O O 105° H + O H H ( 0 O H H H O O + + - H O O H - + + O H H O + - + - + 1 H - + - + - + H H - + - + - H
A causa della maggiore elettronegatività dell'O questo attrae la nuvola elettronica più dell'H Questa ineguale distribuzione delle cariche fanno si che questa molecola sia definita polare Dunque, l'acqua è una molecola polare, per cui può fungere da solvente per molte altre sostanze polari, composti ionici, etc. Composti ionici come NaCl si solubilizza in acqua perché le molecole di acqua esercitano una forza di attrazione verso gli ioni e li separano formando una sorta di guscio intorno ad essi (ioni idratati o solvatatì) -> Na+ (ag) e Cl (aq)
H H F O O H H + - + 8+ H . X H
Idrolisi
Un sale di ammonio (es .: Cloruro d'ammonio) viene messo in acqua si ha una reazione di idrolisi NH4+(ag) + H2O 4 (ac NH3(aq) + H3O(ag)
In una reazione di idrolisi viene rotto un legame covalente (in questo caso il legame tra azoto e idrogeno) per intervento di una molecola d'acqua Il Saccarosio durante la digestione viene idrolizzato enzimaticamente a Glucosio e Fruttosio
enzima C12H22O11 + H2O C6H12O6 + C6H12O6
Nel nostro organismo anche altre macromolecole come i grassi (acidi grassi e glicerolo), le proteine (amminoacidi)
Concentrazione di una Soluzione
In generale la concentrazione di una soluzione è una misura della quantità di soluto presente in una data quantità di solvente (o di soluzione).
C = Quantità di soluto Quantità di solvente
La quantità di soluto o di solvente possono essere espresse in massa, numero di moli o volume per cui vi sono diversi modi di esprimere la concentrazione di una soluzione:
- Percentuale in massa (P/P, V/V, P/V)
- Molarità
- Molalità
- Parti per milione
- Normalità
Percentuale in Massa di Soluto
E' definita come:
% massa di soluto = massa di soluto ×100 massa della soluzione
Il rapporto m /m soluto soluzione esprime i grammi di soluto in un grammo di soluzione.
Ad esempio: che concentrazione ha una soluzione ottenuta mescolando 10 g di NaCl in 150 g di acqua?
% massa NaCl= 10 g ×100=6,25% 150g+10g
Tale soluzione contiene 6,25 g di NaCl per 100 g di soluzione
Percento in Peso NaCl al 2% (p/p)
Dire che una soluzione acquosa di NaCl è al 2% in peso significa che in 100 g della soluzione ci sono 2 g di NaCl (e 98 di acqua).
2 g NaCl + 98 g H2O 15
Percento in Peso NaCl allo 0.9% (p/p)
La soluzione fisiologica di NaCl ha una concentrazione dello 0.9% in peso.
0,9 g NaCl + 99,1 g H2O 16
Questo significa (moltiplicando x 10) che in 1 kg di soluzione sono contenuti 9 g di NaCl.
Percento in Peso Saccarosio al 10% (p/p)
10 g saccarosio + 90 g H2O 17
In 1 kg di una soluzione acquosa di saccarosio al 10% sono contenuti 100 g di saccarosio.
Percentuale in Volume di Soluto
La concentrazione percentuale in volume (% V/V) indica il volume in millilitri di soluto sciolto in 100 ml di soluzione.
V. soluto (mL) % V/V = V soluzione (mL) · 100
Il grado alcolico di una bevanda corrisponde ai millilitri di alcol disciolti in 100 ml di bevanda.
Calcolo Percentuale in Volume
Si usa di solito quando dei liquidi sono disciolti in altri liquidi, dato che è facile misurare la quantità di liquidi in base al loro volume
Volume di soluto (mL) Percentuale in volume X 100% Volume di soluzione (mL)
Sciogliamo 12.5 ml di EtOH in acqua sufficiente a dare un volume totale di 85,4 ml. Qual è la concentrazione dell'EtOH espressa in percentuale in volume?
12.5 ml EtOH Percentuale in volume = X 100% = 14.6 % 85.4 ml soluzione
Il grado alcolico di una bevanda corrisponde agli mL di alcool disciolti in 100 ml di bevanda.
Percentuale Peso/Volume di Soluto (%P/V)
E' il numero di grammi di soluto presenti in 100 ml di soluzione.
Percentuale massa su volume = grammi di soluto X 100% Volume di soluzione (mL)
Sciogliamo 40 g di KCl in acqua sufficiente a dare un volume totale di 500 ml. Qual è la concentrazione del KCl?
Percentuale in volume = 40 g X 100% = 8 % 500 mL