Gruppi funzionali in chimica organica: nomenclatura, proprietà e reazioni
Schemi sui Gruppi Funzionali. I Riassunti esaminano alogenuri alchilici, alcoli, eteri, ammine e tioli, con focus sui meccanismi di reazione SN1 e SN2. Questo materiale di Chimica per Università è presentato in schemi e tabelle riassuntive, facilitando la comprensione e la memorizzazione dei concetti chiave.
Mostra di più9 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Gruppi funzionali
2 02
Classificazione e Nomenclatura
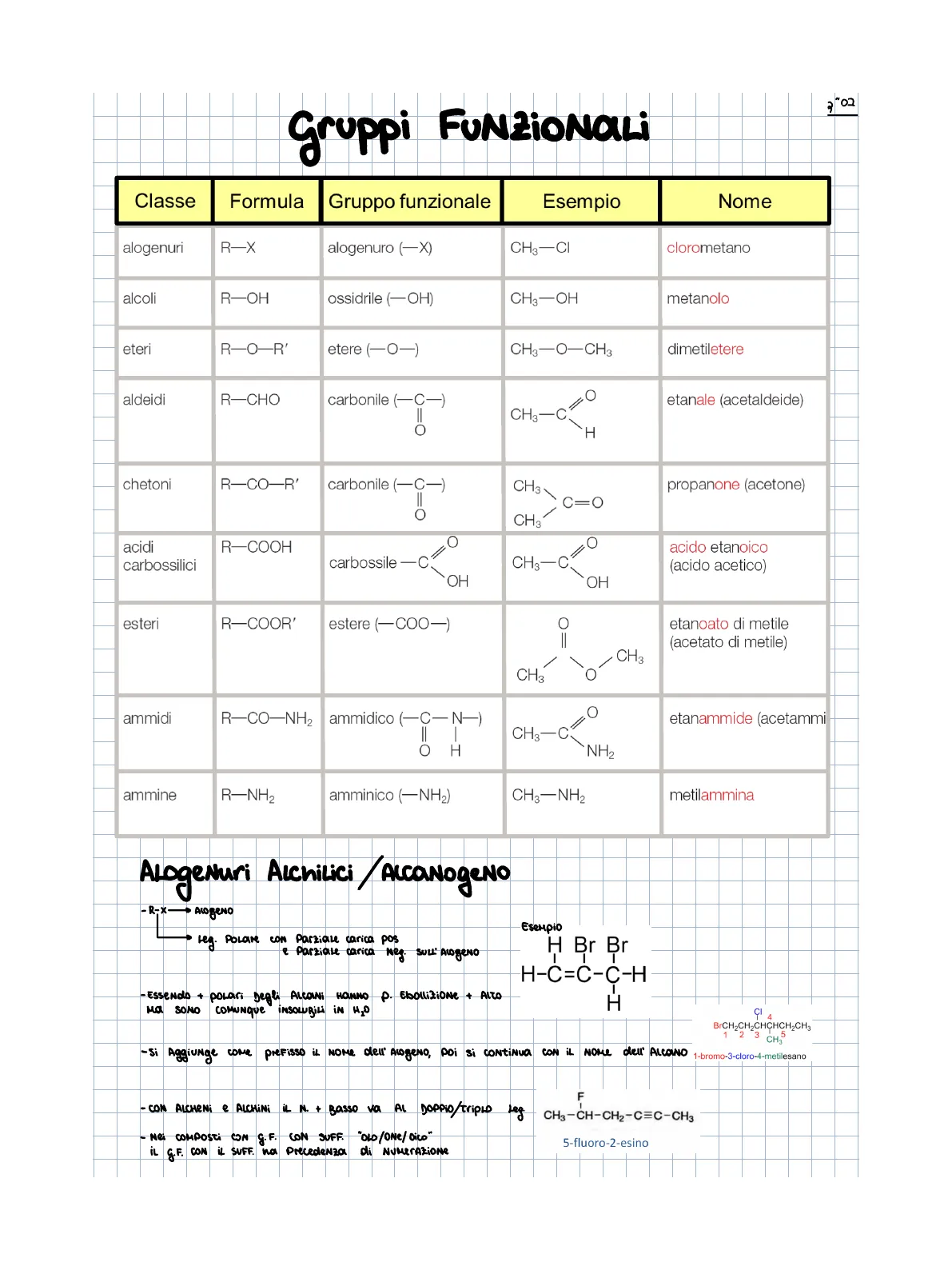
Classe Formula Gruppo funzionale Esempio Nome alogenuri R-X alogenuro (-X) CH3-CI clorometano alcoli R-OH ossidrile (-OH) CH3-OH metanolo eteri R-O-R' etere (-0-) CH3-0-CH3 dimetiletere aldeidi R-CHO carbonile (-C-) CH3-C=0 `H etanale (acetaldeide) chetoni R-CO-R' carbonile (-C-) II Ő CH3 C=0 propanone (acetone) CH3 acidi carbossilici R-COOH carbossile -c" OH C CH3-C=0 OH acido etanoico (acido acetico) esteri R-COOR' estere (-COO-) C CH3 CH3 O etanoato di metile (acetato di metile) ammidi R-CO-NH2 ammidico (-C-N-) OH CH3-C? NH2 etanammide (acetammi ammine R-NH2 amminico (-NH2) CH3-NH2 metilammina
Alogenuri Alchilici / Alcanogeno
Proprietà degli Alogenuri Alchilici
- R-X- AlogeNO
- Leg. Polare CON Parziale carica pos e Parziale carica Neg. SULL' AcogeNo
Esempio H Br Br H-C=C-C-H -Essendo + polari Degli AlCONi Ma SONO COMUNQUE INSOLUBILi İN H2O HONNO P. Ebollizione + ALTO
Nomenclatura degli Alogenuri Alchilici
H CI 4 BrCH2CH2CHCHCH2CH3 1 2 3 CH3 .5 - Si Aggiunge come preFisso il NOME dell' AcogeNo, Poi si CONTINUA CON IL Nome dell' ALCONO 1-bromo-3-cloro-4-metilesano - CON ALCHENI e ALCHINi Basso va AL DOPPIO/Triplo Leg. F CH3-CH-CH2-C=C-CH3 "OLD/ONE/Dico" İL G.F. CON IL SUFF. - Nei COMPOSTI CON G. F. CON SUFF. Precedenza di NUMERAZIONE 5-fluoro-2-esino
Reazioni degli Alogenuri Alchilici
Tipi di Reazioni
O2 02 Reazioni
- DANNO SOSTITUZIONE NUCLEOFiLa ALOgeNO esce e entra UN ALTRO G.
- ELIMINAZIONE NUCLEOFiLa Ad ANiONE Si sosTUisce ANIONe, sempre NUCLEOFILO
- Formazione COMPOSTi Organo Metallici
Sostituzione Nucleofila (SN1 e SN2)
La SOSTITUZIONE NUCLEOFiLa si Divide IN SN1 & SN2 SN1: - CON ALOgenUri terziari, MOLTO ingombranti - Si Divide IN 2 Stadi: Lento e veloce - NEL LENTO: Si Forma il cargocazione staccando l'alogeNo - Nel veloce: AL cargocazione si Attacca L'UNIONE ENTrante se L'aNiONE ENTrante Si Attacca AL C Chirale, La Miscela C' Detta RaceMica SN.2: - CON ALOgenUri PriMari o secondari, Che SONO MENO ingombranti Questo è perché Ossia Avviene IN 1 l' BiMolecolare Fase sola - Quello ENTra, SFratta l'altro Automaticamente chiama : INVersione di CONFigurazione "CONVIVONO" ENTramBi [se il C è chirate DA R diventa s] - per UN Breve tempo IN UNO stato di Transizione, Che Nel grafico e' il PUNTO (energetico) + ALTO
Fattori che influenzano la Sostituzione Nucleofila
La sostituzione NUCLEOFILA È' INFLUENZATO da:
- struttura dell'alogenuro alchilico
- struttura del nucleofilo
- gruppo uscente
- solvente
Influenza della Struttura dell'Alogenuro Alchilico
SN1 Stabilità del carbocatione mai attraverso SN1 R&CX RoCHX RCH2X CH X (3º) (2° (1º) (metilico) mai attraverso SN2 Acceso al sito di reazione Sy2 Governata da fattori sterici Le reazioni SN1 sono influenzate da fattori elettronici, come la stabilità del carbocatione. Un carbocatione terziario è più stabile e quindi gli alogenuri alchilici terziari reagiscono più facilmente rispetto ai secondari. Il carbocatione degli alogenuri alchilici primari è troppo instabile e non reagisce mai con reazione SN1. Le reazioni SN2 sono influenzate da fattori sterici. Minore sarà l'ingombro dei gruppi già presenti, più facile sarà l'accesso del nucleofilo e alta la velocità di reazione. Gli alogenuri alchilici primari hanno l'ingombro minore e reagiscono sempre con meccanismo SN2
Efficacia dei Nucleofili
TABELLA 16.2 Esempi di nucleofili comuni e loro efficacia relativa
Efficacia Nucleofilo (Br", I" Buono( CH3S", RS" HO", CHỊO", RO" Aumento della nucleofilicità O La tabella mostra che le specie cariche negativamente sono nucleofili migliori di quelle neutre Medio( CH3CO", RCO" CH3SH, RSH, ROS NH3, RNH2, R2NH, RN H2O CHỊOH, ROH Scarso O O= CH3COH, RCOH La nucleofilicità relativa è diversa nei vari nucleofili. Le specie cariche sono più nucleofile che le specie neutre. Questo influisce sulla velocità di reazione. La nucleofilicità è una proprietà cinetica Principalmente le reazioni SN2 sono influenzate dalla nucleofilicità del nucleofilo 1 1 1 come nucleofilo O= Governata da fattori elettronici2 "02
Stabilità del Gruppo Uscente
La stabilità come anione del gruppo uscente influenza il processo di sostituzione nucleofila, sia SN1 che SN2. Gruppi uscenti più stabili sono le basi coniugate di acidi forti. R-F R-CI < R-Br < R-I Aumento velocità di reazione
Influenza del Solvente
TABELLA 16.3 Comuni solventi protici
Solvente protico Polarità Struttura del solvente Note Acqua H2O Acido formico HCOOH Metanolo CH3OH Etanolo CH3CH2OH Acido acetico CH3COOH Questi solventi favoriscono reazioni SN1. Maggiore è la polarità del solvente, più facilmente si forma in esso il carbocatione perché sia il carbocatione, sia il gruppo uscente carico negativamente sono solvatati. Solventi che contengono gruppi -OH (solventi protici) sono donatori di legami idrogeno e favoriscono le reazioni SN1
TABELLA 16.4 Comuni solventi aprotici
Solvente aprotico Polarità Struttura del solvente Note O Dimetilsolfossido (DMSO) CH3SCH Crescente Questi solventi favoriscono reazioni SN2. Pur essendo i solventi in alto piuttosto polari, la formazione di carbocationi in essi è di gran lunga più difficile che in solventi protici perché il gruppo uscente non può essere solvatato da questi solventi. Solventi che NON contengono gruppi -OH (solventi aprotici) favoriscono le reazioni SN2 anche se sono polari
Eliminazione Nucleofila
Caratteristiche dell'Eliminazione Nucleofila
ELIMINAZIONE NUCLEOFiLa
- La FANNO Tutti quelli che POSSONO Rimuovere UN ELETTROFILO
- P ELIMINAZIONE perché Avviene A Livello di UN C B, UN C INTERNO
- GeneraLmente Avviene İN AMBIENTE BASICO La BASE "stacca" e Favorisce i Leg. Ad H
- Si Divide iN E1 E2
Meccanismi E1 e E2
È' MONOMOLECOLARE e Avviene Negli AlogenUri BiMolecolare, terziari, + INGOMBRANTI FUNZIONA COME LO SN2 エ ー x- R R FUNZIONA COME La SN1 R-C-C-R + B 'c=C + H-B+ + X" R R R R - IL Risultato di questa Reazione è SEMPre UN ALCheNe
Eliminazione E1
Eliminazione E1: la rottura del legame C-X avviene prima della reazione che porta alla perdita dell'idrogeno. La velocità dipende solo dall'alogenoalcano v = k[alogenoalcano]
( Br CH3-C-CH3 CH3 stadio lento Formazione carbocatione (come SN1) CH3-Č-CH3 + Br CH H2O H + CH2-C-CH3 1- CH3 CH2=C-CH3 + H3O+ - CH3 Un protone viene ceduto ad una base O= Acetone CH3CCH3 Diclorometano CH2Cl2 Etere dietilico (CH3CH2)2O Crescente Base2"02
Eliminazione E2
Eliminazione E2: la rottura del legame C-X avviene contemporaneamente alla perdita dell'idrogeno. La velocità dipende dall'alogenoalcano e dalla base. Più forte è la base, più veloce sarà il meccanismo E2. v = k[alogenoalcano][base]
stato di transizione 8OH --- H CH3-CH2-CH2-Br + "OH = CH3 -CH === CH2 ------ Br CH3-CH=CH2 + HOH + Br
Alcoli e Fenoli
Classificazione degli Alcoli
OH R-OH H R エ ー R-C-OH R-C-OH R-C-OH A seconda di quante catene carRONiose H R Ř Alcol primario Alcol secondario Alcol terziario
Nomenclatura e Proprietà degli Alcoli
- SUFF. "-OLO"
- Si METTE AL N° + Basso Possibile
- OH ha Priorità su G. ALchiLici [MeziLe, PropiLE ecc.]
- SE Ci SONO + G. OH, si MeTTE "di-/Tri- ecc." Prima di "OLO"
- IL Leg. C-O & O-H SONO POLari, Perciò FANNO Leg. Ad H
- i Leg. Ad H DONNO ALTi P. FUSIONE ed EBOLLIZIONE
- SONO SOLUBILI IN H2O
- + carbonio Nella catena MiNOMe SOLUBILITÀ + di 5 c SONO INSOLUBILi
Enoli
ENOLI : R1 OH C = C -OH Doppio Leg. & OH HANNO proprietà Diverse degli ALCOLi R2 R3
Fenoli
Fenoli OH
- OH Si METTE IN POS. 1
- SONO + Acidi degli ALCOLI
- Se Ci SONO Altri gruppi che Mettono SUFFISSO IL FENOLO x indicare Si usa iL PreFisso "IDrossi-"
1CH2 OH 2CH-OH 3CH2-OH 1,2,3-propantriolo (glicerolo) L (sia tra Loro Che CON H2O)2"02
Reazioni degli Alcoli e Fenoli
Reazioni Coinvolgenti i Legami C-O e O-H
RealZIONi: che COINVOLGONO IL Leg. C-O e O-H
- Reazione acido-base
- Reazioni di sostituzione nucleofila Le stesse degli alogenuri alchilici
- Reazioni di eliminazione
- Ossidazione Disidratazione (rimozione di H2O) in ambiente acido, con formazione di un alchene
Reazione Acido-Base degli Alcoli
Reazione Acido-Base: - gli ALCOLI SONO AMFOTERI -Si comportano da Basi IN Presenza di Acioli Si comportano da Acioli in Presenza di Basi - Quindi Reagendo CON Acidi O Basi FormaNo gli Alcossidi - La Reaz. l' spostata a Sx -gli ALCOL primari SONO Acidi + Forti perché NONNO MENO C
Reazione di Ossidazione degli Alcoli
Reazione di ossidazione: -GLI ALCOLI primari si ossidaNo ad Aldeidi Che si può' Ossida Di NUOVO Ad A. CarbossiLici -Gli ALCOLI Secondari Si OssidoNO A CheTONi
O O RCH2OH R-C R-C H OH Aldeide Acido carbossilico
Etilometro e Ossidazione dell'Etanolo
ETILOMetro, ReaZ. Tra ETANOLO E CONe Bicromato: ETANOLO si ossida, Riducendo coNe Arancione/ Rossastro A loNe CrOMO Bicromato la persona soffia attraverso il boccaglio nel tubo il tubo di vetro contiene come reagente bicromato di potassio con acido solforico impregnato su gel di silice quando la persona soffia nel tubo, il palloncino si gonfia
Sostituzione Nucleofila degli Alcoli
+ SOSTITUZIONE NUCLEOFiLa: - GLI ALCOLI DANNO Sia SNA Che SN2 - Sostituisci LOH CON UN NUCLEOFiLD SE Attacco: - RO" = Eter - NH2 = AHMiNe
Reazioni dei Fenoli
FENOLI: - L'UNICO REDUZ. Che POSSONO È: SOSTITUZIONE ELETTroFiLa Grazie Agli è" Della Delocalizzazione Dell'ANELLO BENZENico
Tioli
Caratteristiche dei Tioli
TioLi H H-C-S-H MITONTiOLO - R-S-H - ALCOLI CON S AL posto di O SH NON OH H - SUFF. "-TiOLi" HS -se ci SONO sia OH Che SH PREF: " Mercapto-" OH -odore sgradevole SUFF. : "-OLD" 2-mercaptoetanolo - SONO MENO POLari- Leg. Ad H + deBoli P. EBOLLIZIONE + BASSO - Acidi + Forti
Reazioni dei Tioli
- stesse Reaz degli ALCOLI : - Acido-Base -Sostituzione -EUNANAZIONE -Ossidazione Si OssidaNO A DiSOLFuri CON Ossidanti DeBOLI Si OssidaNO Ad Acido SOLFORICO CON OssidaNti Forti
Alcol2"02
Eteri e Tioeteri
Proprietà e Nomenclatura
Eteri e Tioeteri R-O-R R-S-R
- SONO COMPOSTI Basici -Zio SONO BASI + Forti
- se gli R SONO uguali Etere Simmetrico, SENNÒ ASIMMetrico
CH3 - SUFF. "_Etere" OPPURE SUFF. "-OSSi 1 CH3CH2-0-CH-CH3 2-Etossipropano (etil isopropil etere)
Ammine
Classificazione delle Ammine
AMMiNe H H R" R-N R-N R-N H R' R Ammina Terziaria Ammina Primaria Ammina Secondaria
Nomenclatura delle Ammine
SUFF. - AMMING "N-SOST- AMMING" "N,N- SOST - AMMING" :NH2 CH2 CH2 CH3 1 ProPANAMMING CH, NH CH, CH. N-Metil ETaNAMMiNA CH3 CH2-N-CH3 N,N-dimetil ETON AMMING - se ci SONO Altri G. CON Priorità' (Tipo OH). PreFISSO "AMMINO-"
Proprietà delle Ammine
- SONO Molecole POLari
- Le Primarie e seconarie POSSONO FAM Leg. H
- HOWNO P. EBOLLIZIONE + BASSO degli ALCOLi L'azoto ha un doppietto elettronico non legato, si comporta come una base migliore dei composti contenenti ossigeno. La presenza di un sostituente arilico diminuisce la basicità Kb = 6 . 10-4 Kb = 5 . 10-4 Kb = 6.6 . 10-5 .. :Z H H CH3 H3C NACH3 CH3 H H+ H H H H Z H H H3C NOCH3 CH3 CH3 CH3 Ammina Secondaria > Ammina Primaria Basicità > Ammina Terziaria .. NACH3 CH3 + H CH2 Dipende dalla Quantità di R che sostituiscono gli H2"02
Sostituzione Nucleofila delle Ammine
SOSTITUZIONE NUCLEOFiLa SONO NUcleoFile Perché SONO Ricche di è Quindi FANNO SN CON ALOgeNuri Alchilici L'ALogeNuro Alchilico Si Attacca All' AMMING Primaria generando Una secondaria H H H CH3 I- + HI + WY H H CH3 CH3
Aldeidi e Chetoni
Gruppo Carbonilico
ALdeidi e CHECONi - g. carBonifico C=0
O C C R H R R' Aldeide Chetone
Nomenclatura e Proprietà
1 SUFF "-ALE" SUFF. "- ONE" (+ NOME) PreF. Numero di posizione dei vari sostituENTi - COMPOSTi POLari - HOWNO P. EBOLLIZIONE + ALTO degli eteri e ALcaNi 2 Perché NON FANNO Leg H INTerMolecolari
Reazioni Coinvolgenti il Legame C=O
Reazioni: che COINVOLGONO iL Leg. C=O
- Reazione acido-base
- Reazioni di addizione nucleofila IN AMBIENTE Acido perché L'Acido ProtoNa, carica positivamente La Molecola
- Reazioni di ossidazione
- Reazione di riduzione
Addizione Nucleofila
Se Add. : ALCOL/Aldeide/ ChecoNe Si Forma UN EmiacezaLe se Add. ChecoNe EMiChetate gli EMinCezaLe SONO Zuccheri, Che daNNO IsoMeria di Tipo H H :Q-R R-C. R- R + O-R > R C-ÖR O: + GOH :OH :OH
Tautomeria Cheto-Enolica
TautoMeria cheto-ENOLica H II .C. C H3C CH3 H.C C L'ENOLO è MeNO staBile del chezone H 99.999 999 9% 0.000 000 1% Acetone Ħ H H H H H + così UNA secondaria si Attacca generando Una Terziaria All' AlogeNuro Alchilico CH3 H O + BASSO degli ALCOLi e A. carBossiLici emiacetale