Chimica generale: atomo, legami chimici e reazioni
Slide sulla chimica generale che introduce i concetti base della chimica, partendo dalla struttura dell'atomo e dei suoi componenti. Il Pdf, utile per la scuola superiore, tratta i legami covalenti e metallici, le reazioni chimiche e le equazioni bilanciate, con un focus sugli argomenti principali.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
L'atomo e la sua struttura
Le sostanze sono formate da particelle molto piccole: gli atomi. Se sono formate da atomi uguali si chiamano sostanze semplici o elementi chimici; se sono formate da atomi diversi si chiamano sostanze composte o composti.
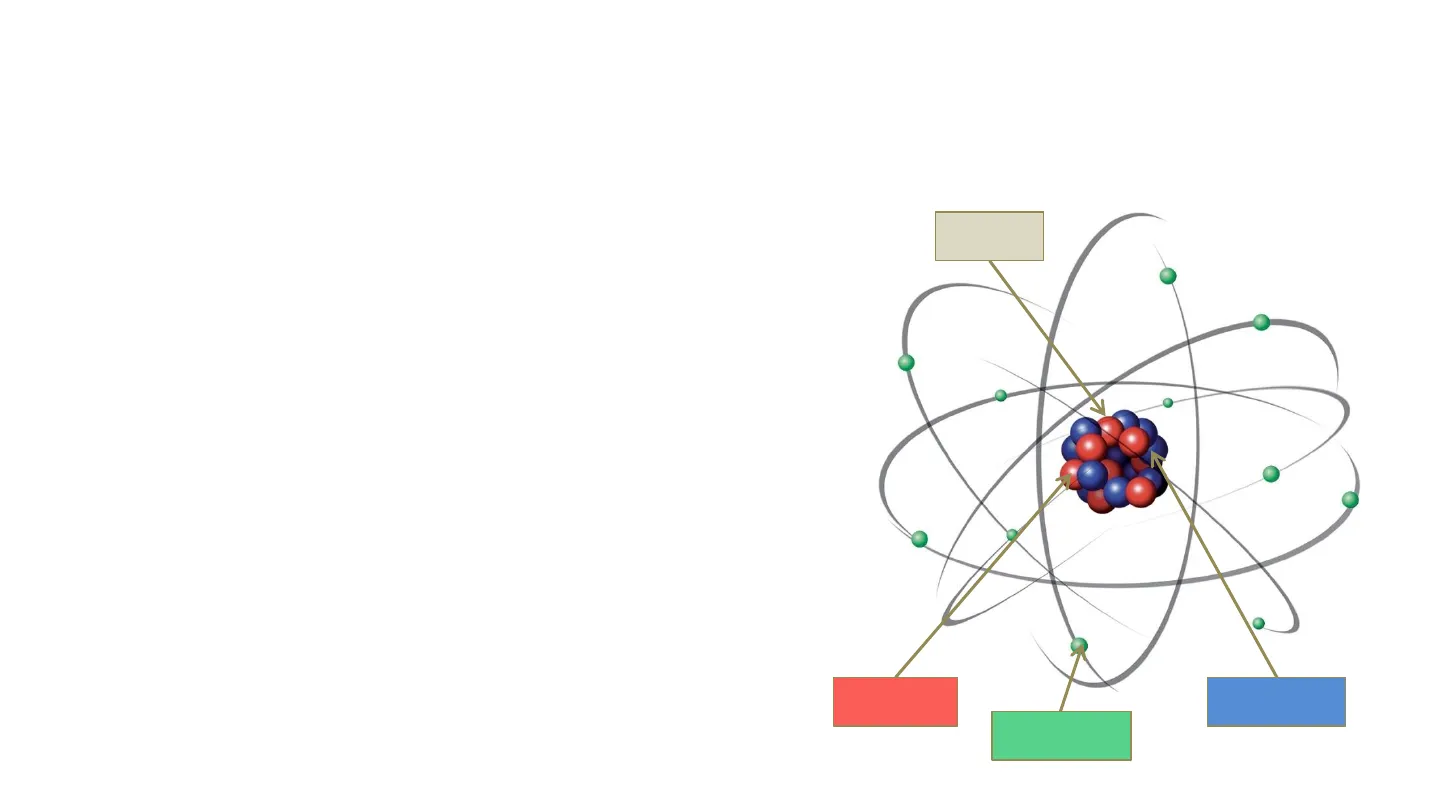
Ogni atomo è formato da una parte centrale, il nucleo, in cui è concentrata la quasi totalità della sua massa. Il nucleo è formato da protoni, particelle con carica elettrica positiva e da neutroni, particelle che non hanno carica elettrica.
Intorno al nucleo ruotano gli elettroni, particelle che hanno carica elettrica negativa.
nucleo protone neutrone elettroneL'atomo e la sua struttura
Gli elettroni non si trovano tutti alla stessa distanza dal nucleo ma si muovono all'interno di orbite concentriche poste a distanze crescenti dal nucleo. Particolari insiemi di orbite formano i gusci elettronici. Nei diversi atomi gli elettroni occupano i gusci a partire da quello più interno, più vicino al nucleo, e solo quando un guscio è completo incominciano a occupare il guscio successivo. Ogni guscio ospita un numero fisso di elettroni che varia da guscio a guscio.
È importante ricordare che in ogni atomo il guscio più esterno può contenere al massimo otto elettroni.
Numero atomico e numero di massa
Ciò che rende differenti gli elementi chimici è il diverso numero di protoni presente nel nucleo dell'atomo.
Il numero atomico è il numero di protoni presenti nel nucleo e viene indicato in basso a sinistra (Z).
Un atomo, per quanto molto piccolo, ha una sua massa. Il numero di massa è il numero dei protoni e dei neutroni presenti nel nucleo e viene indicato in alto a sinistra (A).
Gli atomi sono troppo piccoli per essere misurati in kilogrammi. Si è deciso di usare un'unità di misura convenzionale chiamata Unità di massa atomica.
La massa atomica è la somma della massa di protoni, neutroni ed elettroni.
numero di massa simbolo chimico generico A Z X numero atomico
Gli isotopi
Un elemento chimico ha sempre lo stesso numero di protoni. Però il numero dei neutroni può variare.
Gli isotopi sono gli atomi di un elemento che hanno lo stesso numero di protoni ma diverso numero di neutroni.
L'idrogeno, ad esempio, è una miscela di tre isotopi, ciascuno dei quali possiede un solo protone:
- l'idrogeno comune o pròzio, che non ha neutroni;
- il deuterio che ha un neutrone;
- il trizio che ha due neutroni.
1 H 1 protone 1 elettrone pròzio 1 2 2 H 1 1 protone deuterio 1 elettrone 1 neutrone 3 H 1 1 protone 1 elettrone 2 neutroni trizio
La tavola periodica
Dopo il 1700 gli scienziati hanno scoperto diversi elementi chimici prima sconosciuti e hanno tentato di raggrupparli in base alle loro caratteristiche.
A metà dell'Ottocento il chimico russo Dimitrij Mendeleev li classificò in una tabella, chiamata tavola periodica degli elementi.
Oggi si usa una versione più moderna della tavola di Mendeleev, in cui gli elementi sono disposti in ordine crescente secondo il numero atomico.
Nella tavola periodica ogni elemento è inserito in una casella che riporta il nome, il simbolo chimico, il numero atomico e la massa atomica.
Il simbolo chimico deriva generalmente dal nome latino dell'elemento ed è formato da una lettera maiuscola oppure da una lettera maiuscola e una minuscola. Per esempio l'ossigeno è O, il calcio Ca.
Dimitrij MendeleevLa tavola periodica
Gli elementi chimici sono ordinati in righe orizzontali, chiamate periodi, e in colonne verticali, chiamate gruppi.
Gli elementi appartenenti allo stesso gruppo hanno proprietà molto simili.
Questo comportamento è legato al fatto di avere tutti lo stesso numero di elettroni nel guscio esterno.
Le proprietà chimiche di un elemento sono determinate dal numero di elettroni presenti nel guscio più esterno.
Gli elementi sono inoltre suddivisi in metalli, non metalli, semimetalli e gas nobili.
Gli elementi della tavola periodica
Metalli alcalini Metalli Metalli alcalino terrosi Non metalli Alogeni (non metalli) Semi metalli Gas nobili Lantanidi Attinidi
Tavola periodica degli elementi
Gruppo > I Periodo = III IV V VI VII VIII 1 2 H He Idrogeno 5 6 7 8 9 10 Metalli alcalini B C N O F Ne Boro Carbonio Azoto Ossigeno Fluoro Neon 11 12 13 14 15 16 17 18 AI Si P S CI Ar Metalli alcalino terrosi Sodio Magnesio Alluminio Silicio Fosforo Zolfo Cloro Argo 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 Non metalli K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Potassio Calcio Scandio Titanio Vanadio Cromo Manganese Ferro Cobalto Nichel Rame Zinco Gallio Germanio Arsenico Selenio Bromo Cripto Alogeni (non metalli) Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Cd In Sn Sb Te I Xe Rubidio Stronzio Ittrio Zirconio Niobio Molibdeno Tecnezio Rutenio Rodio Palladio Cadmio Indio Stagno Antimonio Tellurio Iodio Xeno Semi metalli 55 56 57-71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 Gas nobili Cesio Bario Lantanio Afnio Tantalio Wolframio Renio Osmio Iridio Platino Oro Mercurio Tallio Piombo Bismuto Polonio Astato Rado 87 88 89-103 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 Lantanidi Fr Ra Ac Rf Db Sg Bh Hs Mt Ds Rg Cn Uut FI Uup Lv Uus Uuo Francio Radio Attinio Rutherfordio Dubnio Seaborgio Bohrio Hassio Meitnerio Darmstadtio Roentgenio Copernicio Ununtrio Flerovio Ununpentio Livermorio Ununseptio Ununoctio Attinidi 57 58. 59 60 61 62 63 64 65 66 67 68 - 69 70 71 La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Lantanio Cerio Praseodimio Neodimio Promezio Samario Europio Gadolinio Terbio Disprosio Olmio Erbio Tulio Itterbio Lutezio 89 90 91 92 93 - 94 95 - 96 - 97. 98 99 100 101 102 103 Ac Th Pa U Np Pu Cm Bk Cf Es Fm Md No Lr Attinio Torio Protoattinio Uranio Nettunio Plutonio Curio Berkelio Californio Einstenio Fermio Mendelevio Nobelio Laurenzio 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54. 5 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg TI Pb Bi Po At Rn 6 Na Mg 3 Li Be 2 Litio Berillio Metalli 1 Elio 3 4 4 7 Am Americio Ag Argento
Metalli, non metalli e semimetalli
Metalli: sono solidi a temperatura ambiente (tranne il mercurio che è liquido); sono lucenti; sono buoni conduttori di calore ed elettricità; possono essere lavorati con facilità per ottenere lamine e fili. Tra i metalli più conosciuti ci sono il ferro (Fe), l'oro (Au), il rame (Cu), il sodio (Na) e il calcio (Ca).
Non metalli: a temperatura ambiente possono essere solidi, liquidi o gassosi; sono opachi; sono fragili; sono cattivi conduttori di calore ed elettricità. Tra i non metalli ci sono l'ossigeno (O), l'azoto (N), il carbonio (C) e il cloro (Cl).
Semimetalli: sono elementi che presentano caratteristiche intermedie tra metalli e non metalli. In particolari condizioni alcuni di essi possono essere usati come semiconduttori. Un esempio è il silicio (Si).
Lattine in alluminio. Transistor usati per i dispositivi elettronici.
Le formule chimiche
Le molecole, cioè gli aggregati di atomi, sono rappresentate da formule chimiche che indicano quali e quanti atomi sono presenti.
La formula di una sostanza semplice si scrive indicando il simbolo corredato da un indice (un numerino posto in basso a destra) che indica quanti atomi costituiscono la molecola: per esempio Cl2 indica che la molecola del cloro è formata da 2 atomi. Se l'indice è 1 viene omesso.
La formula di una sostanza composta si scrive indicando i simboli degli elementi presenti nella molecola, ciascuno corredato dal proprio indice che ne rappresenta il numero di atomi.
Il numero di molecole, invece, si indica prima della formula del composto; se c'è una sola molecola, il numero 1 viene omesso.
2CaCO3 sono 2 molecole di carbonato di calcio, ognuna delle quali è formata da 1 atomo di calcio, 1 di carbonio e 3 di ossigeno.
C = atomo di carbonio Ca = atomo di calcio Ca C O = atomo di ossigeno CaCO3
I legami chimici
La regola dell'ottetto
Gli atomi che hanno 8 elettroni presenti nel guscio più esterno sono estremamente stabili e hanno quindi una scarsa tendenza a partecipare a reazioni chimiche, come accade nei gas nobili. Gli atomi che non hanno questa configurazione stabile tendono a raggiungerla.
- Gli elementi che hanno più di 4 elettroni nel guscio esterno tendono a combinarsi con altri elementi acquistando un numero di elettroni che consente loro di arrivare a 8 per completare l'ottetto. Il fluoro, ad esempio, ha 7 elettroni nel guscio esterno e, nel combinarsi con atomi di altri elementi per formare dei composti, tende ad acquistarne 1; l'ossigeno, che ha 6 elettroni nel guscio esterno, tende ad acquistarne 2.
- Gli elementi che hanno meno di 4 elettroni tendono invece a cederli. Così il litio, che cede 1 elettrone, o il berillio, che ne cede 2.
atomo isolato di neon (Ne) atomo isolato di fluoro (F) atomo isolato di ossigeno (O) atomo isolato di litio (Li) atomo isolato di berillio (Be)
Il legame ionico
In condizioni normali, l'atomo è elettricamente neutro perché ha tanti protoni quanti elettroni.
Se un atomo cede elettroni a un altro atomo e rimane con più protoni, ha una carica positiva.
Se acquista elettroni da un altro atomo e rimane con meno protoni rispetto agli elettroni, ha una carica negativa.
Questi atomi carichi elettricamente si chiamano ioni. Poiché le cariche elettriche di segno opposto si attraggono, gli ioni positivi e quelli negativi restano uniti tramite un'attrazione elettrostatica che si chiama legame ionico.
Per esempio, il sodio (Na) ha 1 solo elettrone nel guscio esterno che perde facilmente per la regola dell'ottetto. Il cloro (Cl) ha 7 elettroni nel guscio esterno e ne acquista 1 facilmente. I due ioni Na+ e CI si uniscono e formano il cloruro di sodio (NaCl), il sale da cucina.
Il legame covalente
Il legame covalente si forma tra atomi di uno stesso elemento o di elementi differenti che mettono in comune una o più coppie di elettroni.
L'idrogeno ha 1 solo elettrone e per diventare stabile ha bisogno di 2 elettroni. Allora 2 atomi di idrogeno si uniscono e mettono in comune il proprio elettrone. La molecola H2 che si è formata è stabile.
Nella molecola del metano (CH4) il carbonio (C), che ha 4 elettroni nel guscio esterno, si lega con 4 atomi di idrogeno (H) e completa l'ottetto.
Nella molecola dell'acqua (H2O) i 6 elettroni dell'atomo di ossigeno si legano con i 2 dell'idrogeno per completare l'ottetto e diventare stabili.
H H idrogeno molecola di idrogeno H H molecola del metano H H H H metano C C H H H H H H O molecola dell'acqua H acqua H