Rehearsal 6: i composti organici in chimica
Documento di Università sui composti organici. Il Pdf esplora i fondamenti della chimica organica, concentrandosi su idrocarburi alifatici e aromatici, e derivati come gli alcoli, utile per lo studio della Chimica a livello universitario.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
I composti organici
Che cos'è la chimica organica? È quella parte della chimica che studia la chimica dei viventi. Studia in particolare, il Carbonio, pochi altri elementi quali Idrogeno, Ossigeno, Azoto, Zolfo e Fosforo e i loro comportamenti.
Il Carbonio è l'elemento cardine della chimica organica grazie a delle caratteristiche che lo rendono molto versatile:
- Ha 4 elettroni nel suo guscio di valenza. Ciò significa che non ha tendenza né a cedere né a guadagnare elettroni, ma è propenso a condividerli.
- Può esistere in diverse ibridazioni (sp, sp2, sp3). In base a quali assume modifica la sua forma e la tipologia di legame tra gli atomi (legami singoli, doppi o tripli). Presente in alcan alcheni alchini Legame C-C 10 10+1T 10 +2 Geometria tetraedrica trigonale lineare
- Ha un'alta tendenza a formare delle catene, ha una forte capacità di concatenazione. Si combina con altri atomi di carbonio per formare dei composti che possono essere estremamente lunghi. Queste catene di atomi di carbonio rappresentano lo scheletro carbonioso delle molecole organiche, questo può avere diverse conformazioni (aperte, chiuse, ramificate, cicliche, ... ).
Idrocarburi alifatici
Sono i composti più semplici della chimica organica. Sono composti binari, composti solo da Carbonio e Idrogeno. Sono gli unici che non presentano un vero e proprio gruppo funzionale.
Possono essere:
- Idrocarburi alifatici: catene lineari aperte o chiuse o ramificate idrocarburi aromatici: hanno a almeno un anello aromatico
- Saturi: contengono solo legami semplici
- Insaturi: molecole con almeno un doppio o un triplo legame
Idrocarburi Alifatici Aromatici (sp2) Alcani (sp3) Alcheni (sp2) Alchini (sp)
Alcani - CnH(2n+2)
Sono idrocarburi alifatici saturi, presentano quindi solo legami singoli.
- Sono tutti ibridati sp3
- Formano 4 legami. Solo legami covalenti puri
- Hanno un angolo di legame di 109,5° e formano un tetraedro
- Il più semplice è il metano, CH4 I composti successivi al metano vengono generati con l'aggiunta di un gruppo CH2 (un'unità metilica); quando si costruisce un gruppo di molecole aggiungendo a ripetizione lo stesso elemento si parlerà di serie omologa.
エ ー H-C-H H metano H C H H 109,5° H sp sp- sp ... 109,5 109,5° sp Px 109,5 Ibridazioni del carbonio Sp SD2 DX py px 109,5 109,5° 120° 180 DX sp Sp -Chimica #38V - Piccoli - Rehearsal 6 Pag. 2 a 18 Grazie alla versatilità dei legami del carbonio possiamo avere delle catene ramificate e non solo lineari.
Cicloalcani - CnH2n
Sono alcani con una struttura chiusa ad anello. Il più semplice è il ciclopropano. Li rappresentiamo con dei poligoni regolari.
Il cicloesano è la struttura più stabile tra le strutture cicliche, poiché, nonostante abbia un angolo di legame di 120° nella forma planare, assume delle conformazioni particolari per una questione di stabilità.
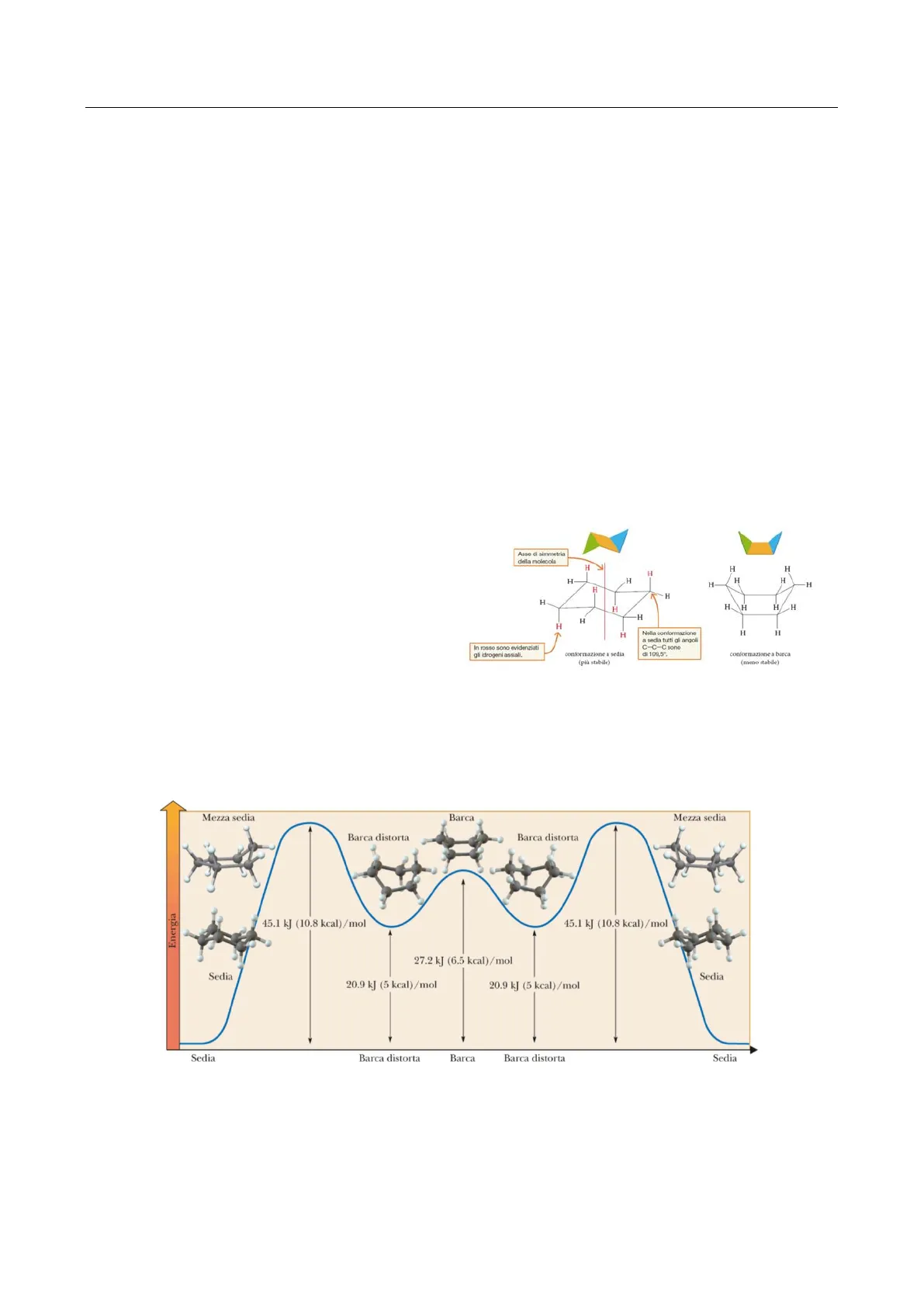
- Conformazioni a sedia: sono 2 e sono le conformazioni più st abili. Permettono di ridurre al minimo le tensioni angolari, portando l'angolo a 109,5°. Con queste conformazioni si sfalsano completamente tutti i legami CH presenti andando così a ridurre al minimo le repulsioni di legame tra C e H. L'inversione d'anello nel cicloesano a sedia interconverte le posizioni assiali ed equatoriali in un processo in due stadi. Le conformazioni del cicloesano a sedia si interconvertono passando da conformazioni ad energia più alta, come quella a barca, quella a barca intrecciata (twist) e quella a semisedia. Le due conformazioni a sedia sono energeticamente equivalenti, ma cambiano nell'orientamento: o Assiali: legami C-H puntano 3 sopra e 3 sotto il piano o Equatoriali: giacciono sul piano della molecola (6 atomi di H nella posizione equatoriale)
- Conformazione a barca: è meno stabile perché presenta ingombro sterico e alcuni legami a idrogeno vengono eclissati aumentando le forze di repulsione
- La più instabile in assoluto è quella a semisedia.
Si può passare da una conformazione all'altra, ma con dispendio energetico.
Mezza sedia Barca Mezza sedia Barca distorta Barca distorta Energia 45.1 kJ (10.8 kcal)/mol 45.1 kJ (10.8 kcal)/mol 27.2 kJ (6.5 kcal)/mol Sedia Sedia 20.9 kJ (5 kcal)/mol 20.9 kJ (5 kcal)/mol Sedia Barca distorta Barca Barca distorta Sedia H H -H H H H H H/H H H H H H H In rosso sono evidenziati gli idrogeni assiali. conformazione a sedia (più stabile) conformazione a barca (meno stabile) Asse di simmetria della molecola H H H H H H H H H Nella conformazione a sedia tutti gli arigoli C-C-C sono di 109,5°%Pag. 3 a 18 Chimica #38V - Piccoli - Rehearsal 6
Proprietà e caratteristiche degli alcani
Isomeria degli alcani
Isomeria > Negli alcani troviamo solo un'isomeria di catena. Si possono generare concatenazioni diverse, solo a partire dal Butano che presenta 4 atomi di C. Esempio: se sposto un gruppo metile nel butano posso ottenere un 2- metilpropano
catena lineare catena ramificata CH CH3-CH2-CH2-CH3 n-butano C4H10 CH3-CH-CH3 2-metilpropano C4H10
Proprietà fisiche degli alcani
Proprietà fisiche > gli alcani sono apolari, hanno quindi un punto di ebollizione molto basso perché tra loro avranno solo forze di dispersione di London. La forma e lunghezza delle catene carboniose degli alcani può influenzare il punto di ebollizione. Sono dunque anche insolubili in acqua
Proprietà chimiche degli alcani
Proprietà chimiche > hanno dei legami covalenti semplici e non polari. Sono poco reattivi, per questo vengono anche chiamati paraffine.
Reazioni degli alcani
Reazioni > gli alcani fanno solo 2 reazioni:
- Combustione: si libera calore. Gli alcani sono spesso dei combustibili che trasformiamo in anidridi (CO2 e H2O). È una reazione di ossidazione, gli elettroni di legame 2 CH4 + 3 02 -> |2 CO |+ 4 H2O + calore vengono presi tutti dall'ossigeno. Il numero di ossidazione del Carbonio aumenta = ossidazione.
- Alogenazione: sostituzione radicalica a catena. Prende il nome di alogenazione perché coinvolge degli alogeni (ione bromuro, clorurazione). Radicalica perché coinvolge dei radicali, come bromo e cloro. In una molecola biatomica di bromo o cloro non c'è differenza di elettronegatività tra i due. Questi Clorurazione: reazione di sostituzione di un atomo di idrogeno con un atomo di cloro romperanno il loro legame in modo Bromurazione: reazione di sostituzione di un atomo di idrogeno con un atomo di bromo simmetrico e genereranno 2 radicali uguali R-H + CI-CI luce o calore + R-CI + H-CI dello stesso elemento. Uno dei due radicali strappa un idrogeno dalla catena, per potersi R-H + Br-Br luce o R-Br + HBr calore attaccare al carbonio, andando così a generare un radicale alchilico che a sua volta potrà reagire generano un radicale alchilico e dall'altra parte un acido. Per terminare la catena si devono mettere insieme due specie radicaliche (questo non sempre genera dei prodotti desiderati).
Idrocarburi alifatici insaturi
Alcheni CnH2n
Sono idrocarburi alifatici insaturi, presentano almeno un doppio legame.
- Sono tutti ibridati sp2
- Hanno un angolo di legame di 120° con forma planare
- Doppio legame formato da: o Un legame sigma: ottenuto per sovrapposizione dei due orbitali sp2 dei due carboni adiacenti o Un legame pigreco: ottenuto per sovrapposizione laterale (perpendicolarmente) di due orbitali pz dei due carboni adiacenti
Dieni: molecole alifatiche insature con 2 doppi legami. Il più semplice tra i dieni è 1,3-butadiene con formula molecolare C4H6, importante per la sintesi di materiali plastici come gli pneumatici.
Polieni coniugati: molecole che presentano un'alternanza di doppi legami con legami semplici, importante perché ogni atomo di C presenta un orbitale pz perpendicolari agli orbitali sp2 che permette di delocalizzare il C generando una sorta di unico legame Pigreco lungo tutta la molecola. Esempio, il betacarotene che partecipa alla sintesi della vitamina AChimica #38V - Piccoli - Rehearsal 6 Pag. 4 a 18
Proprietà e caratteristiche degli alcheni
Isomeria degli alcheni
Ci sono vari tipi di isomeria che coinvolgono gli alcheni:
- Catena: come per gli alcani c'è una differenza unione degli atomi di carbonio lungo la catena alifatica
- Posizione: il doppio legame potrebbe essere posizionato in varie zone della catena alifatica, quasi come se fosse un gruppo funzionale
- Geometrica: se i due sostituenti sono uguali in base a come questi saranno disposti avremo gli isomeri cis (sostituenti dallo stesso lato) o Trans (sostituenti da parti opposte). In questo ci sarà necessario utilizzare la nomenclatura E-Z per definire la posizione dei sostituenti. H H H C C C C C CI C isomero cis isomero
Proprietà fisiche degli alcheni
Tra le proprietà fisiche possiamo riconoscere gli alcheni come composti apolari che hanno hanno quindi un punto di ebollizione basso leggermente più basso rispetto agli alcani a causa del doppio legame. Sono tendenzialmente insolubili.
Reattività degli alcheni
Gli alcheni sono molto reattivi a differenza degli alcani. La presenza del doppio legame rende quel punto della molecola molto reattivo, a causa della presenza di 4 elettroni concentrati in un piccolo spazio. Questa zona sarà attaccabile da tutte le specie cariche positivamente TYPE OF ADDITION REACTION NAME (elettrofili).
- Addizione elettrofila: L'elettrofilo attacca il doppio legame, si lega ad uno dei due atomo di C del doppio legame. Si apre il doppio legame e si genera un carbocatione che verrà annullato da un nucleofilo. Questo è il meccanismo generale, cambierà solo il tipo di elettrofilo.
- Idrogenazione catalitica del doppio legame: catalisi in fase eterogenea nella cinetica. Un catalizzatore metallico lega un alchene e un idrogeno, forma due radicali rompendo idrogeno e si aggiunge idrogeno al doppio legame. Addition of H and X fx Hydrohalogenation (X=CI, Br, or 1) Hydration Addition of H and OH H OH Hydrogenation Addition of Hand H H- H Addition of X and X x Lx Halogenation (X=Cl or Br) Addition of OH and X - x Halohydrin formation (X=Cl, Br, or I) Dihydroxylation Addition of OH and OH HO OH
- Alogenazione del doppio legame: si aggiunge due alogeni al posto di idrogeno
- Idratazione del doppio legame: a partire dall'alchene se aggiungo acqua ottengo un alcol
- Idroalogenazione del doppio legame: lo ione idrogeno si lega ad un atomo di carbonio del doppio legame e il resto dell'acido (ovvero l'alogeno) si lega all'altro atomo di carbonio (ad esempio acido alogenidrico)
Alchini CnH2n-2
Sono idrocarburi alifatici insaturi, presentano almeno un triplo legame.
- Sono tutti ibridati sp
- Hanno un angolo di legame di 180°
- Triplo legame formato da: o Un legame sigma: ottenuto per sovrapposizione dei due orbitali sp2 dei due carboni adiacenti o Due legami pigreco: ottenuto per sovrapposizione laterale (perpendicolarmente) di due orbitali pz e py dei due carboni adiacenti H