Benzene e composti aromatici: stabilità e criteri di Hückel
Slide dall'Università San Raffaele Roma su benzene e composti aromatici. Il Pdf esplora la stabilità energetica e gli orbitali molecolari, introducendo i criteri di Hückel per l'aromaticità in Chimica a livello universitario.
Mostra di più22 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Università San Raffaele
Roma
Professore Gilda Aiello Argomento Benzene e composti aromaticiT Università San Raffaele Roma Gilda Aiello
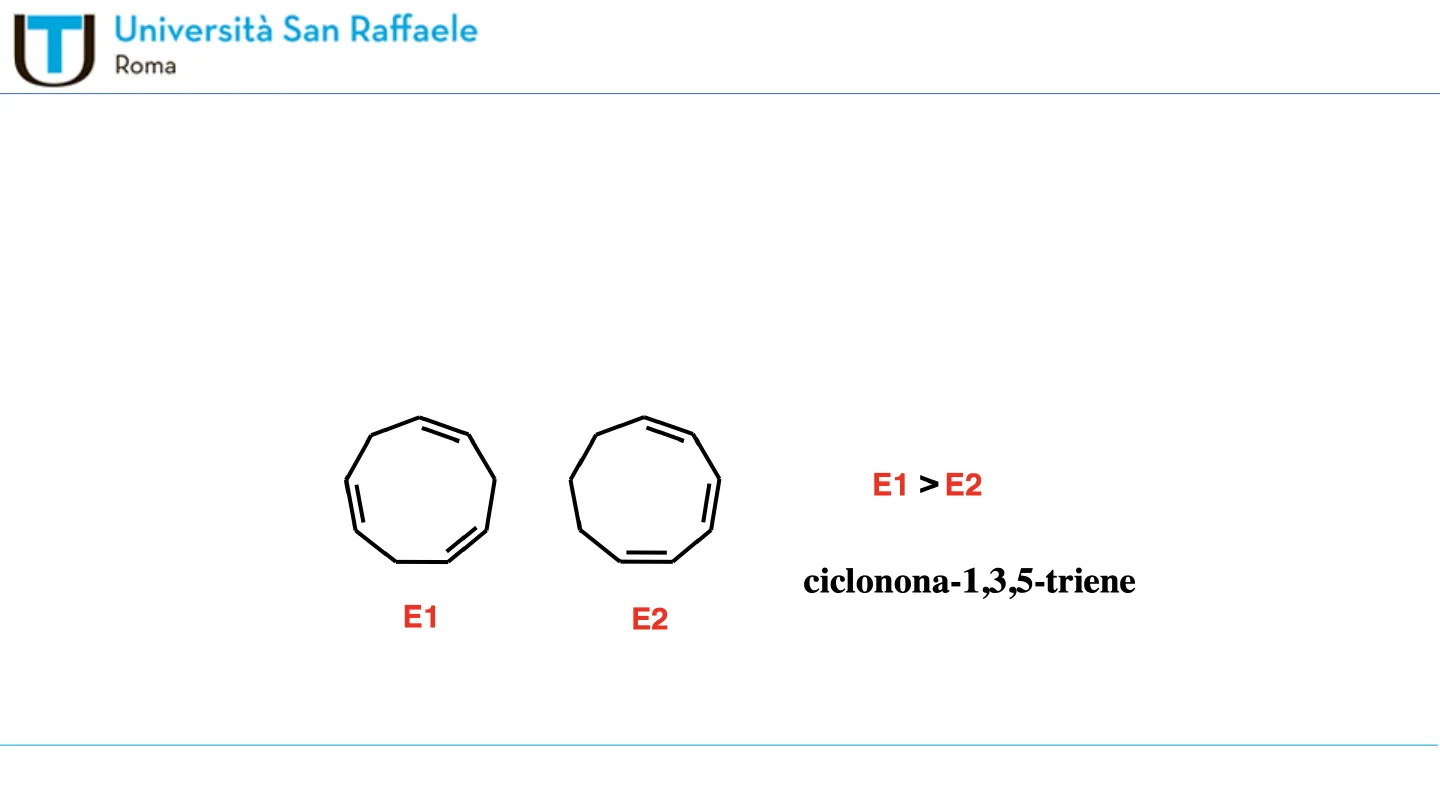
Nelle molecole poli-insature a doppi legami coniugati la possibilità degli elettroni TT di delocalizzarsi su un più ampio numero di atomi determina una rilevante riduzione dell'energia del sistema (energia di risonanza) E1 > E2 E1 E2 ciclonona-1,3,5-triene
Benzene e composti aromatici
Stabilizzazione per risonanza
Un caso di stabilizzazione per risonanza di particolare rilievo è osservato nel caso di alcune molecole cicliche insature nelle quali tutti i doppi legami sono in disposizione coniugata Il più importante tra questi esempi è rappresentato dalla molecola di benzene 1 1 2 2 forme limite (strutture di Kekulè) 1.54 Å 1.33 Å C = 1.39 Å Ibrido di risonanza
Benzene e composti aromatici
Struttura del benzene
Come è fatto il benzene? Questa particolare struttura permette il fenomeno della delocalizzazione degli elettroni, così che la molecola può essere rappresentata con una nuvola elettronica estesa sopra e sotto al piano individuato dagli atomi di carbonio. H H H -H H/ H H H H -- H H H La delocalizzazione degli elettroni può essere evidenziata rappresentando la struttura del benzene con un cerchio all'interno della molecola.
Benzene e composti aromatici
Ibridazione e delocalizzazione
a. b. C. d. Tutti gli atomi di carbonio sono ibridati sp2 ·Il legame tra gli atomi di carbonio è formato per sovrapposizione frontale di orbitali sp2; ·Ogni orbitale p non ibridato contiene 1 elettrone spaiato; in seguito alla sovrapposizione laterale dei 6 orbitali p ciascuno di questi elettroni è condiviso anche dagli altri atomi di carbonio del ciclo. In altre parole gli elettroni TT sono delocalizzati sopra e sotto l'anello molecolare
Benzene e composti aromatici
Aromaticità e stabilità termodinamica
Aromaticità · Il Benzene possiede una stabilità termodinamica maggiore rispetto agli alcheni · Il surplus di stabilità rispetto ai doppi legami coniugati viene definite energia di risonanza ed è caratteristica delle molecole aromatiche hypothetical cyclohexatriene 85.8 1,3-cyclohexadiene benzene Energy cyclohexene 55.4 49.8 28.6 * Il calore di idrogenazione del benzene è di circa 49.8 Kcal per mole. Il benzene quindi è di ben 36 kcal/mole più stabile di quanto ci potessimo aspettare. Questo incremento di stabilità è una caratteristica dei composti aromatici. Questa differenza di energia è detta energia di risonanza ed è dovuta al fatto che in realtà nel benzene non ci sono tre doppi legami, ma "qualcosa" di diverso. cyclohexane
Benzene e composti aromatici
Anuleni e aromaticità
Anuleni . Non tutti I composti ciclici con doppi legami coniugati sono aromatici. · Il ciclobutadine è estremamente reattivo. . Il ciclottatetraene subisce addizione di Br2 facilmente. · L'aromaticità si spiega ricorrendo agli orbitali molecolari. ciclobutadiene Non seguono la regola di Huckel cicloottatetraene
Benzene e composti aromatici
Orbitali Molecolari del Benzene
Orbitali Molecolari del Benzene La grande stabilità energetica del benzene nello stato fondamentale è giustificata dalla completa occupazione di tutti gli orbitali leganti da parte dei 6 elettroni TT · Tre saranno di legame, tre di antilegame. · Gli OM a minore energia avranno tutte interazioni di legame, nessun nodo. · All'aumentare dell'energia degli OM aumenta il numero dei nodi. - 46 44 45 Energy antibonding $2 bonding
Benzene e composti aromatici
Orbitali Molecolari del Ciclobutadiene
Orbitali Molecolari del Ciclobutadiene · Nel ciclobutadiene 4 orbitali atomici p formano 4 orbitali molecolari TT • Seguendo la regola di Hund, due elettroni occupano due orbitali degeneri separati. nonbonding line M2 · L'energia degli elettroni TT del ciclobutadiene è più alta di quella del 1, 3-butadiene ** 1 T3 1
Benzene e composti aromatici
Concetto di Aromaticità: I criteri di Hückel
Concetto di Aromaticità: I criteri di Hückel Con la risonanza riusciamo a spiegare la geometria della molecola ma non ci spieghiamo la sua elevata stabilità. La stabilità del benzene si attribuisce al fatto che il sistema coniugato ha le seguenti caratteristiche: 1. contiene 4n+2 elettroni T 2. è planare Tutti i composti ciclici planari che hanno sistemi coniugati contenenti 4n + 2 elettroni condividono questa stabilità. Sistemi di questo tipo sono definiti AROMATICI.
Benzene e composti aromatici
Regola di Hückel: elettroni e planarità
1º Regola di Hückel: 4n + 2 elettroni JT 6 (n = 1), 10 (n = 2), 14 (n = 3), 18 (n = 4), etc. 4 ntelectrons not aromatic 6 melectrons aromatic 8 mtelectrons not aromatic 6 melectrons aromatic 6 melectrons aromatic NH2 .2 N H H Adenine: 10 ftelectrons Aromatic Uracil: 6 nelectrons Aromatic 2º Regola di Hückel: planarità Cyclodecapentaene Il ciclodecapentaene, possiede 10 x -elettroni ma non è planare quindi non è aromatico!
Benzene e composti aromatici
Derivati del benzene: Nomi sistematici
Derivati del benzene Nomi sistematici CI Br C2H5 NO2 chlorobenzene bromobenzene ethylbenzene nitrobenzene Nomi da imparare a memoria .... 0 OH H „CH3 CH3 HC=CH2 toluene styrene benzoic acid benzaldehyde acetophenone C=N OH 0-CH3 NH2 SO3H benzonitrile phenol anisole aniline benzenesulfonic acid
Benzene e composti aromatici
Benzene e derivati come sostituenti: nomenclatura
. Il gruppo sostituente che si ottiene per formale sottrazione di un H dal benzene si chiama FENILE (Ph) . Il gruppo sostituente che si ottiene per formale sottrazione di un H dal gruppo metilico del toluene si chiama BENZILE · Il gruppo aromatico in generale viene indicato come arile Ar- (qualsiasi anello aromatico). H3C, C-CH3 C H Phenyl Group -CH2www -CH2-Br Benzyl Group benzyl bromide diphenyl ether - CH2 -CI CI 2-benzyl-1,1-dichlorocyclobutane
Benzene e composti aromatici
Nomenclatura: 2 sostituenti
Nomenclatura 2 sostituenti 3 possibili isomeri di posizione A A 2 B 3 B 4 isomero orto isomero meta isomero para B 1,2 sostituzione orto 1,3 sostituzione meta 1,4 sostituzione para CH3 ÇH3 ÇH3 CH3 CH3 orto xilene meta xilene CH2 para xilene 1, 2-dimetilbenzene 1,3-dimetilbenzene 1, 4-dimetilbenzene
Benzene e composti aromatici
Nomenclatura: composti con nome proprio
Nome comune dei 3 possibili dimetilbenzeni 1 AT Università San Raffaele Roma Gilda Aiello Nomenclatura Quando possibile, i composti andranno nominati come derivati del benzene caratterizzati da nome proprio (fenolo, toluene, ecc.) con la numerazione che parte dal sostituente "speciale" ÇH3 F 3-fluorotoluene m-fluorotoluene NH 2 Br 4-bromoanilina p-bromoanilina O OH O2N. 2 Acido 2-nitrobenzoico Acido o-nitrobenzoico
Benzene e composti aromatici
Nomenclatura: ordine alfabetico e numerazione
Nomenclatura Negli altri casi il nome sarà ottenuto riportando prima con ordine alfabetico i due sostituenti, anticipati dal numero che identifica il punto di inserimento sul ciclo, poi il termine benzene. La numerazione parte dal carbonio su cui è inserito il sostituente di più basso ordine alfabetico CH2 CH3 .CI 1-cloro-2-etilbenzene 0-cloroetilbenzene F NO2 1-fluoro-3-nitrobenzene m-fluoronitrobenzene NO2 NO2 1,4-dinitrobenzene p-dinitrobenzene
Benzene e composti aromatici
Idrocarburi aromatici policiclici
Idrocarburi aromatici policiclici 8 1 c 8 9 1 8 9 10 7 10 3 9 4 8 7 6 5 chrysene C18H12 m.p. 253º C 10 1 9 2 8 3 7 4 6 5 pyrene C16H10 m.p. 150° C corannulene C20H10 m.p. 268º C coronene C24H12 m.p. 442º C 12 1 11 2 7 2 B 7 2 6 6 3 5 4 5 10 4 anthracene C14H10 m.p. 217º C phenanthrene 4 C14H10 m.p. 100° C 2 3 naphthalene C10H8 m.p. 81º C 3 6 1 5 hexahelicene C26H16 m.p. 230° C Naftalene, antracene, fenantrene si trovano nel catrame minerale e nei residui del petrolio altobollenti Il naftalene era utilizzato come repellente per le tarme e come insetticida per preservare la lana e le pellicce ma il suo uso è diminuito a causa dell'introduzione degli idrocarburi clorurati come il p-diclorobenzene. Il benzopirene e il coronene si possono rinvenire nei gas di scarico dei motori a benzina e nel fumo di sigaretta. Il benzopirene ha provata attività cancerogena.
Benzene e composti aromatici
Composti aromatici eterociclici
Composti aromatici eterociclici N piridina pirrolo O S furano tiofene I composti eterociclici sono composti ciclici nei quali uno o più atomi dell'anello sono di elementi diversi dal carbonio La piridina è aromatica N
Benzene e composti aromatici
Aromaticità della piridina
La piridina è aromatica Questa coppia di elettroni è su un orbitale sp2, a 90° rispetto all'orbitale p non ibridato che ospita uno dei 3 elettroni spaiati dell'atomo di azoto Nel complesso il ciclo ospita 6 elettroni TT , delocalizzati su 6 atomi, 5 di carbonio e 1 di azoto (eterociclo TT deficiente sugli atomi di carbonio)
Benzene e composti aromatici
Aromaticità di pirrolo, furano e tiofene
Anche pirrolo, furano e tiofene sono aromatici. In questo caso, però, ogni eteroatomo partecipa alla aromaticita con 2 elettroni invece che 1. In totale sei elettroni TT sono delocalizzati su 5 atomi anulari (eterocicli TT eccessivi) pirrolo H N .. 1º I 1 > 1 > :ZE +ZI +ZI +ZI +ZI Forme di risonanza € > € + + + + O O O O O Forme di risonanza
Benzene e composti aromatici
Esempi di composti eterociclici aromatici
furano : IT Università San Raffaele Roma Gilda Aiello Altri importanti esempi di composti eterociclici aromatici :N. :NH N chinolina indolo imidazzolo N :N N N H purina :N N pirimidina
Benzene e composti aromatici
Esempi di aromatici
Esempi di Aromatici .... aromatici C H O OH C Benzaldeide: Isolata dall'olio di mandorele amare Acido benzoico: Presente nella gomma benzoino, una resina balsamica CH3 CH2OH Toluene: Presente nel balsamo del tolù Alcol benzilico: Presente nella gomma benzoino, una resina balsamica