La materia e le sue caratteristiche: stati fisici e metodi di separazione
Slide di Scuola superiore sulla materia e le sue caratteristiche. Il Pdf esplora la materia e le sue proprietà, definendo il concetto di sistema e illustrando i tre stati fisici, con tabelle comparative di solidi, liquidi e aeriformi. Vengono descritti i principali metodi di separazione dei miscugli in Chimica.
Mostra di più23 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
La materia e le sue caratteristiche
Un sistema è una porzione delimitata di materia.
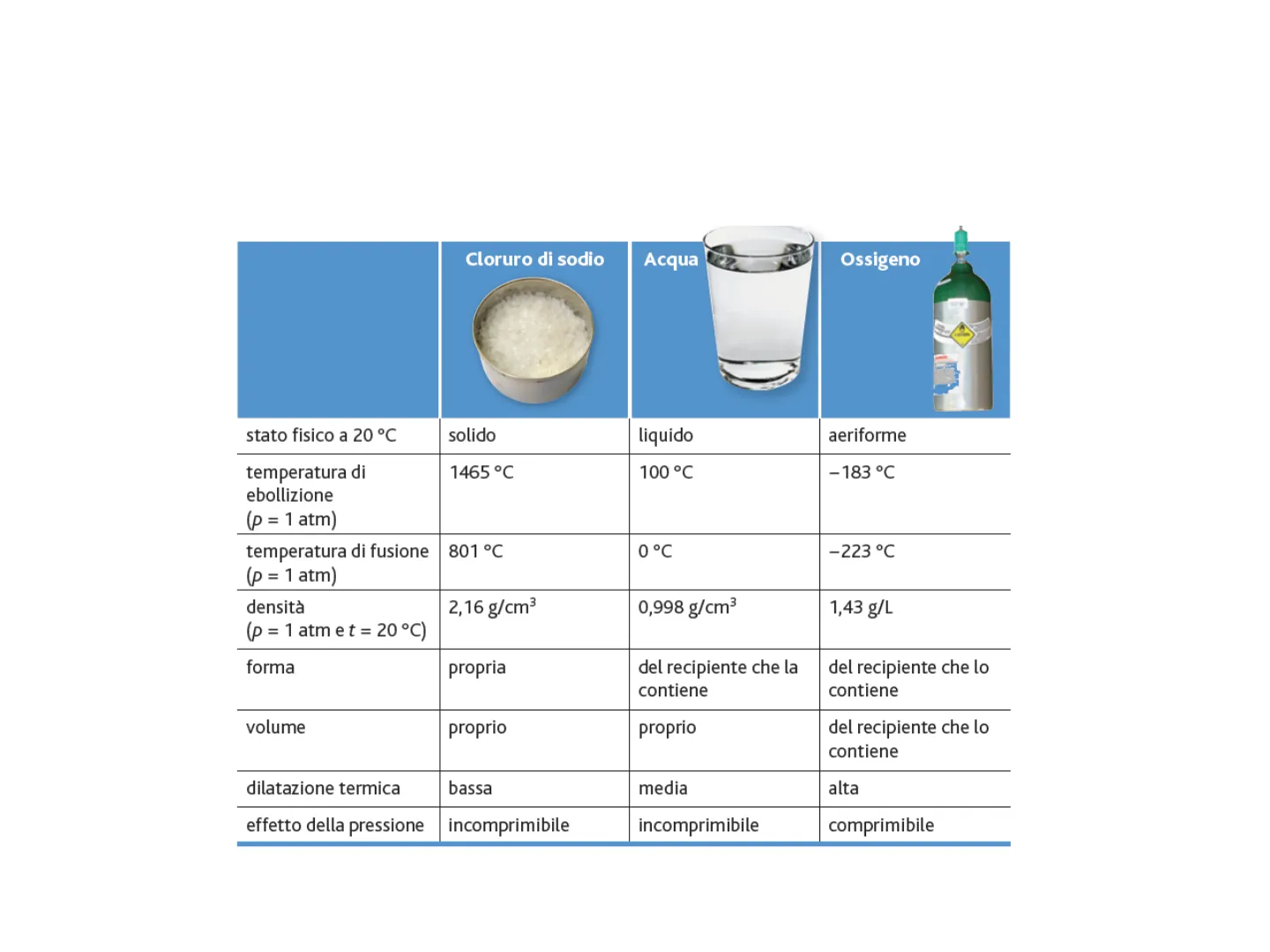
Cloruro di sodio Acqua Ossigeno stato fisico a 20 ℃ solido liquido aeriforme temperatura di ebollizione (p = 1 atm) 1465 ℃ 100 ℃ -183 ℃ temperatura di fusione (p = 1 atm) 801 °C 0 °℃ -223 ℃ densità (p = 1 atm e t = 20 ℃) 2,16 g/cm3 0,998 g/cm3 1,43 g/L forma propria del recipiente che la contiene del recipiente che lo contiene volume proprio proprio del recipiente che lo contiene dilatazione termica bassa media alta effetto della pressione incomprimibile incomprimibile comprimibile
Gli stati fisici della materia
1La materia e le sue caratteristiche (II) Gli stati fisici in cui la materia si può trovare sono:
- solido;
- liquido;
- aeriforme.
STATO LIQUIDO -200 STATO GASSOSO STATO SOLIDO
Sistemi omogenei ed eterogenei
Definizione di fase
2I sistemi omogenei e i sistemi eterogenei (I) Si definisce fase una porzione di materia fisicamente distinguibile e delimitata che ha proprietà intensive uniformi.
Sistemi omogenei ed eterogenei (II)
3I sistemi omogenei e i sistemi eterogenei (II) Quando un sistema è costituito da una sola fase si dice che è omogeneo. Quando un sistema è costituito da due o più fasi si dice che è eterogeneo.
Le sostanze pure
Sostanze pure (I)
4Le sostanze pure (I)
- Un sistema formato da una singola sostanza si dice puro.
- Le sostanze pure hanno caratteristiche e composizione costanti.
L'acqua distillata è un si- stema puro. Per identifi- carla è sufficiente la sua formula chimica: H2O. acqua distillata
Sostanze pure (II)
5Le sostanze pure (II) L'acqua potabile è una so- luzione costituita da più componenti.
- Un sistema formato da due o più sostanze pure è un miscuglio.
- I miscugli hanno composizione chimica variabile.
Miscugli omogenei ed eterogenei
Miscugli omogenei ed eterogenei (I)
6Miscugli omogenei e miscugli eterogenei (I) Una soluzione è un miscuglio di due o più sostanze fisicamente omogeneo. Il componente più abbondante della soluzione si chiama solvente, gli altri si chiamano soluti.
Miscugli omogenei ed eterogenei (II)
7Miscugli omogenei e miscugli eterogenei (II) Al microscopio si vedono le goccioline di grasso. A occhio nudo il latte appare uniforme. Un miscuglio eterogeneo è formato da componenti chimicamente definiti e da fasi fisicamente distinguibili.
Miscugli omogenei ed eterogenei (III)
8Miscugli omogenei e miscugli eterogenei (III) una sola sostanza: chimicamente omogeneo presenta una sola fase fisicamente omogeneo due o più sostanze: chimicamente eterogeneo miscuglio omogeneo o soluzione SISTEMA una sola sostanza: chimicamente omogeneo presenta più fasi fisicamente eterogeneo due o più sostanze: chimicamente eterogeneo miscuglio eterogeneo
Miscugli omogenei ed eterogenei (IV)
9Miscugli omogenei e miscugli eterogenei (IV) I miscugli eterogenei possono presentare aspetti anche molto diversi al variare dello stato di aggregazione delle fasi che li costituiscono. La panna è una schiuma. La maionese è un'emulsione. TT
I passaggi di stato
Passaggi di stato (I)
10I passaggi di stato (I) brinamento condensazione STATO AERIFORME temperatura crescente solidificazione evaporazione Nei solidi, le particelle sono vicine e ordinate. STATO LIQUIDO Nei liquidi, le particelle sono vicine e distribuite disordinatamente. Negli aeriformi, le particelle sono distanti e distribuite disordinatamente. STATO SOLIDO fusione sublimazione
Passaggi di stato (II)
11I passaggi di stato (II)
- La fusione è il passaggio dallo stato solido allo stato liquido.
- L'evaporazione è il passaggio dallo stato liquido allo stato di vapore.
- La sublimazione è il passaggio diretto dallo stato solido allo stato di vapore.
0 0
Passaggi di stato (III)
12I passaggi di stato (III)
- La condensazione è il passaggio dallo stato di vapore allo stato liquido.
- La solidificazione è il passaggio dallo stato liquido allo stato solido.
- Il brinamento è il passaggio diretto dallo stato di vapore allo stato solido.
Passaggi di stato (IV)
13I passaggi di stato (IV) Ogni sostanza pura ha una curva di riscaldamento e temperature di fusione e di ebollizione caratteristiche in funzione della pressione a cui avviene il passaggio di stato. solido solido + liquido liquido liquido + vapore vapore t (°C) 1 100 E D sosta termica ebollizione B C 0 A sosta termica fusione -18 tempo
Passaggi di stato (V)
14I passaggi di stato (V) Ogni sostanza pura ha una curva di raffreddamento attraverso la quale si distinguono:
- temperatura di condensazione;
- temperatura di solidificazione.
vapore vapore + liquido liquido liquido + solido solido t (ºC) A sosta termica condensazione 100 B C Durante le soste termi- che, la temperatura ri- mane costante. sosta termica solidificazione 0 D E tempo
La pressione e i passaggi di stato
Pressione e passaggi di stato (I)
15La pressione e i passaggi di stato (I) La tensione di vapore di un liquido, a una data temperatura, è la pressione che esercita un vapore in equilibrio con il proprio liquido puro, ed è tanto più alta quanto maggiore è la temperatura. Dal pallone, contenente acqua distillata, viene allontanata l'aria. Dalla superficie dell'acqua comincia a liberarsi del vapore, che genera una pressione. La pressione aumenta, fino a quando non si stabilizza (tensione di vapore). 150 00 15 5 50
Pressione e passaggi di stato (II)
16La pressione e i passaggi di stato (II) La temperatura di ebollizione di un liquido è la temperatura a cui la tensione di vapore uguaglia la pressione esterna: maggiore è la pressione, più difficile è l'ebollizione del liquido.
Pressione e passaggi di stato (III)
17La pressione e i passaggi di stato (I La fusione e la solidificazione sono poco influenzate dalla pressione esterna: infatti sono passaggi caratterizzati da piccoli cambiamenti di volume, non particolarmente contrastati da pressioni elevate.
Metodi di separazione di miscugli e sostanze
Metodi di separazione (I): Filtrazione
18I principali metodi di separazione di miscugli e sostanze (I) La filtrazione è il metodo per separare, per mezzo di filtri, i materiali solidi da un miscuglio liquido o gassoso. Miscuglio eterogeneo acqua-ioduro di piombo, sale giallo, insolubile Il precipitato solido giallo (ioduro di piombo) si è depositato sulla superficie del filtro. Il filtrato è limpido: il componente solido è rimasto sul filtro.
Metodi di separazione (II): Centrifugazione
19I principali metodi di separazione di miscugli e sostanze (II) La centrifugazione è il metodo per separare miscugli eterogenei di liquidi e/o solidi aventi densità diversa. B
Metodi di separazione (III): Stratificazione, Estrazione, Flottazione
20I principali metodi di separazione di miscugli e sostanze (II
- La stratificazione è utilizzata per separare liquidi con densità diversa, come acqua e olio.
- L'estrazione è il metodo per separare i componenti di un miscuglio per mezzo di un solvente.
- La flottazione è usata per esempio nell'estrazione del rame dai suoi minerali.
Metodi di separazione (IV): Cromatografia
21I principali metodi di separazione di miscugli e sostanze (IV) La cromatografia è il metodo per separare i componenti di un miscuglio che si spostano con velocità diverse su un supporto (fase fissa), trascinati da un solvente (fase mobile). La fase mobile trascina con sé i diversi componenti del miscuglio iniziale. La separazione dei componenti dipende anche dalla loro interazione con la fase mobile e con la fase fissa. 00€ Osserviamo la separa- zione dei componenti dell'inchiostro di una penna, utilizzando come supporto la carta da fil- tro e come fase mobile alcol etilico.
Metodi di separazione (V): Distillazione
22I principali metodi di separazione di miscugli e sostanze (V) La distillazione si basa sulla diversa volatilità dei componenti di miscele liquide. Minore è la temperatura di evaporazione, maggiore è la volatilità. 200 g 8 23