Elementi di Biochimica e Biologia Cellulare: matrice extracellulare e proteine
Documento di Università su Elementi di Biochimica e Biologia Cellulare. Il Pdf, utile per lo studio della Biologia a livello universitario, esplora la matrice extracellulare, gli amminoacidi, i peptidi e le quattro strutture proteiche, con focus sui legami chimici e le modificazioni post-traduzionali.
Mostra di più24 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Matrice Extracellulare (ECM)
È tutto l'ambiente esterno alla cellula. Si chiama matrice perché è costituita principalmente da componenti non cellulari.
- Fibroblasti: sono quelle cellule deputate nella sintesi dei componenti non cellulari della matrice, come il collagene. Ad esempio, nel tumore, ci sono degli specifici fibroblasti, CAFs, fibroblasti associati al tumore, che sintetizzano una matrice che è tipica del tessuto tumorale, perché il tumore ha una matrice leggermente diversa, è più densa, più compatta, perché limita l'accessibilità dei farmaci;
- Macrofagi: quelle cellule che fagocitano tutto l'estraneo, come infezioni;
- Lamina basale: è una forma specializzata di matrice extracellulare, che si trova attorno alle cellule, sotto strati di cellule epiteliali, prima della matrice extracellulare; ogni tessuto ha la sua specifica lamina basale;
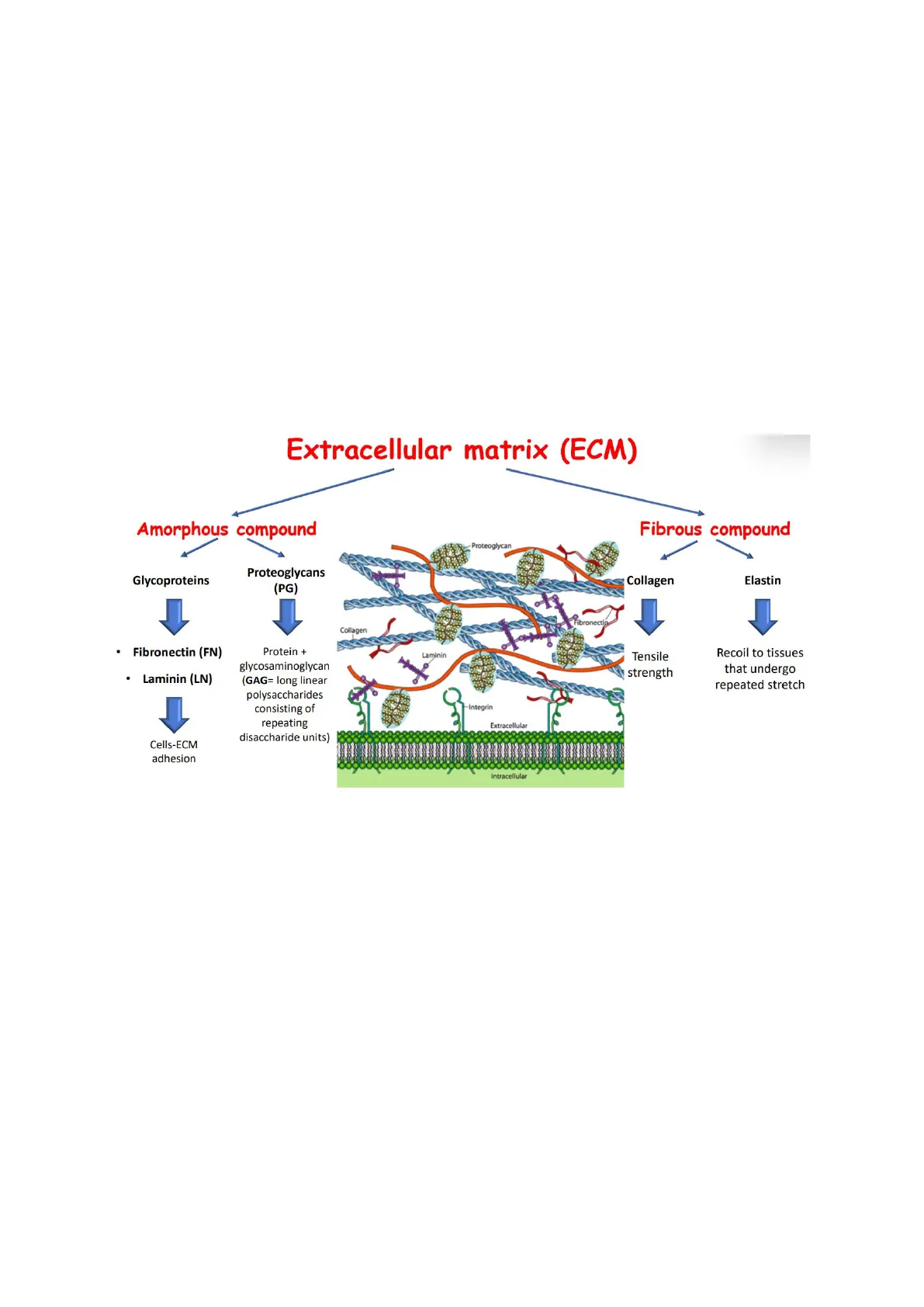
Extracellular matrix (ECM) Amorphous compound Fibrous compound -Proteoglycan Glycoproteins Proteoglycans (PG) Collagen Elastin Fibronectip Collagen · Fibronectin (FN) · Laminin (LN) Protein + glycosaminoglycan (GAG= long linear polysaccharides consisting of repeating disaccharide units) Laminin Tensile strength Recoil to tissues that undergo repeated stretch -Integrin Extracellular Cells-ECM adhesion Intracellular
- Proteoglicani: proteine, a cui sono associati glicosaminoglicani (GAG), che sono delle catene di polisaccaridi;
- Laminina: glicoproteina, residente nella membrana basale, che si ancora principalmente alle integrine (proteine) nella membrana delle cellule bersaglio e ancorandosi dà una risposta, che sono coinvolte nella proliferazione cellulare, nella differenziazione, nell'adesione, nella migrazione, nell'angiogenesi (formazione di nuovi vasi sanguigni);
- Fibronectina: glicoproteina, che svolge un ruolo importante nella riparazione dei tessuti. È organizzata in una rete di fibrille e si lega alle integrine;
- Elastina: componente fibrosa, è una proteina, dà elasticità ai tessuti, permettendo loro di allungarsi quando necessario e poi ritornare al loro stato originale;
- Collagene: proteina più abbondante nel nostro corpo, con una struttura molto complessa.
Amminoacidi, Peptidi e Proteine
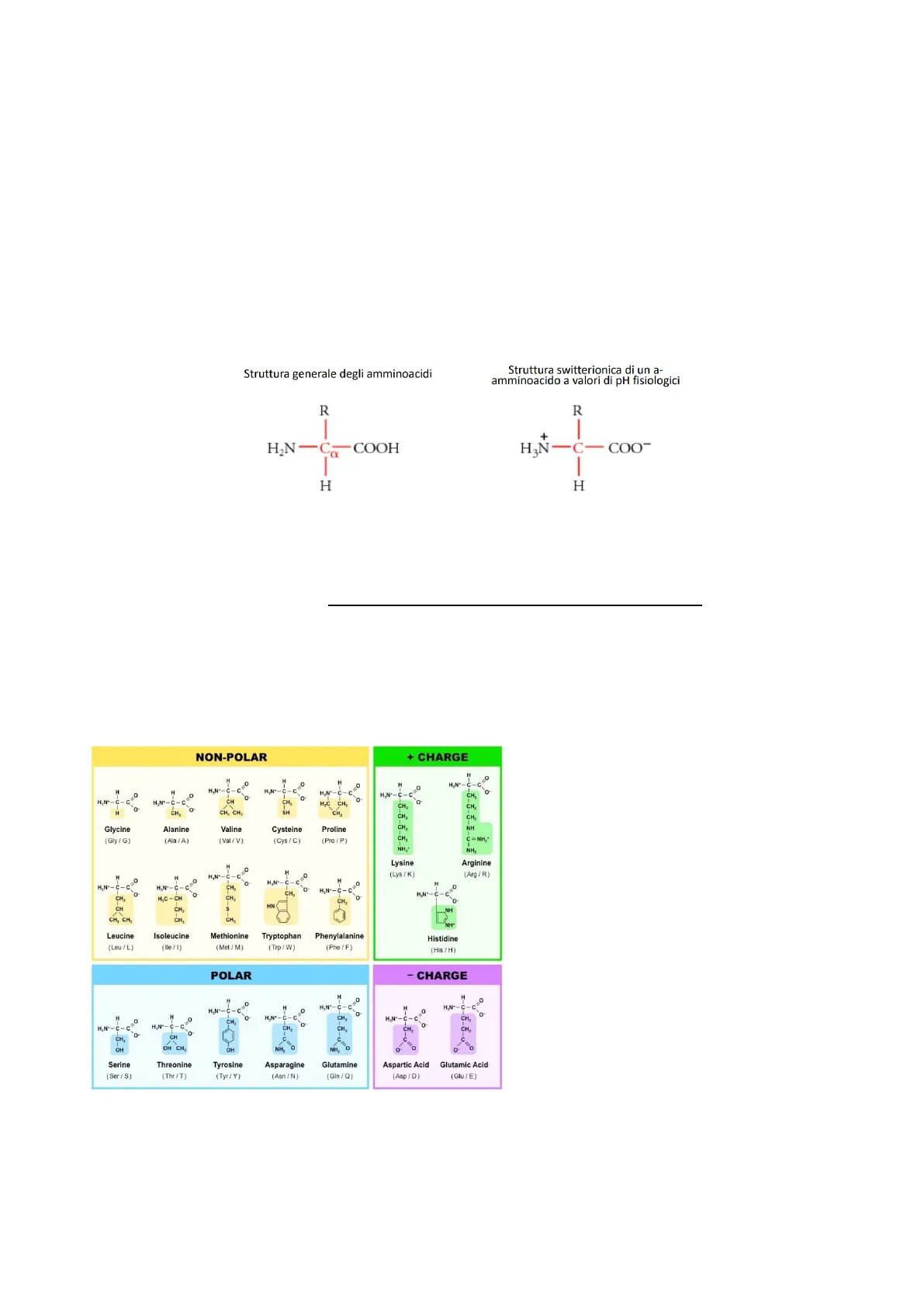
10Elementi di Biochimica e Biologia Cellulare Gli amminoacidi sono i mattoni che costituiscono le proteine e si organizzano nella formazione di catene polipeptidiche. Hanno tutti una struttura comune: un carbonio centrale a, che è legato ad un gruppo amminico NH2, un gruppo carbossilico COOH, un idrogeno H e ad una catena laterale R, diversa per ogni amminoacido, per cui è R a conferire a ciascun amminoacido le proprie caratteristiche specifiche. A pH fisiologico (7,2 - 7,4), gli amminoacidi si trovano in forma switterionica, cioè, sono protonati del gruppo amminico NH3+ e de-protonati del gruppo carbossilico COO.
Struttura degli Amminoacidi
Struttura generale degli amminoacidi R - H H2N-C-COOH Struttura switterionica di un a- amminoacido a valori di pH fisiologici R I + H3N-C-COO- I H Negli organismi viventi ci sono 20 tipi di amminoacidi diversi. In tutti gli amminoacidi, il carbonio a è legato a quattro sostituenti diversi, perciò, si dice che è un centro chirale. In particolare, proprio perché è un carbonio chiarale, è possibile avere due conformazioni, due enantiomeri dell'amminoacido, cioè due facce speculari: enantiomero L ed enantiomero D. Come si capisce se un amminoacido è in forma D o L? La luce polarizzata viene indirizzata verso il campione che contiene l'amminoacido di interesse e questa viene deviata verso destra o verso sinistra. Dobbiamo, però, utilizzare un riferimento, la gliceraldeide, che può essere sintetizzata con D-gliceraldeide o come L-gliceraldeide. Quindi, se metto nel polarimetro la L-gliceraldeide e un amminoacido e la luce polarizzata viene deviata dallo stesso lato della L-gliceraldeide, avrò un L- amminoacido; se è deviata in direzione opposta, avrò un D-amminoacido. Esistono diversi tipi di amminoacidi NON-POLAR + CHARGE H H,Nº-C- H,Nº- エ ー U-H H I-0- H A,N .- C-C .0 H,Nº- エ ー ひ ー モ ー み エ ー じ ー ち 、 Amminoacidi con catena laterale non polare H.Nº- o CH2 CH CH, O -c H,Nº CH HỌC CH, CH2 La glicina, con sostituente H, è una molecola -3-0 O CH, CH H,N .- C-C CH non chirale ed è l'unico amminoacido ad CH, сн, сн, Glycine (Gly/G) Alanine (Ala /A) Valine (Val /V) Cysteine (Cys/C) Proline (Pro / P) NH NH esserlo; la metionina è il primo amminoacido C = NH, CH Lysine Arginine (Arg /R) H -C H H H O H H,N+-C-C NH I-0-6 CH, I-U H,N+-C-C CH H,Nº-C- 0 `o H,Nº- -C H,Nº- CH (Lys/K) della sintesi di una catena polipeptidica; la prolina è un imminoacido e l'unico ad esserlo, H,N+-C-C HỌC - CH CH CH HN CH. S quindi, viene erroneamente chiamato CH, CH, CH, CH. NH- Leucine Methionine Tryptophan Phenylalanine (Phe /F) (Trp /W) (Met /M) Histidine (His / H) (Leu /L) Isoleucine (Ile /1) amminoacido, poiché ha un gruppo imminico, invece, di un gruppo amminico. Essendo un POLAR - CHARGE imminoacido, ha un ruolo fondamentale H O H H,Nº-C-C CH -C H.N H soprattutto nella formazione di strutture 0 CH, HẸN *- H,N+-C-C I- I- CH 0 C HẸN H.N C. CH C. H,Nº-C secondarie delle proteine. Infatti, funge da CH CH OH CH, CH, OH OH CH, NH, 0 Aspartic Acid Glutamic Acid NH, Serine (Ser /S) Glutamine (Gin / Q) (Asp /D) (Glu / E) punteggiatura nelle alpha eliche. Può, inoltre, Threonine Asparagine (Asn /N) (Thr /T) Tyrosine (Tyr /Y) assumere delle conformazioni particolari. La cisteina ha come catena laterale un SH (gruppo tiolico), che, avendo questo SH, può reagire con altre cisteine. In particolare, si può formare un legame S-S, che si chiama ponte disolfuro, tra due cisteine. Il ponte disolfuro è un'interazione che aiuta anche in quello che è il corretto raggiungimento della struttura primaria della proteina.
Amminoacidi con Catena Laterale Polare Non Carica
11Amminoacidi con catena laterale polare non carica La serina, la treonina, la tirosina hanno un gruppo -OH (per questo sono polari). La presenza del gruppo ossidrile è fondamentale, in quanto questi amminoacidi possono subire un processo, chiamato fosforilazione. Cosa vuol dire fosforilare un amminoacido? Vuol dire che il suo gruppo -OH viene sostituito da un gruppo fosfato PO4". Il gruppo fosfato è molto più grande di OH e soprattutto è carico, essendo carico, avrà interazioni con una catena laterale di un altro amminoacido. Quindi, si può far cambiare la conformazione della proteina. Cambiare la conformazione di una proteina, vuol dire anche cambiare l'attività di quella proteina. Ad esempio, molti enzimi vengono regolati da processi di fosforilazione o di de-fosforilazione, in una fase possono essere attivi o inattivi. La chinasi va ad aggiungere il fosfato all'amminoacido; quindi, il processo di fosforilazione è sempre mediato da enzimi che si chiamano chinasi. Nel momento in cui abbiamo il fosfato, l'amminoacido cambia conformazione e la chinasi si attiva e può fosforilare altre proteine. Questa chinasi stessa può, però, essere defosforilata dalla fosfatasi e diventa inattiva, quindi, non può fosforilare altre proteine. La fosfatasi è quell'enzima che inattiva la chinasi. Il processo di fosforilazione può, quindi, regolare l'attività di un enzima.
Regolazione Enzimatica tramite Fosforilazione
Phosphatase Kinase P P OFF ON Activation Phosphatase Kinase P P ON OFF Inactivation
Amminoacidi con Catena Laterale Polare Carica
Li distinguiamo in: amminoacidi con catene laterali acide, come acido aspartico (può essere fosforilato, solo se posto in ambienti idrofobici; es. nella pompa sodio/potassio) e acido glutammico, e amminoacidi con catene laterali basiche, come istidina, lisina e arginina.
Legame Peptidico e Struttura Primaria
Gli amminoacidi si legano fra di loro, tramite il R1 O legame peptidico, andando a formare quella che è 1 H // // + O la struttura primaria delle proteine. Il legame H3N+-C- H3N+ -C -C-C peptidico è un legame che avviene tra il gruppo Amino 1 H O R2 Carboxyl group group carbossilico di un amminoacido e il gruppo amminico di un altro amminoacido, con la liberazione di una molecola di acqua. Infatti, il R1 H2O gruppo carbossilico perde un ossigeno e il gruppo O エ –– O= Carboxyl Amino (N- terminal) H3N+-C-C-N-C-C 1 H / R2 end O (C-terminal) end amminico perde due idrogeni. Questo legame viene chiamato peptidico perché ha delle proprietà particolari. Quando si forma un legame H peptidico, in genere, gli amminoacidi coinvolti Peptide @ 2010 Pearson Education, Inc. bond assumono una configurazione che si dice trans, cioè i gruppi R sono in lati opposti. Se fossero stati entrambi nello stesso lato, sarebbero stati in cis. È normale che assumano questa configurazione ed è anche abbastanza logico perché, se immaginiamo che i gruppi R possono essere anche molto grandi, come per esempio il gruppo R del triptofano, ovviamente se li mettiamo in cis ci sarà un ingombro sterico, se invece li mettiamo in trans non ci sarà questo ingombro. In particolare, però, c'è un amminoacido, la prolina, che ha la catena laterale condensata con il gruppo amminico, ciò vuol dire che la sua catena laterale è molto piccola, infatti, può assumere una configurazione in cis, in quanto l'ingombro sterico sarebbe talmente piccolo che non creerebbe problemi. Se immaginiamo tante proline, una 12dopo l'altra, tutte in configurazione cis, il fatto che abbiano questa configurazione man mano le fa curvare. Nel caso di una conformazione trans avremo invece una retta, perché le catene laterali si alternano. Il carbonio e l'azoto, che fanno parte del legame peptidico, sono sullo stesso piano con l'H, che è legato all'azoto del vecchio gruppo amminico, che, quindi, è imminico, e l'ossigeno del gruppo carbossilico che, dopo il legame peptidico, è diventato gruppo carbonilico. Questo ha un ruolo molto importante, perché il legame peptidico è a cavallo tra un legame singolo e un legame doppio. Se guardiamo i quattro atomi coinvolti nel legame (carbonio, azoto, ossigeno legato al carbonio, e idrogeno legato all'azoto), ci sono degli elementi che sono fortemente elettronegativi (tendenza di un atomo ad attrarre a sé elettroni condivisi): ossigeno e azoto, che tendono ad acquistare elettroni. Ci saranno, quindi, degli elettroni che andranno oscillando e non staranno fissi, per cui ci sono queste forme di risonanza, a causa degli elettroni che spaziano tra azoto e ossigeno. Ciò vuol dire che il legame è parzialmente singolo per il 60% in alcune fasi e parzialmente doppio per il 40% in altre. Non vi può, pertanto, essere libera rotazione attorno al legame peptidico, per questa doppia natura, in quanto gli atomi di carbonio, azoto, ossigeno e idrogeno si trovano sullo stesso piano. Ci può essere, però, una rotazione tra il carbonio a e l'azoto precedente, e il carbonio a e il carbonio successivo di un gruppo carbossilico.
Rotazione e Strutture Secondarie
R 124À Estremità C-terminale 1,53 Å 1,46 Å C Co N o Ca 1,32 À Estremità N-terminale H L JL N-Ca Ca-C C-N (b) Foglietti Tripla elica del collagene ß antiparalleli Questa rotazione permette la Le a eliche sinistrorse con estensione di oltre 7 Foglietti Foglietti ß avvolti in modo destrorso ß paralleli residui amminoacidici sono teoricamente possibili ma non sono mai state osservate nelle proteine. formazione sia delle strutture +180 secondarie che di quelle terziarie. +180 cx-elica sinistrorse 120 In particolare, la rotazione 120 60 60 0 determina degli angoli, chiamati + e ¢. Ma non possono essere 0 a-elica -60 (gradi) + (gradi) -60 - destrorsa assunte tutte le diverse tipologie -120 +180 di conformazione. Questo è stato -120 dimostrato dallo scienziato -180 0 -180 -180 -180 0 +180 Ramachandran, che si era posto + (gradi) (b) + (gradi) la domanda se fosse o meno possibile assumere tutte le conformazioni o solo alcune. Ha iniziato a studiare, facendo dei grafici, chiamati grafici di Ramachandran, dove ha messo in relazione gli angoli ų e gli angoli . Analizzando molte proteine, ha visto che avevano delle zone in cui c'era un maggior numero di angoli ų e + dello stesso tipo, come descritto dal grafico. Controllando cosa succedesse alle proteine quando avevano valori specifici di ų e ¢, ha visto che le proteine assumevano delle configurazioni particolari. In particolare, ha scoperto quella che noi chiamiamo struttura secondaria di una proteina, riscontrandone due tipi: a elica e foglietto B. 13