Lezione 2: Concentrazioni, Diluizioni ed Errori in Chimica
Documento universitario sulle concentrazioni, diluizioni ed errori. Il Pdf, utile per lo studio della Chimica a livello universitario, esplora i concetti di molarità, le tipologie di errori strumentali, di metodo e personali, e le strategie per la loro mitigazione.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
PREPARAZIONE DI UNA SOLUZIONE MADRE E DILUIZIONI
L'ERRORE DELLA MISURA: TIPOLOGIE DI ERRORI, PRECISIONE ED ACCURATEZZA, CIFRE SIGNIFICATIVE
Le soluzioni
- Soluzione, miscela omogenea di due o più sostanze con proprietà chimiche e fisiche identiche in ogni sua parte.
- Le sostanze presenti in minor quantità sono chiamate soluti, sono disperse uniformemente nella sostanza presente in maggior quantità, chiamata solvente.
- Soluzione acquosa-> soluzione in cui il solvente è l'acqua.
- Soluzione non-acquosa-> il solvente non è acqua.
- Per caratterizzare una soluzione è necessario conoscere i componenti e il rapporto quantitativo in cui essi stanno tra loro (concentrazione).
MODI DI ESPRIMERE LA CONCENTRAZIONE DELLE SOLUZIONI
Esistono quattro modi fondamentali di esprimere le concentrazioni delle soluzioni:
- concentrazione molare
- concentrazione percentuale
- rapporti di volume soluzione-diluente
- funzioni-p
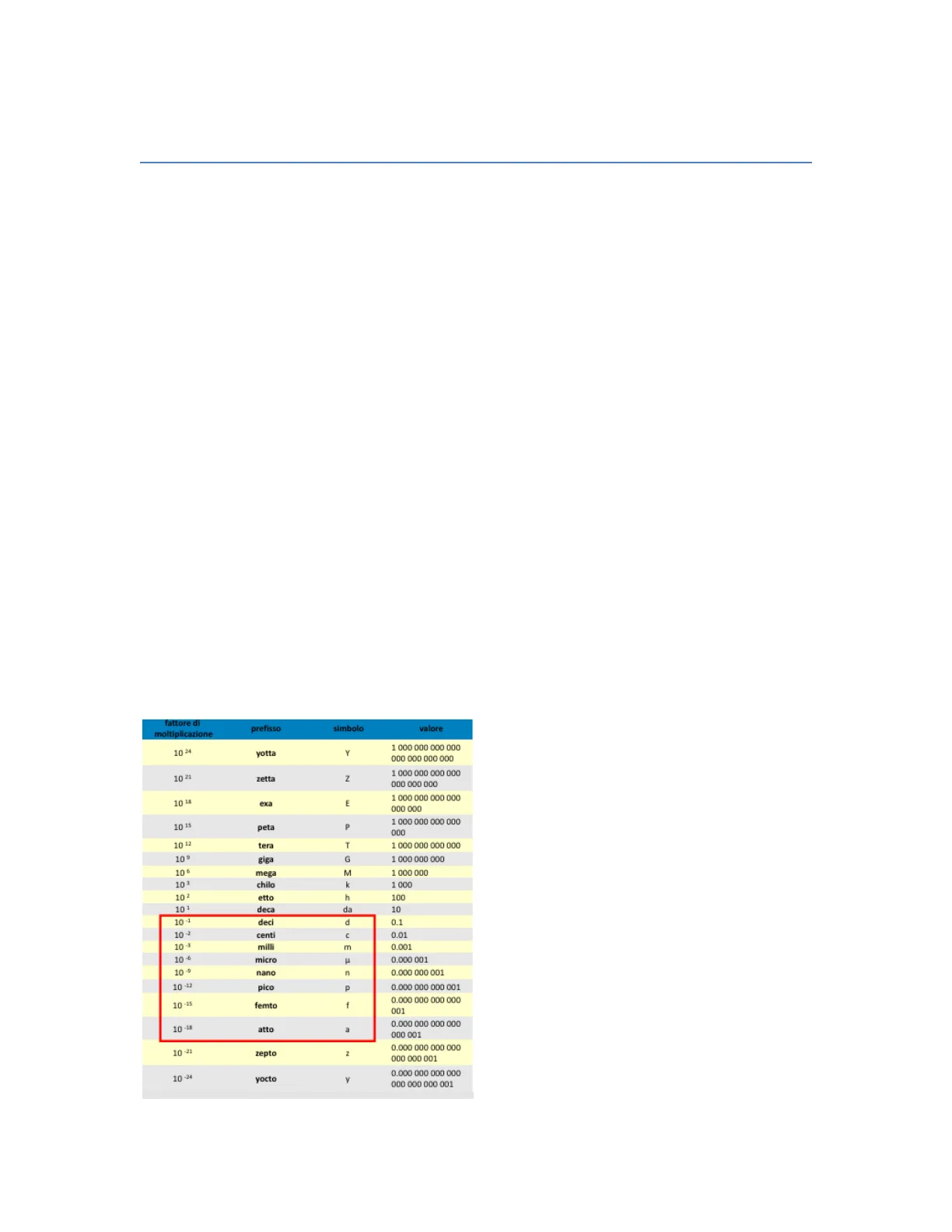
Multipli e sottomultipli nel Sistema Internazionale
fattore di moltiplicazione prefisso simbolo valore 10 24 yotta Y 000 000 000 000 10 21 zetta Z 1 000 000 000 000 000 000 000 1 000 000 000 000 10 18 exa E 000 000 10 15 peta p 000 10 12 tera T 1 000 000 000 000 10 º giga G 1 000 000 000 10 € mega M 1 000 000 103 chilo k 1 000 102 etto h 100 10 deca da 10 10-1 dec d 0.1 10-2 centi C 0.01 10-3 milli m 0.001 10 -6 micro 1 0.000 001 10 -9 nano 0.000 000 001 10 -12 pico a 0.000 000 000 001 10 -15 femto f 0.000 000 000 000 001 10-18 atto 2 0.000 000 000 000 000 001 10 -21 zepto 7 0.000 000 000 000 000 000 001 0.000 000 000 000 10 -24 yocto V 000 000 000 001 1 000 000 000 000
Comuni unità metriche di conversione
milli m 10-3 micro μ 10-6 nano n 10-9
Relazioni comuni tra volumi
1 dm3 1000 ml 106 μl 10-3 dm3 1.0 ml 1000 ul 106 nl 0.100 ml 100 ul
Relazioni comuni tra grammi
1.000 g 1000 mg 106 µg 0.100 g 100 mg 1 mg 1000 µg 106 ng
MOLARITÀ
CONCENTRAZIONE MOLARE
La concentrazione molare cx della soluzione della specie chimica X è il numero di moli di quella specie contenuto in un litro di soluzione (non in un litro di solvente). In termini del numero di moli di soluto, n, e del volume di soluzione, V, si può scrivere mol soluto concentrazione molare =- Volume in L L'unità di misura della concentrazione molare è la molarità, M, che ha le dimensioni di mol/L, o mol L-1. Esprime anche il numero di millimoli di soluto per millilitro di soluzione. La concentrazione molare si può esprimere in due modi. ·Concentrazione molare analitica (numero di moli di soluto totali, indipendentemente da ciò che accade in soluzione). · Concentrazione molare di equilibrio (numero di moli di una particolare specie in una soluzione all'equilibrio). ·Concentrazione molare analitica ... indipendentemente da ciò che accade in soluzione H2SO4 1M equivale a 1 mol, o 98 g di H2SO4 puro in H2O, diluendo fino a 1 L. ·Concentrazione molare di equilibrio ... in una soluzione all'equilibrio La concentrazione molare di equilibrio di H2SO4 in una soluzione avente una concentrazione analitica 1M è in realtà 0! Questo perché l'acido solforico è completamente dissociato in una miscela di H+, HSO4meno ed SO4 2-con le rispettive concentrazioni di equilibrio 1,01; 0,99; 0,01 M.
CONCENTRAZIONE PERCENTUALE, RAPPORTI DI VOLUME E FUNZIONI-p
CONCENTRAZIONE PERCENTUALE->
- Percentuale in peso (p/p) p/p = peso del soluto/peso della soluzione x 100%
- Percentuale in volume (v/v) v/v = volume del soluto/volume della soluzione x 100%
- Percentuale in peso/volume (p/v) p/v = peso del soluto, g/volume della soluzione, mL x 100%
RAPPORTI DI VOLUME SOLUZIONE-DILUENTE->
La composizione di una soluzione diluita a volte viene specificata in termini di volume di una soluzione più concentrata e di volume di solvente da usare per diluirla. Es.: soluzione 1:4 di HCl ovvero 4 volumi di H2O per ciascun volume di HCl.
FUNZIONI-p->
La funzione-p o valore-p è il logaritmo negativo (in base 10) della concentrazione molare di quella specie. Così, per la specie X si avrà pX = - log [X] Vantaggio di esprimere piccole concentrazioni con piccoli numeri positivi. Per soluzioni molto diluite, proprie della chimica analitica, la concentrazione viene espressa in parti per milione (ppm) o parti per miliardo, cioè biliardo (ppb). 1 ppm = 1 mg/L Parti per milione (ppm): corrisponde a una parte di soluto per 1 milione di parti di soluzione (106). Parti per miliardo (bilione) (ppb): corrisponde a una parte di soluto per 1 miliardo di parti di soluzione (109). Parti per trilione (ppt): corrisponde a una parte di soluto per 1 trilione di parti di soluzione (1012).
p/p V/V p/v ppm ug/g; mg/kg nL/ml; µL/L µg/ml; mg/L ppb ng/g; µg/Kg nL/L ng/ml; µg/L ppt pg/g; ng/Kg PL/L pg/ml; ng/L 1.0 µg/L 0.001 mg/L SAME NUMBER 0.001 ppm 1.0 ppb
MATRACCIO
TABELLA 3.3 Caratteristiche del matracci tarati di classe A*
Tipo di matraccio (mL) Massimo errore ammissibile (mL) 1 ± 0.01 ± 0.015 5 ± 0.02 10 ± 0.02 25 ± 0.03 50 ± 0.05 60 ± 0.05 100 ± 0.08 110 ± 0.08 200 ± 0.10 250 ± 0.12 500 ± 0.20 1000 ± 0.30 2000 ± 0.50 *Le proprietà riportate in questa tabella sono quelle specificate dalla American Society for Testing Materials. Il termine "tolleranza" viene spesso impiegato al posto di "massimo errore ammissibile" nel descrivere le proprietà di questi dispositivi. Tappo rimovibile Linea di riferimento del volume dichiarato Indicazione che il matraccio è progettato "per contenere" il volume dichiarato A Classe e volume del matraccio 20℃ 500 ml = 0.20 Temperatura di taratura Massimo errore ammissibile sul volume
FIGURA 3.7 Aspetto generale di un matraccio tarato. Sul collo del matraccio è incisa una linea che indica il livello che il menisco deve raggiungere affinché il volume di liquido nel matraccio sia uguale al volume dichiarato. L'entità di questo volume e la temperatura alla quale è stata effettuata la taratura del matraccio sono riportate nella parte inferiore del pallone insieme al simbolo "TC", il quale indica che il matraccio è stato progettato "per contenere" la quantità di liquido indicata. 45 1.40 35 30 25 20 15 10 5 50 ml 20℃ Buretta Pipetta di Mohr E 10 Pipetta sierologica 5 ml 5 ml ± 0.01 ml 20℃ Pipetta di Ostwald-Folin
FIGURA 3.9 Esempi di buretta, pipetta di Mohr, pipetta sierologica e pipetta di Ostwald-Folin. Temperatura di taratura Indicazione che la pipetta è progettata "per trasferire" il volume dichiarato Tipo di pipetta (mL) Massimo errore ammissibile (mL) Tempo minimo di flusso (s) 0.5 ± 0.006 5 1 ± 0.006 10 ± 0.006 10 3 ± 0.01 10 ± 0.01 10 ± 0.01 15 ± 0.02 15 ± 0.02 15 8 ± 0.02 15 ± 0.02 15 10 ± 0.02 15 15 ± 0.03 25 20 ± 0.03 25 25 ± 0.03 25 30 ± 0.05 25 40 ± 0.05 25 50 ± 0.05 25 75 ± 0.08 30 100 ± 0.08 30 6 8 10 in 1/10 ml TD 20 ℃ D = 1 E 2 3 9 Volume della pipetta (in mL) 25 Punta affusolata per -il rilascio del liquido
FIGURA 3.8 Aspetto generale di una pipetta volumetrica. Sul collo della pipetta è incisa una linea ad indicare il livello che il menisco del liquido deve raggiungere affinché il suo volume sia pari al volume dichiarato della pipetta. L'entità di questo volume e la temperatura alla quale è stata fatta la taratura sono riportate di lato insieme alla sigla "TD", la quale sta a significare che la pipetta è stata progettata "per erogare" la quantità di liquido indicata senza fare ricorso a forze o pressioni aggiuntive.
TABELLA 3.4 Caratteristiche delle pipette volumetriche di classe A*
Classe della pipetta Linea di riferimento del volume dichiarato Massimo errore ammissibile sul volume - - 10 ml in 1/10 ml 5 *Le proprietà riportate sono quelle specificate dalla American Society for Testing Materials. Il termine "tolleranza" è spesso impiegato al posto di "massimo errore ammissibile" nel descrivere le proprietà di questi dispositivi. Il "tempo minimo di flusso" è il più breve intervallo di tempo accettabile per il trasferimento di tutto il liquido nella pipetta in un altro contenitore.
PREPARAZIONE DI UNA SOLUZIONE MADRE (detta anche stock solution)
PESATA DIRETTA IN UN PALLONE TARATO->
La preparazione diretta di una soluzione standard richiede l'introduzione di una massa di soluto in un pallone tarato. Un imbuto per polveri ridurrà al minimo le possibili perdite di solido durante il trasferimento.
TRASFERIMENTO QUANTITATIVO DI UN LIQUIDO IN UN PALLONE TARATO->
Inserite un imbuto nel collo di un pallone tarato usando una bacchetta da mescolamento per dirigere il flusso di liquido dal beaker nell'imbuto. Fate cadere l'ultima goccia di liquido attaccata al beccuccio del beaker usando la bacchetta da mescolamento.
DILUIZIONE FINO AL SEGNO->
Dopo avere trasferito il soluto riempite il pallone sino a circa la metà ed agitate il contenuto per accelerare la soluzione. Aggiungete ancora solvente e mescolate bene. Portate il livello del liquido quasi fino al segno lasciate scolare il liquido e poi portate definitivamente a volume.
Cobalt(II) chloride dihydrate (CoCl2. 2H2O) Ethanol 500 ml 500 mL 0.0 g (a) An amount of solute is weighed out on an analytical balance and then (b) A portion of the solvent is added to the volumetric flask. (c) The mixture is swirled until all of the solute is dissolved. (d) Additional solvent is added up to the mark on the volumetric flask.
DILUIZIONE DI UNA SOLUZIONE
... volume di soluzione concentrata da prelevare? ... fino a che volume diluire? Mark Volumetric pipette Stock solution (a) A volume (V3) containing the desired moles of solute (M3) is measured from a stock solution of known concentration. (b) The measured volume of stock solution is transferred to a second volumetric flask. Solvent Mark Dilute solution (c) The measured volume in the second flask is then diluted with solvent up to the volumetric mark [(V5)(Ms) = (Va)(Ma)]. Come preparare una soluzione 10 ppm a partire da una soluzione 100 ppm? Il calcolo in questo caso è molto semplice, basta eseguire una diluizione 1 a 10. Per esempio, per preparare 10 mL di soluzione, basterà utilizzare 1 mL di soluzione 100 ppm e portare a volume TOTALE 10 mL. Ma esiste anche una formula: Ci x Vi = Cf x Vf 500 mL Mark 500 ml