Interazioni fra molecole: interazioni intermolecolari in Chimica
Slide dall'Università sulle interazioni fra molecole e interazioni intermolecolari. Il Pdf esplora le forze attrattive elettrostatiche che influenzano lo stato della materia, classificando le interazioni in ion-dipolo, legame a idrogeno, dipolo-dipolo, ion-dipolo indotto, dipolo-dipolo indotto e forze di dispersione, per lo studio della Chimica a livello universitario.
Mostra di più26 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Interazioni Intermolecolari
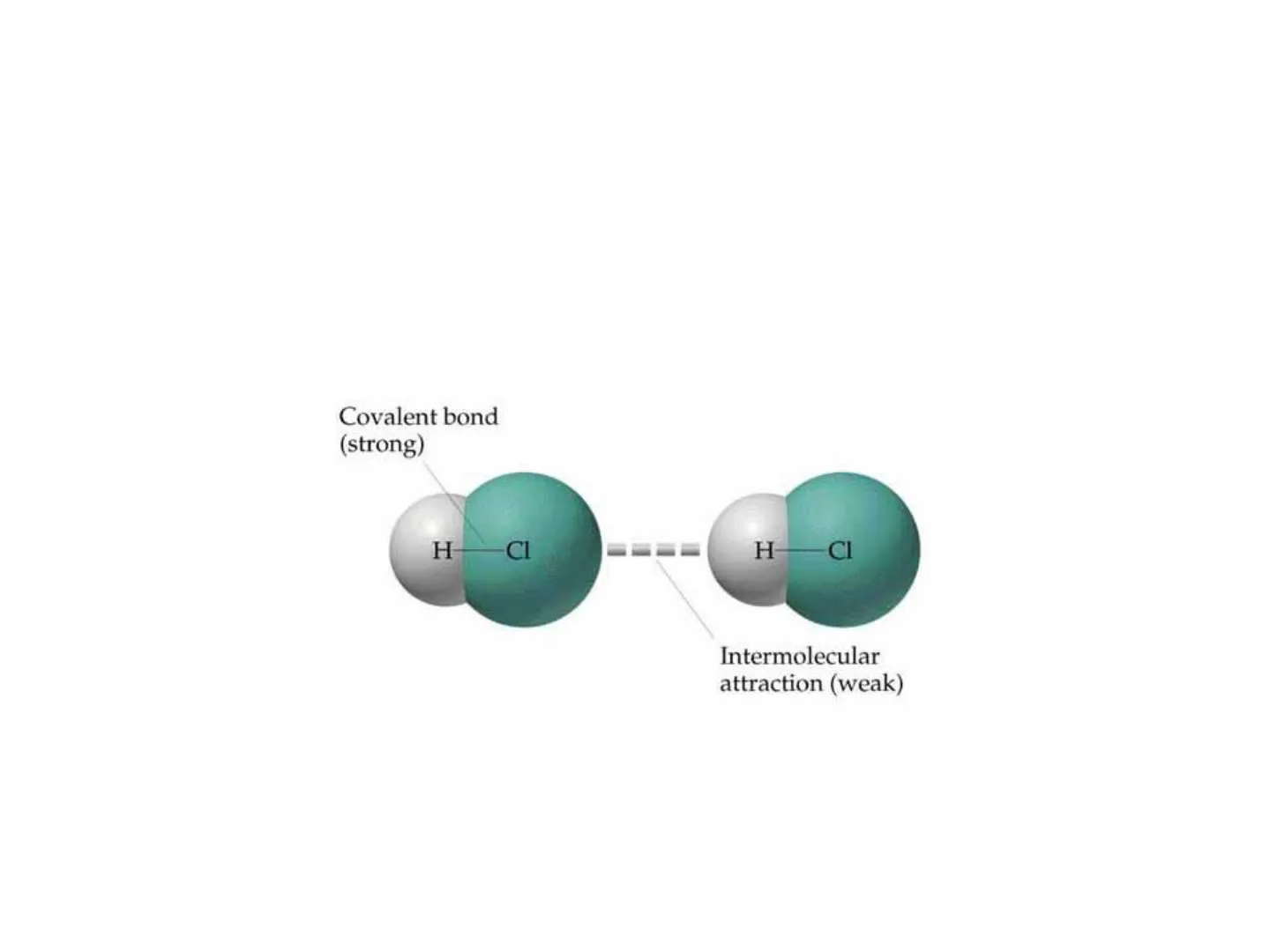
Sono forze attrattive di natura elettrostatica che si esercitano fra molecole neutre e fra molecole neutre e ioni. Le energie di attrazione coinvolte sono molto inferiori a quelle relative ai legami covalenti o alle interazioni elettrostatiche fra ioni (legame ionico). Per questo sono anche dette "interazioni deboli".
Covalent bond (strong) (431 KJ /mol) H -CI H CI Intermolecular attraction (weak) (16 KJ/mol)
Anche se deboli hanno un ruolo fondamentale nel determinare il comportamento di molte sostanze (stato di aggregazione: gassoso, liquido o solido, punto di fusione e di ebollizione, solubilità ecc ... ).Le forze intermolecolari rispondono dell'esistenza delle diverse fasi della materia.
Cl2 2 Br 2 2 I Forza delle interazioni intermolecolari crescente
La temperatura alla quale un gas condensa a liquido o a solido dipende dall'intensità delle forze attrattive tra le sue molecole.Tutte le interazioni interioniche e quasi tutte quelle intermolecolari sono riconducibili all'interazione elettrostatica tra due cariche Ep = P 9192 ΑπεργDistribuzione elettronica in una molecola
Le molecole dinucleari neutre polari possiedono un momento di dipolo permanente (u) dovuto alla distribuzione non omogenea degli elettroni di legame fra due atomi a diversa elettronegatività (es. H+-CIÒ-). Molecole polinucleari con legami covalenti polari possiedono un u permanente i dipendenza della loro forma ( es. CO2 apolare; SO2 polare). Nelle molecole apolari si creano dipoli istantanei a causa di una distribuzione non omogenea della densità elettronica sull'intera molecola e dipoli indotti dalla vicinanza con uno ione o un dipolo.
H CI (a) HCI is polar O C O (b) CO2 is nonpolar nucleus δ+ ô- electrons symmetrical distribution unsymmetrical distributionLe interazioni classificate: intermolecolari possono essere COSI
H2O + Na+ Methanol (CH3OH) + CHJOH Chloroform (CHCL) Ion-dipole H bond Dipole-dipole + Acetone (C3H6O) C6H14 C6H14 Octane (CgH18) Dipole-induced dipole Dispersion CI Hexane (C6H14) Ion-induced dipole
Forze Interioniche e Intermolecolari
Tabella 5.1 Forze interioniche e forze intermolecolariª
| Tipo di interazione | Energia tipica, kJ·mol-1 | Specie interagenti |
|---|---|---|
| Ione-ione | 250 | Solo ioni |
| Ione-dipolo | 15 | Ioni e molecole polari |
| Dipolo-dipolo | 2 | Molecole polari ferme |
| 0,3 | Molecole polari rotanti | |
| London (dispersione)b | 2 | Tutti i tipi di molecole |
| Legame a idrogeno | 10-20 | N, O, F; il collegamento è un atomo H condiviso |
ª La forza totale sperimentata da una specie è la somma delle forze alle quali essa può trovarsi soggetta. b Nota anche come interazione dipolo indotto-dipolo indotto.
Interazioni Ione - Dipolo Permanente
Si instaura tra uno ione e la parte della molecola polare che possiede carica opposta. Sono le interazioni intermolecolari più forti (ma meno di quelle interioniche ione-ione).
Na+ - - Na+ + CI- + CI - + - + - Polare Positive side Hydrogen Hydrogen 105° Oxygen Negative side
Idratazione e Solvatazione
Copyright &Pearson Education, Inc., publishing as Benjamin Cummings. http://www.youtube.com/watch?v=xdedxfhcpWo&feature=endscreen
Cristallizzazione
Quando i sali cristallizzano dalle soluzione acquose, gli ioni possono mantenere alcune delle molecole di acqua idratanti e dar luogo a idrati quali:
Na CO2 .10H O CuSO4 . 5H2O
La misura di tale idratazione dipende dalle dimensioni dello ione e dalla sua carica.
- I cationi piccoli (Li+, Be++) si circondano di (fino a) 15-20 molecole d'acqua in diversi gusci di idratazione.
- I cationi grandi non sono praticamente solvatati (Cs+,Rb+, NHÀ+)
Interazioni Dipolo-Dipolo
L'estremità positiva di una molecola polare (polo positivo) è attratta dalla estremità negativa (polo negativo) di un'altra molecola.
8+ 8- 8+ 8- 8+ 8- 8- S+ (a) Attraction (b) Attraction 8+ 8 8+ S+ L 8+ (c) Repulsion (d) Repulsion
La loro orientazione relativa (fianco a fianco o testa a coda) si risolve in una minore energia
Interazioni tra Molecole Non Polari
Dipolo-Dipolo Indotto (Forze di Induzione)
Una molecola polare, quale ad esempio l'acqua, quando si trova nelle vicinanze di una molecola non polare (ad esempio O) induce una distorsione della nuvola elettronica su quest'ultima creando un dipolo indotto. L'interazione fra il dipolo permanente sull'acqua e quello temporaneo (indotto) su O2 è detta dipolo-dipolo indotto.
8+ 8 8+ Il dipolo dell'acqua distorce la nuvola elettronica di 02 , trasfromandola in dipolo 8+ 8 8+Il processo di induzione di un dipolo è detto polarizzazione e il grado a cui la nuvola elettronica di un atomo o di una molecola può essere distorta è detto polarizzabilità ("mollezza") a dell'atomo o della molecola.
La polarizzabilità è tanto maggiore quanto la nuvola elettronica è estesa (lontana dal nucleo).
Essa, quindi, aumenta con l'aumentare del numero degli elettroni interni e in generale, per una certa serie di molecole con l'aumentare della massa molare.
2 Ep Oc - μία2 6 r
Dipolo Istantaneo-Dipolo Indotto (Forze di Dispersione o di London)
La prova che tra molecole apolari sussistono interazioni attrattive sta nel fatto che i gas nobili i quali, per essere monoatomici, sono inevitabilmente apolari, si possono liquefare. Gli elettroni negli atomi e nelle molecole si muovono continuamente e quando due atomi o due molecole non polari si avvicinano le attrazioni e le repulsioni tra gli elettroni ed i nuclei generano delle distorsioni nelle nuvole elettroniche e quindi dei dipoli istantanei (temporanei).
8+ 8- dipolo istantaneo molecola che subirà l'induzione 8+ 8- 8+ 8- dipolo istantaneo dipolo istantaneo indotto interazioni dipolo ist. - dipolo ist. indotto forze di London forze di dispersioneDipendono dalla polarizzabilità e dalle dimensioni e forma molecolare (le molecole allungate mostrano interazioni più forti).
Ep oc - 6 2 r
Si generano tra tutte le molecole o atomi ma per quelle non polari sono le uniche interazioni intermolecolari.
Aumenta la dimensione ed il numero di elettroni Quindi la polarizzabilità ed il p.e. I2 > Br2 > Cl2 > F2 solido volatile liquido gas
Legame a Idrogeno
E' una interazione specifica che si instaura tra molecole aventi un idrogeno legato ad un elemento molto elettronegativo (O, N o F) che è attratto da una coppia di elettroni solitaria di un altro atomo di N, O o F.
Hydrogen bond 8- 8+ 8+ 8+ H C H N 8+ 6 8+ 8 C H O ... 8- C Ammonia (NH3) N N H N H H 8+ 8+ H 8+ Water (H2O) O H 8+ Hydrogen bond a+ 8 C
Quando presente, il legame H è talmente forte (10% di un legame covalente) da predominare su tutti gli altri tipi di interazioni.Esso è talmente forte da sopravvivere anche nel vapore di talune sostanze. Il fluoruro di idrogeno liquido contiene linee spezzate di molecole HF e il vapore contiene brevi frammenti di catene o anelli (HF)6 Il vapore dell'acido acetico CH3COOH contiene dimeri cioè coppie di molecole legate da due legami H.
C200 100 H2O 100 Punto di ebollizione (°C) 20 HF H2Se-42 0 AsH3-55 H2Te-2 SbH3-17 -33 NH3 -61 H2S HI -35 SnH4-52 -85 HCI HBr-67 -100 -88 PH3 GeH4-88 SiH4-112 -164 CH4 -200 2 3 4 5 Periodo
La presenza del legame ad idrogeno influenza notevolmente i punti di ebollizione (p.e, ºC) di molte sostanze. Per composti analoghi questi aumentano, in genere, con il numero atomico (Z, e quindi con il numero di elettroni) a causa delle forze di van der Waals. Vedi ad esempio: CH < SiH < GeH SnHA. I p.e. di NH3, H2O e HF sono, tuttavia, fortemente fuori scala a causa dell'interazione di legame H.
Forze Repulsive
Tutte le interazioni viste finora sono attrattive. Vi sono, tuttavia, anche forze di natura repulsiva che derivano dalla repulsione nucleo-nucleo e soprattutto da quella fra le nuvole elettroniche . Tali repulsioni diventano molto importanti a distanze interatomiche corte. L'andamento dell'energia potenziale per le molecole al variare della distanza è descritta dal grafico seguente:
The non-bonding electrons repel as the atoms approach one another 1 + + As the atoms get closer the nuclei also start to repel 100 E /cm-1 Repulsive +A/r12 50 0 12 6 -50 V(r) = 4€ 012 - r r -100 Attractive -B/ r6 3.0 4.0 5.0 6.0 7.0 8.0 r/Å 0
Stato Liquido
Nei liquidi le molecole sono tenute insieme da forze attrattive dette Forze Coesive (essenzialmente di van der Waals e legami ad idrogeno) che ne impediscono la dispersione in tutto lo spazio a disposizione. L'energia potenziale associata alle forze coesive è comparabile con l'energia cinetica associata ai moti termici. Le molecole, quindi, nei liquidi sono libere di muoversi pur rimanendo a contatto con le altre.
solido liquido gas
Densità del liquido: circa 10% inferiore al solido .. caso particolare ACQUA/GHIACCIO a 0℃ dlig 7% > dighiaccio (max. d 4 ℃)
Legame a Idrogeno nel Ghiaccio
H Nel ghiaccio ogni molecola di acqua dà 4 legami ad idrogeno. Gli atomi di H e quelli di O si trovano disposti ai vertici di un tetraedro secondo una disposizione regolare. legami a idrogeno ... O-I-ONe risulta una struttura aperta per il ghiaccio che, per questo motivo, ha una densità minore dell'acqua liquida. Quando il ghiaccio si scioglie parte (ma non tutti) i legami ad idrogeno si rompono e la sua densità aumenta.
H2O ghiaccio (p = 0.92) H2O liquida (p = 1)
Tensione Superficiale
Attitudine delle molecole della superficie a farsi attrarre verso l'interno: quanto maggiore è la tensione superficiale , tanto più compatta appare la pellicola superficiale. Le molecole all'interno del liquido sentono le interazioni attrattive da parte di altre molecole in tutte le direzioni. Quelle sulla superficie sono attratte, invece, solo verso l'interno del liquido. Inoltre, è ragionevole pensare che una molecola all'interno abbia interazioni con un numero maggiore di altre molecole rispetto ad una sulla superficie.
In assenza di gravità il liquido assume una forma sferica poiché è la forma geometrica che massimizza le interazioni con la minima area superficiale rispetto al volume. La tensione superficiale (y) è l'energia richiesta per aumentare la superficie di un liquido. Ha le dimensioni di una energia per unità di superficie J/m2. Dipende dalle forze coesive e diminuisce con l'aumentare della temperatura. La tensione superficiale dell'acqua è maggiore rispetto a molti altri liquidi (legami ad idrogeno) ma è minore rispetto al mercurio (legame metallico).