Estudios morfológicos de células sanguíneas en sangre y médula ósea
Documento de Hematología Clínica sobre estudios morfológicos de células sanguíneas en sangre y médula ósea. El Pdf, un material de estudio para Universidad en Biología, describe técnicas de preparación de muestras y coloraciones, como la tinción de reticulocitos y fosfatasa alcalina granulocítica.
Ver más15 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Introducción al Estudio Morfológico Celular
El estudio morfológico de las células sanguíneas en sangre y médula ósea se realiza en la sección de citología. Permite calcular la proporción de los distintos tipos celulares normales presentes en los 2 tipos de muestras.
El estudio se lleva a cabo sobre extensiones y preparaciones realizadas a partir de muestras obtenidas directamente o anticoaguladas. Este estudio nos permite distinguir los tipos celulares presentes en una muestra con base a criterios morfológicos:
- Forma y tamaño
- Presencia o ausencia de núcleo (eritrocitos y plaquetas)
- Características nucleares.
- Características citoplasmáticas: propiedades tintoriales (si son ácidos o básicos los gránulos)
La Extensión de Sangre Periférica
Es una capa fina de sangre dispuesta sobre un portaobjetos. Está se puede obtener de 2 vías:
- Por venopunción: se debe anticoagular con EDTA.
- Por punción de la yema del dedo con una lanceta (obtenemos sangre capilar)
Técnica del Portaobjetos en Cuña
Para realizar está técnica necesitamos 2 portaobjetos de vidrio limpios. Uno de ellos se utilizará como soporte y otro como extensor:
- Depositar una gota de sangre pequeña en el portaobjeto soporte cerca de uno de los extremos.
- Colocar el portaobjetos extensor por delante de la gota en 45 grados
- deslizar el extensor hacia atrás y la gota se extendera por capilaridad a lo largo del extremo extensor
- Deslizar el portaobjetos extensor sobre el portaobjetos soporte con velocidad y presión uniforme. Tendremos así una monocapa entre 2/3 y 3/4 de la longitud del portaobjetos soporte.
- Dejar secar al aire.
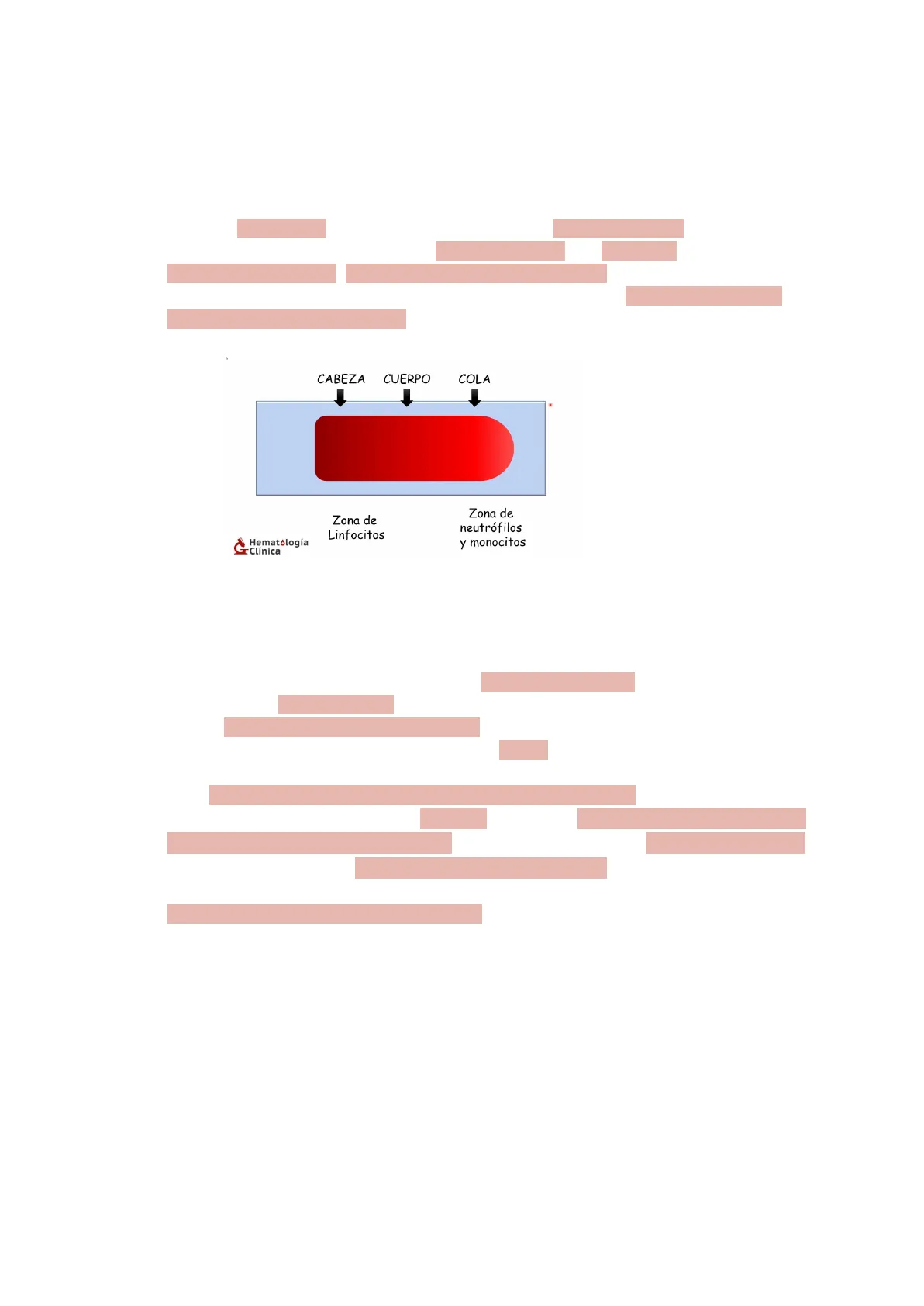
Zonas de una Extensión Sanguínea
- Cabeza: más gruesa, los hematíes pueden formar más de una capa
- Cuerpo: los hematíes se disponen en una sola capa, los leucocitos mantienen una proporción equilibrada. Zona ideal para realizar el estudio.
- Cola: los hematíes se disponen dejando huecos entre ellos. Mayor proporción de leucocitos y plaquetas grandes.
4 CABEZA CUERPO COLA Zona de Linfocitos Zona de neutrófilos y monocitos Hematología Clínica
Factores que Influyen en la Calidad de la Extensión
- Estado portaobjetos: limpios y desengrasados.
- Volumen de sangre utilizado: Una gota demasiado pequeña puede dar lugar a una extensión demasiado delgada, mientras que una gota demasiado grande puede dar lugar a una extensión demasiado gruesa.
- Anticoagulante: las mejores se hacen con EDTA.
- Distribución de la sangre por el canto del portaobjetos extensor: Si esto no se hace se obtendrían extensiones muy estrechas no valorables.
- El ángulo de deslizamiento: Un ángulo demasiado pequeño puede dar lugar a una extensión demasiado gruesa, mientras que un ángulo demasiado grande puede dar lugar a una extensión demasiado delgada.
- Velocidad de desplazamiento: debe ser una velocidad constante sino presentaría un aspecto en forma de persiana/ estrías.
- Presión ejercida: Si no es uniforme se obtendría bordes con distintas longitudes y por tanto una distribución anómala de las células.
Aparte de la técnica del portaobjeto en cuña existen otras 2 técnicas para realizar una extensión sanguínea.
La Técnica de los 2 Cubreobjetos
- Para está técnica se deposita una gota de sangre pequeña sobre un cubreobjetos limpio y desengrasado.
- Se coloca el otro cubreobjetos encima, lo que provocará la distribución homogénea de la muestra por ambos cubreobjetos.
- se hacen girar uno sobre el otro y se separan en dirección opuesta uno de otro. Se realiza de forma rápida y concisa.
Ventajas de la Técnica de los 2 Cubreobjetos
- El cubreobjetos protege el extendido de sangre de la contaminación ambiental y evita que las células sanguíneas se sequen.
- Facilita el recuento celular: la uniformidad en el espesor de la extensión simplifica el proceso del conteo.
Desventajas de la Técnica de los 2 Cubreobjetos
- Hay que tener cuidado al colocar el cubreobjetos para evitar burbujas de aire y daños en las células sanguíneas.
- Agregar un cubreobjetos puede requerir tiempo adicional en comparación con simplemente observar el extendido sin él.
- Si no se coloca correctamente, el cubreobjetos puede causar distorsión en las células sanguíneas, lo que puede dificultar la interpretación precisa de la morfología celular.
- La técnica del cubreobjetos requiere el uso de cubreobjetos y, en algunos casos, tintes específicos, lo que aumenta los costos y la necesidad de suministros adicionales.
La Técnica de la Centrifugación
Se usa una fuerza de centrifugación para producir una sola capa de células con leucocitos y plaquetas distribuidos uniformemente. Este método requiere de equipo especial y tiene el potencial de crear aerosoles que representan riesgos biológicos.
- Se coloca una muestra de sangre en un tubo de ensayo.
- Se centrifuga para separar los componentes de la sangre.
- Se toma una pequeña cantidad de la sangre de glóbulos rojos y se extiende sobre el portaobjetos.
Ventajas de la Técnica de Centrifugación
- Permite la separación rápida y eficiente de los componentes de la sangre. producen una sola capa de plaquetas y leucocitos
- El procedimiento es más sencillo y se requiere el equipo preciso.
Desventajas de la Técnica de Centrifugación
- Requiere equipo especializado y costoso.
- Puede causar daño en algunas células si se utiliza una velocidad o tiempo de centrifugación inadecuados.
- Se pueden formar aerosoles lo que conlleva riesgo biológico.
Tinciones Hematológicas para Extensiones Sanguíneas
Tinciones Convencionales
Son aquellas que se realizan para colorear las diversas estructuras de las células sanguíneas aumentando el contraste entre ellas y el medio que las rodean facilitando la identificación de los diferentes tipos de células. Estas se dividen en tinciones policromas y supravitales.
Tinciones Convencionales Policromas
Se realizan sobre células muertas y necesitan un proceso de fijación el cual facilita la adherencia de las células al portaobjetivo. Las técnicas polícromas más utilizadas en hematología derivan de las tinción de Romanowsky.
Tinción de May Grünwald-Giemsa
Esta tinción se basa en la combinación de 2 colorantes:
- El May Grünwald: es una solución de eosina y azul de metileno en metanol
que actúa como fijador.
- Azul de metileno: colorante básico que tiene afinidad por los componentes ácidos como los ácidos nucleicos que lo tiñen de azul. Las estructuras celulares que fijan colorantes básicos se llaman basófilas.
- Giemsa: mezcla de eosina y derivados de azul de metileno: azur I y azur II
- La eosina es un colorante ácido de componentes celulares básicos como la hemoglobina . Se llaman acidófilas.
Los componentes neutros se tiñen de ambos colorantes generando diferentes matices tintoriales. Las reacciones de tinción dependen del Ph. Por lo que se recomienda tamponar las soluciones acuosas.
Si la tinción está realizada correctamente las estructuras celulares se verán así:
- Eritrocitos: rosa-salmón
- Núcleos de las células: azul oscuro- violeta
- Gránulos citoplasmáticos de los leucocitos eosinófilos: rojo- anaranjado
- El área entre las células debe estar limpia y sin precipitados.
Procedimiento de Tinción May Grünwald-Giemsa
- Colocar la extensión en un puente de tinción sobre un cristalizador o un fregadero.
- Cubrir la extensión con solución de May Grünwald durante dos minutos (fijación).
- Volcar la extensión para eliminar el colorante y escurrir. Aclara con agua.
- Cubrir la extensión con solución diluida de May Grünwald durante un minuto.
- Volcar la extensión para eliminar el colorante, lavar con agua destilada y escurrir.
- Cubrir la extensión con solución diluida de Giemsa durante 20 minutos. (1/10 tampón o agua )
- Volcar la extensión para eliminar el colorante, lavar, escurrir y dejar secar al aire.
Tinción Wright
Se utiliza un solo colorante mezcla de eosina, azul de metileno y derivados de metileno metanol (fijador)
Procedimiento de Tinción Wright
Se incuba con el colorante y luego con una disolución tamponada del mismo colorante:
- Colocar la extensión en un puente de tinción sobre un cristalizador o un fregadero.
- Cubrir la extensión con colorante Wright sin diluir durante 5-8 minutos (no más tiempo que deshidrata). Este fija la extensión se inicia la tinción de las células.
- Volcar y escurrir para eliminar excedente.
- Cubrir la extensión con el colorante en un tampón de 7,2 durante 10-15 minutos.
- Volcar la extensión para eliminar el colorante con agua y dejar secar.
Tinción Panóptica Rápida
Es una combinación de las otras 2. Se utiliza mucho en laboratorios de urgencias ya que la ejecución es muy rápida. Se utilizan 3 reactivos:
- Solución fijadora: a base de metanol.
- Ácido tamponado: derivado de eosina en tampón fosfato.
- Colorante básico tamponado: derivado de azul de metileno.
Procedimiento de Tinción Panóptica Rápida
Se hace por inmersión secuencial. Por lo que hay que preparar 3 cubetas.
- Sumergir la extensión en la solución fijadora.
- Luego en la del colorante ácido tamponado.
- Finalmente en la del colorante básico.
Cada inmersión puede durar entre 5-10 segundos o meterlo en cada cubeta 5 veces.
Ventajas de la Tinción Panóptica Rápida
- No realizar lavados intermedios entre un paso y otro.
- Se puede obtener resultado en un tiempo más corto ya que es una técnica fácil y rápida. Reduce la posibilidad de cometer errores.
Desventajas de la Tinción Panóptica Rápida
- No todas las muestras son adecuadas para ticiones tópicas rápidas. (Las muestras con contengan tejidos muy densos )
- Calidad ligeramente inferior a otras tinciones.
- Menor contraste.
Las tinciones panópticas rápidas son útiles cuando se necesita un resultado rápido, pero las otras tinciones policromas ofrecen una mayor profundidad de información a costa de un tiempo y esfuerzo adicionales.
Comparación de las Tres Tinciones
Características Tinción May Grünwald- Giemsa. Tinción Wright Tinción Panóptica rápida
Fijador
Un fijador especial llamado May Grünwald Metanol Metanol derivado de Eosina.
Reactivo
2 reactivos 1 para fijar y otro para teñir Giemsa. Un solo reactivo (solución fijadora. sería el colorante (mezcla de eosina azul de metileno y derivados del azul de metileno en metanol ) 3 reactivos. 3 cubetas
- solución fijadora,
- colorante ácido
- colorante básico
Tiempo de Procedimiento
Mínimo 20 minutos 10-15 minutos 5-10 segundos
Sitio
Portaobjeto directamente. Portaobjeto directamente. Se sumerge el portaobjetos en 3