Hemoglobina normal y pigmentos anormales: estructura y metabolismo del hierro
Diapositivas de Universidad sobre Hemoglobina (normal y pigmentos anormales). El Pdf aborda la estructura de la hemoglobina, el transporte de oxígeno y el metabolismo del hierro, incluyendo la síntesis de protoporfirina, útil para estudiantes de Biología.
Ver más46 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
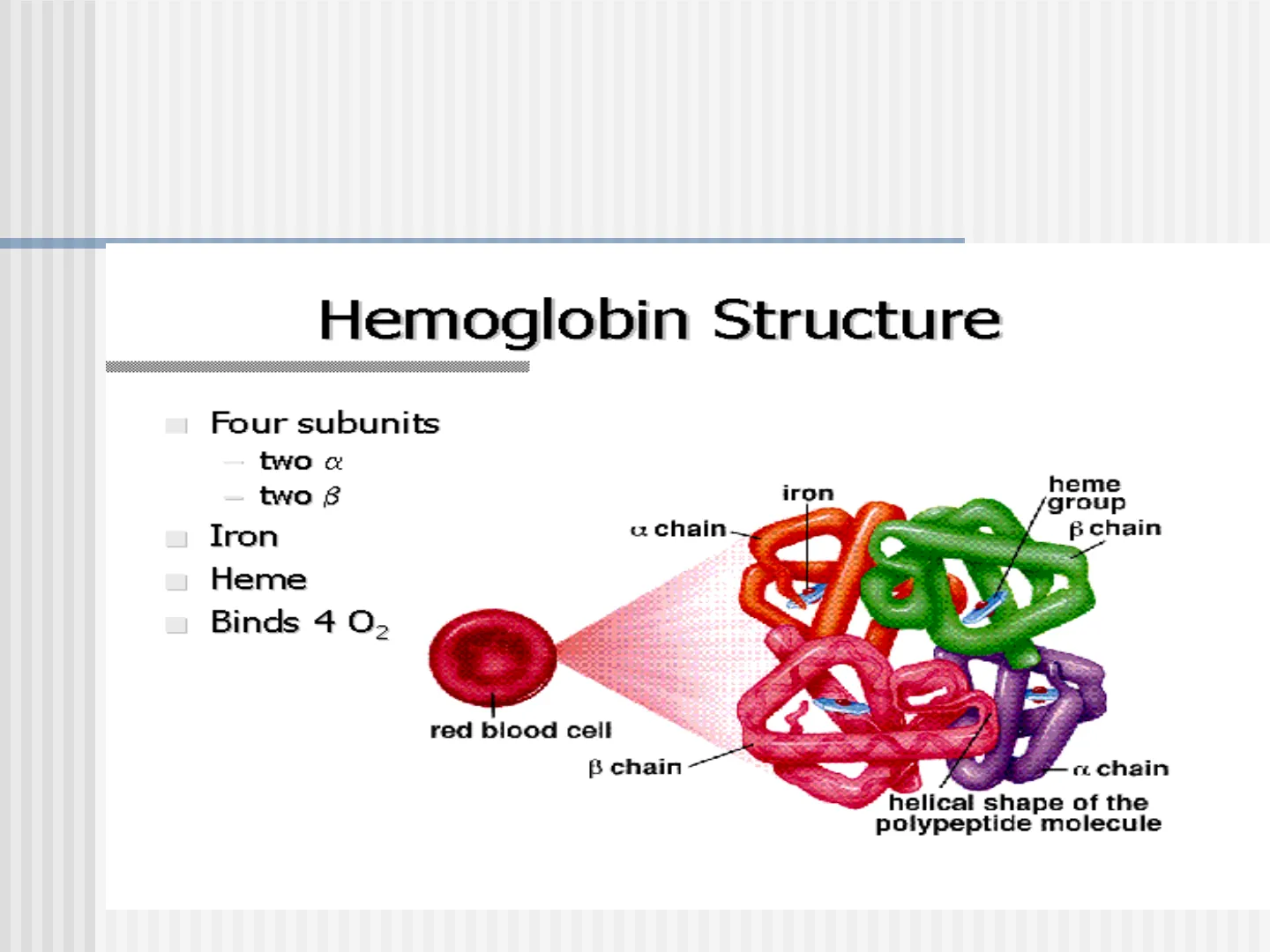
Estructura de la hemoglobina
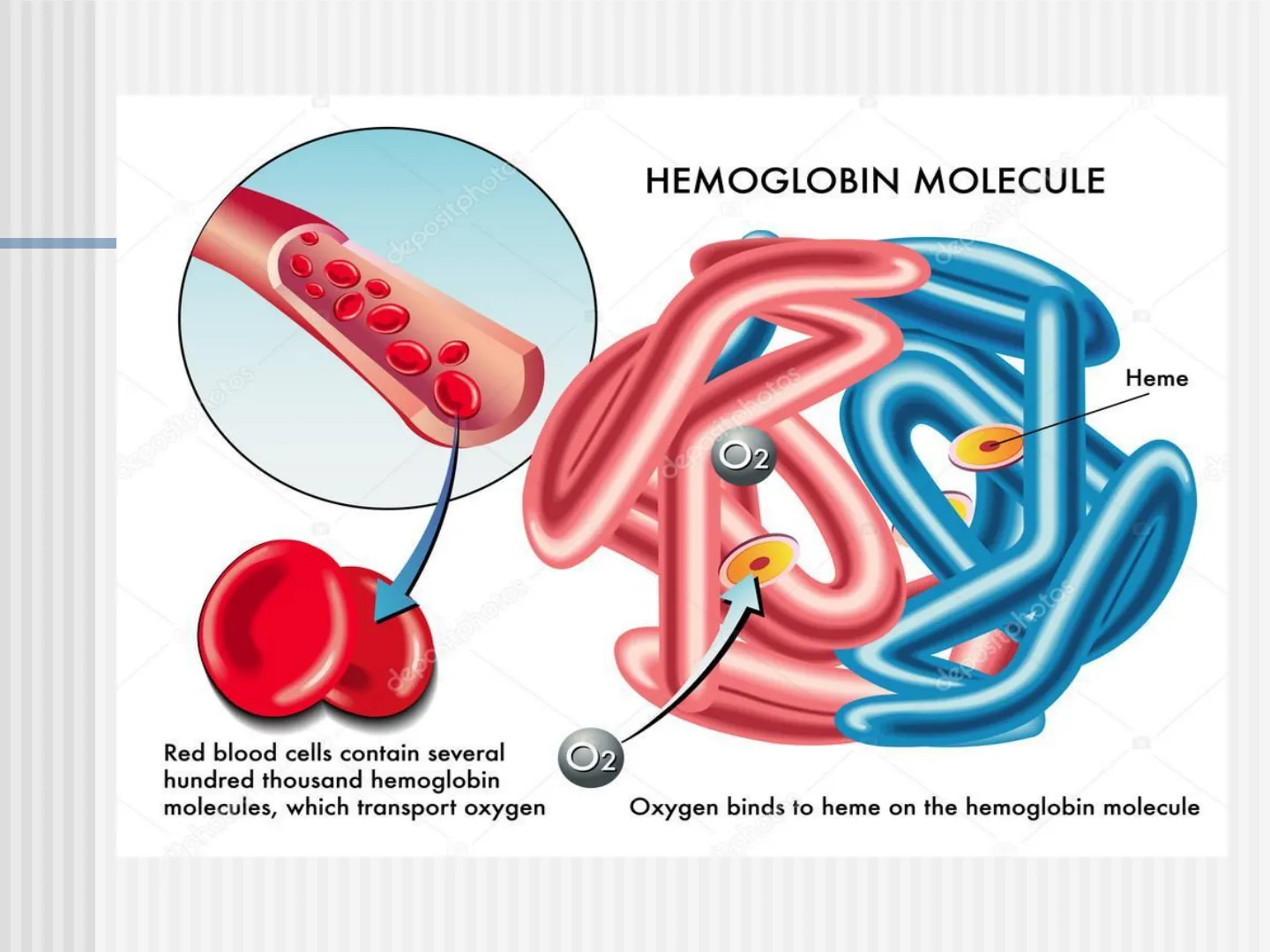
HEMOGLOBINA (normal y pigmentos anormales) Hemoglobin Structure Four subunits - two a - two 8 Iron Heme Binds 4 O2 Proteina Cuaternaria iron heme group ₿ chain a chain red blood cell B chain -n chain helical shape of the polypeptide moleculedepositphoto HEMOGLOBIN MOLECULE tos Heme otos O2 yoshiphoto Red blood cells contain several hundred thousand hemoglobin molecules, which transport oxygen O2 Oxygen binds to heme on the hemoglobin molecule
Objetivos de la hemoglobina
Objetivos Describir la estructura basica de la molécula de hemoglobina normal. ◼ Enumerar elementos requeridos para una síntesis adecuada. Explicar la funcion principal de la hemoglobina. Discutir composición normal de la hemoglobina.enlaza peption grupo amino y I-Z I-O-I 1 0=0 I-Z - I-0-6 CH3 1 Primary structure - 0 / Z-TA 0 -R 0 2 Secondary structure A I 3.000( I-2-0 C ® Z-I se pliegan 3 Tertiary structure 14 Quaternary structure Figure 2.1 Four hierarchies of protein structure. Copyright 2005 Lippincott Williams & Wilkins se empiezan a pagan SP aulcian 1 Z.I ........ 0-0-0
Componentes y estructura de la hemoglobina
Estructura · Principal componente de RBC , 90% del peso, conjugada , transporta O2 y CO2. ◼ C/ molécula de Hgb esta compuesta por una molécula de globina y cuatro moléculas o grupos heme. · Globina - dos pares diferentes de palo cadenas de polipéptidos ( 4 cadenas ) aBeta ◼ Heme - una molecula de protoporfirina IX combinada con un átomo de Fe , ferroso color CamBiaLos átomos de Fe forman enlaces coordinados, en la superficie de la molécula. El hierro es capaz de enlazar y liberar oxígeno sin producir ningún cambio en el grupo heme.
Síntesis de hemoglobina
Síntesis, depende de Suministro y transporte adecuado de hierro . Síntesis adecuada de protoporfirina. Síntesis adecuada de globina.
Suministro y transporte de hierro
Suministro y transporte de Hierro ◼ Hierro de alimentos se absorbe como ferroso en duodeno y yeyuno. Se oxida a férrico en células mucosa intestinal, almacenado como ferritina. . Cuando se necesita se libera de la ferritina mucosa y se enlaza a transferina Precursores de RBC tienen receptores para complejo transferina/hierro.Hierro es llevado al mitocondrio para sintetizar heme. Transferina es devuelta al plasma.
Síntesis de protoporfirina
Síntesis de protoporfirina ◼ Comienza en mitocondrio Succ CoA+glicina/enz delta ALA sintetaza yvit. B6 · Citoplasma - condensación de 2 moléculas = porfo 4 porfo =uro ◼ Uro es decarbox=copro ◼ Etapas finales ocurren en mitoc donde se convierte en protoporfirina Se incorpora el hierro =heme
Síntesis de globina
Síntesis de globina Ocurre en citoplasma de NRBC y retic Cadenas de polipeptidos se manufacturan en ribosoma -enz-RNA polimerasa Sintetizadas son liberadas al citoplasma Cadenas alpha y beta forman dimeros a las cuales dos moléculas HEME se unen · Dos de estos dimeros forman un tetramero y asume estructura tridimensional.
Función de la hemoglobina
Función Union reversible con 02 y el transporte de este de los pulmones al tejido. Efecto: mol de O facilita la entrada de los otros O Interacción heme-heme. Afinidad por oxígeno -curva de disociación de Hgb- sigmoidal La afinidad por O depende de: pH,T ,CO2 y 2,3-DPG. por glicolisis◼ (aumento en T y/o 2,3-DPG o disminución en pH o aumento en CO2 (adictosvocariavoca_disminución en afinidad y lo libera 7 acidosis provoca Oxygen-Hemoglobin Dissociation Curve Oxygen Saturation of Hemoglobin (%) Left-Shift Increased affinity for O2 Į pCO2 [H+] 1 2,3-DPG Į Temp HbF Right-Shift Decreased affinity for O2 1 pCO2 1 [H+] (ĮpH) 1 2,3-DPG 1 Temp Lineage @ Oxygen Partial Pressure (mm Hg) Moises Dominguez2,3-DPG se enlaza ◼ causa disminución de afinidad y libera el O al tejido. Shift/ left - afinidad ◼ por O2 aumenta, no lo libera. ◼ Shift/right- disminuye afinidad por O2, lo libera (aum en T, 2,3-DPG o disminución en pH o aumento en CO2. Figure 1. Hemoglobin-oxygen dissociation curve % Saturation 100 180 Left shifted. Right shifted 60 Normal 40 20 0 0 10 20 30 40 50 60 70 80 90 100 Partial pressure O2, mm Hg
Propiedades del pigmento respiratorio
Propiedades del pigmento respiratorio Capacidad de transportar gran cantidad de oxígeno Gran solubilidad pulmón Capacidad de "captar" y "ceder " oxígeno a presiones determinadas Capacidad de amortiguar una solución de bicarbonato Buffer
Hemoglobinas normales
Hemoglobinas normales Tres tipos distintos de Hgb " Hgb A - predominante en adulto normal. 90-95% ◼ Cadenas de polipéptidos - dos cadenas alfa y dos cadenas beta. ◼ Síntesis ocurre durante desarrollo fetal, de forma lenta. Producción aumenta en semanas que preceden al nacimiento. · Al nacer - 40 % Hgb A. elresto es FHgb F- predominante en feto y NB. Cadenas de polipéptidos - dos cadenas alfa y dos cadenas gamma.protr Existen dos tipos de cadena gamma- difieren entre si por 1 aa en 136. alanina o glicina. Al nacer - 60-80%. Gradualmente es sustituida por A.Hgb A2 - adulto normal 1.5-3.5% Cadenas de polipeptidos - dos cadenas alfa y dos cadenas delta. Síntesis comienza tarde en la vida fetal. Niveles aumentan gradualmente durante el 1 er año.
Composición de cadenas de hemoglobina
Composición de cadenas Hemoglobin Type Symbol Globin chains Embrionic : -Gower-1 32 €2 2 zeta 2 epsilon - Gower-2 a2₴2 2 alpha 2 epsilon - Portland-1 32 y2 2 zeta 2 gamma Hemoglobin F a2y2 2 alpha 2 gamma Hemoglobina A a2B2 2 alpha 2 beta Hemoglobin A2 262 2 alpha 2 delta
Genes envueltos en la síntesis de hemoglobina
Chromosome 16 Q 2 5' 3' Chromosome 11 E GY AY 8 ß EmBranico Birth Q B Globin Chain Synthesis E y 8 10 20 30 10 20 30 40 Weeks <2€2 - Gower 1 S2 Y2 - Portland Q2 €2 - Gower 2 Q2 Y2 - Hb F a2 B2 - Hb A CX2 82 - Hb A2 Figure 1 Globin Chain SynthesisGenes envueltos Hemoglobin Synthesis si no tiene una de las cadenas RIP . 5 0-1 Chromosome 16 (a - genes) Y Y 8 B Chromosome 11 (8 - genes)La secuencia de proteinas esta codificada en el cromosoma 11 para la produccion de cadenas beta, delta y gamma. La secuencias de proteinas para las cadenas alpha en el cromosoma 16
Electroforesis de hemoglobina
Electroforesis de Hgb Hemoglobin Electrophoresis Regularmente Básica : Cellulose Acetate, pH 8.5 Pata confirmar medio soporte Ácido Citrate Agar, pH 6.0 Control groups groups HemoglobinaC con SU balda aminolada Sichle Fetal Adulto 1 falda F amindadaA S SU con C pueden migrar por eso se hace este
Hemoglobinas embriónicas
Hemoglobinas embriónicas Durante los primeros tres meses despues de la concepción, Detononica produce HI lbg 'S. Portland, Gower I, Gower II Estas Hab's son sustituidas por HgbF
Variantes de hemoglobina normal
Variantes de Hgb normal Son Hgb normales en composición pero que son incapaces de transportar y entregar O2 a los tejidos. Pigmentos Se incluyen : Jama Carboxihemoglobina. methemoglobina sulfhemoglobina. y enlaza O En estos derivados la porción heme esta alterada en cierta forma pero no la porción de globina.
Carboxihemoglobina
Carboxihemoglobina " Hgb tiene capacidad de combinarse con CO. monoxido I Afinidad por CO es 210 veces mayor. ◼ Carboxihemoglobina es estable. ◼ Inutiliza la molécula para transportar O2. eptemBle Disociación es 10,000 veces más lenta Si saturada 40% con CO - muerte rápida Sangre - cherry red. parece ser arterial silenciosaBlocks Oxygen Transport to Tissues AIR 1 1 O2 O2 Heart 020 0202 Hb 0202 Hb 0202 Hb 02 0202 1,02 8202 Hb 202 0202_020 Hb Hb Hb Hb 02 02 O2 02 O202 0202 0202 Muscle AIR + CO Blood Circulation co CO 1 O2 co.co Co Hb 0202 0202 H6 o. do Hb C0202 Hb Hb 0202 a co & coº O2CO o, CO 0202 0, CO Muscle Camara hiper Bonica: para tratamiento c. D. G. Penney, 1997 O2 Heart 0202 Có Co C 2COCO 0202 Hb Hb 0202 Hb o. co COCOb Lungs Hb 9886 0202 70 Hb Hb Hb Hb 0202 02 02 O2 Lungs O202 Hb 0202 0202 0202 HD HD 01 02 нь 0202 02 O2 O2
Methemoglobina
Methemoglobina Fota Fe + 3 ◼ Hierro ferroso es oxidado a férrico. Incapacitada para enlazar O Puede ser heredada o adquirida, por envenenamiento con químicos o drogas. 10 % o mas de methemoglobina - cianosis ciente falta de O azul 60 % o mas hipoxia falta de 0 -Pigmento Brown
Sulfhemoglobina
Sulfhemoglobina ◼ Enlaze estable con sulfuro formándose un derivado verdoso. Formación por efectos tóxicos de drogas oxidantes como phenatecin,sulfonamidas o bacteremia por Clostridium welchii. Hemoglobina precipitada ◼ Puede precipitarse en forma de Heinz bodies. ◼ Sulhemoglobina es estable e irreversible y se mantiene en RBC hasta que completa su ciclo de vida. ◼ Si se combina con CO= carboxisulfhemoglobin. Se mueve
Métodos de variantes de hemoglobina
Métodos de variantes Espectofotométricos Colorimetricos Gasométricos
Métodos de hemoglobina
Métodos de Hemoglobina Método de gravedad específica- sulfato de cobre, razón de peso de un volumen de sangre en relación a un volumen igual de agua a 4ºC. Se uitlizan diferentes soluciones de distintas gravedades específicas. Es un método de screening. Se utiliza en banco de sangre. estimado
Método gasométrico
Cont. Métodos hemoglobinaMétodo gasométrico Se puede medir 02 y/o CO2 mado 482 Se basa en que la Hbg enlaza una cantidad fija de O ( 1 gramo de Hgb se combina con 1.34 ml de O2). La sangre se hemoliza con saponina y el O liberado es colectado en aparato Van Slyke. Vol 02/100ml/1.34 = gramos Hgb/100ml Desventaja inactivas. - poca precision,no mide Hgb
Métodos químicos de hemoglobina
Métodos químicos Se basa en que la Hgb tiene una cantidad fija de hierro (aprox.34%) y en que en 1 gramo hay 3.47mg de hierro. " Wong - hierro es liberado, las proteínas son hierro es determinado colorimetricamente y el valor de Hgb se calcula. io. precipitadas con acido tungstico. El Fórmula mg Fe/100 ml/3.47=gramos de Hgb /100 ml ximacions
Métodos colorimétricos de hemoglobina
Métodos colorimétricos Direct matching - el color de la sangre se compara con stds. " A) Tallquist - escala graduada 10 a 100%. Se compara gota de sangre con papel absorbente con la escala de colores. ◼ B) Dare - usa dos placas de cristal. ◼ C) Spencer - transmision de luz atraves de una capa fina de sangre hemolizada a una profundidad constante.◼ Método de hematina ácida - Sahli-Hellige. Sangre se mezcla con HCl diluído, se hemolizan los rbc y convierte la Hgb a una solución marrón de hematina ácida. Solución se compara con standares. Método de hematina alcalina - sangre se mezcla ◼ con solución diluída de hematina alcalina, se calienta. La Hgb es convertida a una solución verde-azul he hematina alcalina. Color se compara con standares. Método no bueno para Hgb fetal ( resistente).más importante
Método de cianmetahemoglobina
Cyanmethemoglobin Method Principle · Blood is mixed with Drab kins solution. Drabkins solution -pH 7.0 -7.4 Potassium ferricyanide Potassium cyanide Potassium dihydrogen phosphate Non-ionic detergent Distilled water . Erythrocytes are lysed producing an evenly distributed Hb solution. . Potassium ferricyanide converts Hb to methemoglobin. . Methemoglobin combines with potassium cyanide to form cyanmethemoglobin. . All Hbs present in blood are converted to this form. . Absorbance is measured in spectrophotometer at 540 nm . To obtain amount of unknown Hb sample, its absorbance is compared with the standard cyanmethemoglobin solution