Trascrizione delle lezioni di Pifferi sulla membrana plasmatica
Documento di Biologia sulla trascrizione delle lezioni di Pifferi. Il Pdf esplora la struttura della membrana plasmatica, i meccanismi di trasporto e il potenziale di membrana, con un focus sugli esperimenti FRAP e le fasi della refrattarietà, utile per studenti universitari.
Ver más53 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Membrana plasmatica
La mebrana plasmatica è costruita da un doppio strato lipidico, questa organizzazione a doppio strato è dovuta al fatto che questa disposizione è quella più energeticamente favorevole nell'organizzare lipidi in un'ambiente acquoso. Questo doppio strato lipidico crea una barriera idrofobica. Impermeabile a trasporto, risolto dalle proteine.
Lipidi di membrana
I lipidi di membrana: la classe più importante: glicerolipidi, con una struttura di glicerolo esterificato, legato a un fosfato legato a un gruppo di testa: colina o etanolammina (positive) o serine, glucosio, glicerolo, inositolo (negative). L'inositolo è un poliolo ciciclo (6C, con 6 gruppi OH) che possono esere esterificati con fosfato. La posizione del fosfato è importante: diversi tipi di membrana presentano fosfolipidi con inositolo fosforilato in posizione diversa. E.g. le membrane del Golgi: fosfatidilinositolo-4P, quella plasmatico il 4,5-bisfosfato. Questa viene idrolizzata e viene usata come molecola di segnale. I glicerolipidi si distinguono non solo in base alla testa, ma anche in base dei acidi grassi che esterificano il glicerolo. Questo è importante perche membrane di organi diversi, hanno tassi di acidi grassi diversi. Nel cervello quello più diffuso è l'acido stearico, nel cuore è in minorità e prevale altro. Questa differenza da proprietà meccaniche diverse. La ridigidità e risposta ai stimoli meccanici sono importante, e.g cardiomiociti vs neuroni che stanno protetti. In situazioni patologiche: il tumore cresce dove puo. Con membrane rigide, avrà più difficoltà iniziale di proliferarsi. L'altra grande classe di lipidi di membrana sono i sfingolipidi, più abbondante la sfingomielina. Infine l'ultimo lipide delle memrbane plasmatiche è il colesterolo, lipide particolare con una parta carboniosa rigida e una piccola cosa idrofobica e solo 1 -OH idrofilo. La parte rigida conferisce ridigità alle membrane.
Proteine di membrana
L'altra componente della membrana sono le proteine: integrali e periferiche. Integrali vuole dire che attraversano completamente la membrana, quindi è impossibile distaccarle senza distrugerre la membrana, le periferiche sono distaccabili.
Mosaico fluido
Mosaico fluido: ipotesi che le proteine e i lipidi nella memrbana si possono muovere liberamente all'interno di essa. Questi movimenti non sono tutti favoriti energeticamente. Per esempio la flessione degli acidi grassi avviene spesso, la rotazione del fosfolipide e molto frequente, stessa cosa per la diffusione laterale (movimento lungo l'asse della membrana). Il flip-flop il trasferimento di un lipide o proteine avviene con frequenza bassisima. In alcune vie di segnale questo viene velocizzato. I lipidi di membrana non sono disposti in maniera simmetrica nei due foglietti, ma in modo asimmetrica. Normalmente, la fosfatidil-serinasi trova abbondantemente solo nel foglietto interno, il contrario per la fosfatidil-colina. Esistono una serie di proteine che traslocano da un foglietto all'altro. Queste proteine utilizzano energia, perche questo movimento è sfavorito energeticamente. Viene da l'idrolizzazione di ATP. Quindi esistono proteine flippasi che mediano l'importo di fosfolipidi che normalmente si trovan all'esterno. Nella direzione opposto esistono le floppasi che traslocano lipidi dal foglietto interno all'esterno. Un'altra classe di proteine importante media questo processo senza utilizzo di energia, usa il 1gradiente di concentrazione dei fosfolipidi. Quindi la fosfatidilserina dall'interno all'esterno. Questo è meccanismo di segnale, per cellule che vanno incontro ad apoptosi, che veranno rimosse da macrofagi attraverso la presenza annomale del fosfatidilserina sull'esterno della membrana. Un'altro meccanismo importante che è mediato dall'esternalizzazione della fosfatidilserina è l'emostasi. Le varie vie di controllo di emostasi convergono sull'esternalizzazione della fosfatidilserina. La patologia associata: La esternalizzazione della fosfatidilserina non efficiente porta ad un'alterazzione dell'accumulo del sangue.
Esperimento FRAP
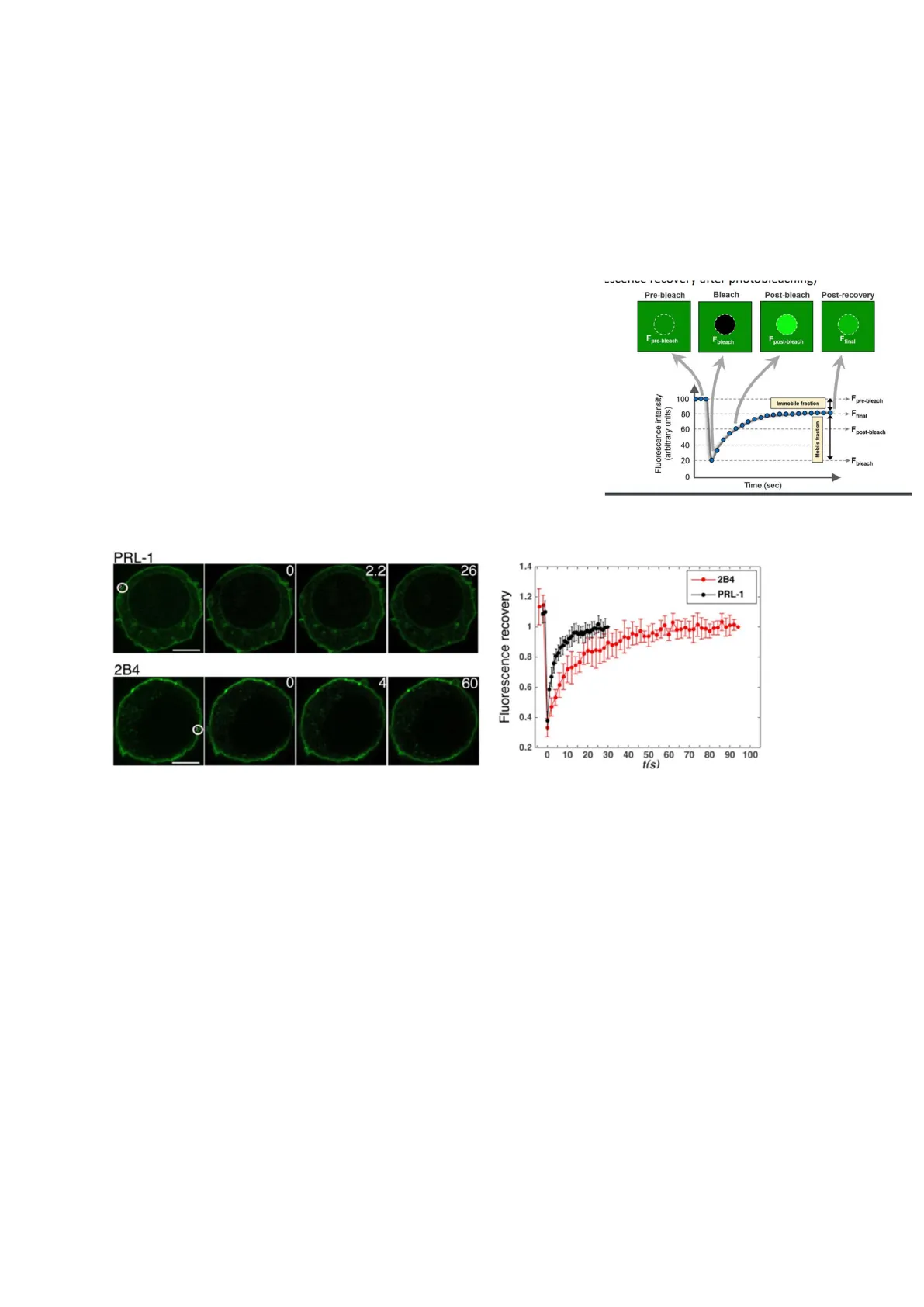
FRAP: Come dimostrare che anche le proteine si possono muovere, che quindi sono fluide: esperimento FRAP (fluorescence recovery after photobleaching). Si marca con una molecola fluorescente una proteina. Quando la illumino con una lunghezza d'onda, la proteina ne emette un'altra. A un certo punto si usa una luce molto interna, per bleachare, distruggere tutto il colorante in una data regione. Poi si aspetta, quello che si osserva è che lo spot nero torna ad essere fluorescente. Perche le proteine dalle zone non-bleachate si muovono per colonizzare di nuovo la zona bleachata. (fig. 1)
Pre-bleach Bleach Post-bleach Post-recovery Fpre-bleach Fbleach F post-bleach F final 100 Fpre-bleach Immobile fraction 80 . Frina 60 Fpost-bleach 40 Mobile fraction 20 Fbleach 0 Time (sec) Figure 1: FRAP
PRL-1 0 2.2 26 1.4 -2B4 ·PRL-1 1.2 HT 1 2B4 0 4 60 0.6 0.4 0.2 0 10 20 30 40 50 60 70 80 90 100 t(s) Figure 2: esperimento usando FRAP
Nel cerchietto è stato fatto il bleaching, ha distrutto tutto il colorato(fig. 2). Poi è stata misurata la fluorescenza in intervalli di tempo e messi in un grafico. Simile allo schema, però le due proteine 2b4 e PRL-1 si muovono con velocità diversa. Quindi le proteine si muovono, ma non tutte nella stessa maniera.
Movimento delle proteine
Il movimento delle proteine è permesso, ma è regolato. Ci sono 4 categorie:
- Proteina da movimento random
- Proteina con movimento confinato, si muove in un raggio limitato
- Proteina che si muove a tratti, movimenti in una zona e poi riesce a spostarsi in un'altra zona dove rimane confinata
- Proteina con movimento diretto, definito. Si muove nel modo quasi piu veloce da A a B. Questo è importante perche se pensiamo a un recettore per un ormone, se è un recettore che si puo muovere in una cellula polarizzata e l'ormone passa solo da un lato. Se un recettore si muove o no, dipende se la cellula può rispondere o meno all'ormone.
2 In un esperimento: Fluorescence intensity (arbitrary units) Fluorescence recovery 0.8Il modello realistico di membrana: Le proteine di membrana si dividono in integrali e periferiche. Gran parte delle integrali sono transmembrana. A cosa servono le proteine di membrana? Rilevano la presenza di molecole, sono i recettori. E servono per trasporto transmembrana. Un modello realistico di come è fatta una membrana plasmatica, non è l'originale di Singer-Nicholson.
Modello realistico di membrana
La differenza tra il modello originario e realistico è la densità di proteine. In quello originale le proteine galleggiavano e le proteine erano pensate come avere una dimensione paragonabile a quella dei fosfolipidi. La dimensione dei domini proteici invece è piu grande dei fosfolipidi, e non sono simmetriche. E.g. l'ATP-sintetasi ha un mega-dominio che guarda la matrice del mitocondrio e un piccolo dominio transmembrana. Il peso relativo a quello dei fosfolipidi crea un'alterazione della struttura del fosfolipidi, perche sono costretti ad assumere forme strani per fare spazio alle proteine giganti. Tutto ciò è rilevante perche altera le proprietà meccaniche della membrana.
Curvatura della membrana
Un'altro aspetto che era non c'è nel modello originale è la curvatura. Mediamente le cellule hanno forma con zone curvate. Come fa a curvarsi? Ci sono 2 meccanismi che la regolano:
- La posizione dei fosfolipidi e la percentuale diversa dei fosfolipidi con forme diverse. I fosfolipidi possono avere diversa forma a seconda del rapporto tra testa e corpo. Se la testa è relativamente piccola abbiamo fosfolipidi cilindrici e una membrana piana. Se ci sono fosfolipidi con testa relativamente piccola, otteniamo un fosfolipide conico e una membrana con curvatura negativa. Se al contrario abbiamo fosfolipidi con una testa grande abbiamo un cono invertito, con tanti insieme otteniamo una curvatura positiva e diventerà una sfera.
- Presenza di proteine che interagendo che interagendo con la membrana la curvano. Una di questa sono le BAR proteins. Tutto cio è importante in se ma anche perche i fenomeni di curvatura sono molto importanti in divisione cellulare, quando va incontro alla mitosi. Quindi il controllo della curvatura è importante per il controllo di divisione cellulare. Quindi BAR proteins sono mutate in molti tipi di tumore, perche la divisione cellulare viene più favorita perche le modifiche strutturali vengono favorite da queste varianti proteiche.
Meccanismi di trasporto di sostanze
Se immaginiamo di avere uno spazio diviso in 2 compartimenti da una superficie dimensioni S. Flusso molare unidirezionale- numero di particelle(n) che passa area(S) nell'unità di tempo(dt). n essendo espresso in mole: numero di particelle(n)/ numero di avogrado(N)= numero di particelle in mole. (eq. 1)
f1-2; N * A * At n flusso molare unidirezionale letto equation 1 equation 2
Flusso molare netto: dato da quanto passo veramente, faccendo la sottrazione di quanto passa da 2 a 1 da quanto passa da 1 a 2. (eq. 2)
3In generale, la forza che spinge un soluto una molecola, a muoversi è data da una costante(K) moltiplicata da X(driving force) che è la forza che spinge la molecola, l'equazione di Teorell. (eq. 3)
Fi = Ki * Xi Xi Driving Force Equazione di Teorell equation 3
Questa è una generalizzazione della legge di Ohm. La corrente (numero di elettroni/tempo), il potenziale spinge gli elettroni, la costante è resistenza R. 1/R è conduttanza (G). (eq. 4)
I = * AV DRIVING FORCE > CONCRETIZ; DIFOSONE Legge di Ohm DONE : MASSE FLUSSO equation 4 ELETTRICO: ELETTROFORESI
Queste driving force possono essere di diversa natura. Se abbiamo in gradiente di pressione, si genera un flusso di massa. Se abbiamo un gradiente di concentrazione si genera il flusso chiamato diffusione. Se abbiamo una differenza di potenziale elettrico, il movimento è una migrazione in campo elettrico, o elettroforesi.
Flusso di massa
Flusso di massa(Fm): Fm= K x (P1-P2)(eq. 6) P1-P2= gradiente di pressione(P) K= data dalla legge di Poiseuille, che vedremo nel sistema cardiovascolare. Il sangue non scorre nel sistema cardiovascolare non è perche deve deve portare nutrienti ma è perche segue un gradiente di pressione. Il sangue si muove dall'atrio dx e ritorna all'atrio dx: nelle arterie c'è una pressione alta, nelle vene cave la pressione è molto piu bassa. Visto che il sistema è chiuso, il sangue fa questo giro. (eq. 5)
ATTr4 Bnl equation 5
Fm = Km * (P1 - P2) = Km * AP equation 6
Diffusione
Diffusione: la driving force è un gradiente di concentrazione. Le molecole si spostano da una zona dove sono piu concentrate a dove sono meno concentrate. Quando aggiungiamo una goccia di colorante in un compartimento, vediamo come nel tempo si andrà a diffondere in tutto il becher. In due becher con temperature diverse vediamo come la diffusione avviene più velocemente nella soluzione con la temperatura piu alta. La diffusione è determinata dalla legge di Fick, che è la legge generale traslata alla diffusione.(eq. 7) Il flusso è determinato da il coefficiente di diffusione moltiplicato per il negativo gradiente di concentrazione 4