Tema 9: Mezclas y su clasificación en química para Bachillerato
Documento de Química sobre el Tema 9: Mezclas. El Pdf explora la clasificación de mezclas en homogéneas y heterogéneas, soluciones, coloides y métodos de separación. Este material de Bachillerato es útil para comprender los conceptos fundamentales de las mezclas.
Ver más8 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Tema 9: Mezclas
2º ESO (FQ)
1. LAS MEZCLAS Y SU CLASIFICACIÓN
Una MEZCLA es una combinación de dos o más sustancias puras. De manera general, para preparar una mezcla:
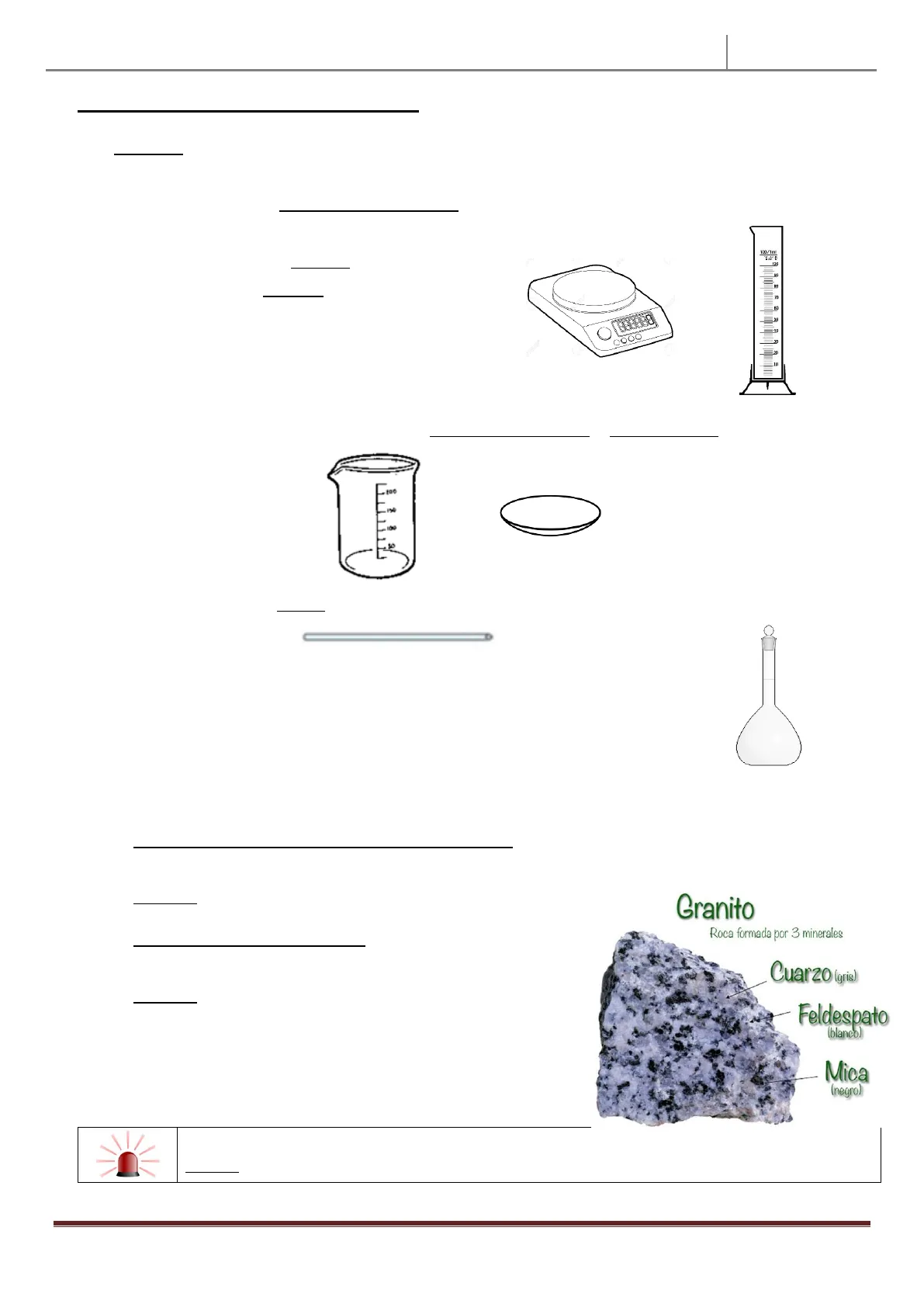
1º) Medimos la cantidad de cada sustancia pura que vamos a utilizar con una báscula (si necesitamos su masa) o con una probeta (si necesitamos su volumen).
120/1n 888888 0000
2º) Introducimos las sustancias puras en un vaso de precipitados o vidrio de reloj.
ட் .100 -30
3º) Removemos con una varilla.
4º) Introducimos la mezcla en un matraz aforado y cerramos con un tapón.
Las mezclas pueden clasificarse en:
MEZCLAS HOMOGÉNEAS O DISOLUCIONES: Aquellas en las que no se distinguen sus componentes a simple vista. Ejemplo: agua+sal
MEZCLAS HETEROGENEAS: Aquellas en las que se distinguen sus componentes a simple vista. Ejemplo: agua+aceite o granito
Granito Roca formada por 3 minerales Cuarzo (gris) Feldespato (blanco) Mica (negro)
DEBERES (en gris los voluntarios): Pág 65 -> 3.
M. H . M. 2Tema 9 .- Mezclas 2º ESO (FQ)
2. DISOLUCIONES
Las DISOLUCIONES son mezclas homogéneas. Mezclas porque se combinan sustancias puras y homogéneas porque NO se distinguen sus componentes a simple vista.
TIC 1 .- Visualiza El siguiente video y contesta a las preguntas. https://www.youtube.com/watch?v=3fOeGGfpiy8
a) ¿Qué sustancia pura hay en el vaso de precipitados al comienzo del experimento? Escribe nombre y fórmula. b) ¿Cuál es la fórmula y el nombre de la sal? c) ¿Cómo se llama un átomo que gana o pierde electrones? d) ¿Cómo se llama un ion que ha ganado electrones? ¿ Cómo queda cargado? e) ¿Cómo se llama un ion que ha perdido electrones? ¿ Cómo queda cargado? f) ¿Quiénes son los aniones de la sal? g) ¿Quiénes son los cationes de la sal? h) La molécula de agua, ¿tiene un polo positivo y otro negativo? Dibuja una molécula de agua representando cada uno de los polos. i) Cuando hablamos de una DISOLUCIÓN DE CLORURO DE SODIO, ¿a qué nos referimos? j) Haz un dibujo que represente una disolución de cloruro de sodio k) Una disolución de cloruro de sodio, ¿conduce la electricidad? Justifica tu respuesta.
2.1. Soluto y disolvente
Cundo una sustancia se disuelve en otra, se produce la separación y posterior dispersión de las partículas de uno de los componentes en el otro.
Existen dos tipos de componentes en una DISOLUCIÓN (D):
DISOLVENTE (d): Aquel en mayor proporción. El agua es el disolvente universal. El estado de una disolución (sólido, líquido o gas) siempre coincide con el del disolvente.
SOLUTO (s): Aquel en menor proporción. Una disolución puede tener uno o varios solutos, pero sólo un único disolvente. El/los soluto/s siempre se dispersa/n en el disolvente de tal forma que al removerlos dejan de distinguirse a simple vista.
En forma simbólica podemos representar una disolución como: soluto + disolvente = Disolución s + d = D
M . H . M. 3Tema 9 .- Mezclas 2º ESO (FQ)
Algunos ejemplos de disoluciones son:
| s (estado) | d (estado) | D (estado) | Ejemplo |
|---|---|---|---|
| S | S | S | Aleaciones (M+M) >Ej .: Sn+Cu = Bronce |
| L | S | S | Amalgamas (Hg+Metal) |
| G | S | S | H2 adsorbido en Pd |
| S | L | L | Suero fisiológico (sales minerales + agua) |
| L | L | L | Alcohol+agua |
| G | L | L | Coca-Cola (azucares + CO2 + ... + agua) |
| S | G | G | Humo (partículas sólidas producto de la combustion+ aire) |
| L | G | G | Niebla ( gotitas agua+ aire) |
| G | G | G | Aire (O2+ CO2 + ... + N2) |
DEBERES (en gris los voluntarios): Pág 66 -> 7; Pág 68 > 10.
2.2. Propiedades de las disoluciones
1 .- La masa de la disolución será igual a la masa del soluto más la masa del disolvente. m(D)=m(s)+m(d)
2 .- El volumen de la disolución no siempre es igual a la suma del volumen del soluto más el volumen del disolvente. Sólo en el caso en que se cumpla decimos que los volúmenes son aditivos.
Si los volúmenes son aditivos-> v(D)= v(s)+ v(d)
TAC 1 .- Teniendo en cuenta que el suero fisiológico se prepara disolviendo 3 g de sal en 330 g de agua, completa la siguiente tabla:
| soluto/s ( .. .... ) | disolvente ( .. ) | Disolución ( .................................. ) |
|---|---|---|
| masa (unidades) |
TAC 2 .- Teniendo en cuenta que para preparar un desinfectante mezclamos 400 ml de agua destilada con 200 mL de alcohol etílico y 10 mL de alcohol bencílico, completa la siguiente tabla. Supon volúmenes aditivos.
| soluto/s | disolvente ) | Disolución ( ... |
|---|---|---|
| (. | ( .. ............. ) | ) |
| volumen (unidades) |
M . H . M. 4
Tema 9 .- Mezclas 2º ESO (FQ)
TAC 3 .- Si preparamos 300 mL de una disolución mezclando 78,9 g de alcohol etílico y 200 g de agua, completa la siguiente tabla. Supón volúmenes aditivos.
Dato: densidad del agua d(agua)= 1 g/mL
| soluto/s ( .. ) | disolvente .) | Disolución ) |
|---|---|---|
| ( | ( | |
| masa (unidades) | ||
| volumen (unidades) |
TAC 4 .- Queremos preparar una disolución de 20 g de bicarbonato sódico, 5 dg de hidróxido de sodio y 8000 cg de agua:
a) Explica cómo prepararías la disolución indicando que instrumentos de laboratrio utilizarías en cada paso b) Completa la siguiente tabla:
| soluto/s (. .) | disolvente (. ................... .) | Disolución (. ) |
|---|---|---|
| masa (unidades) |
TAC 5 .- El bronce fue la primera aleación importante obtenida por el hombre y da su nombre a la «Edad del Bronce». Durante milenios fue la aleación básica para la fabricación de armas y utensilios, joyas, medallas, esculturas y monedas. Hoy en día se utiliza para fabricar instrumentos como campanas, gongs o saxofones, y en la fabricación de cuerdas de arpas, guitarras y pianos.
Para obtenerlo se necesita cobre y estaño fundido. Si se desea preparar una muestra de 5 L de bronce fundido y se dispone de cobre y 400 mL de estaño, completa la siguiente tabla suponiendo volúmenes aditivos.
| soluto/s | disolvente .... | Disolución (. .) |
|---|---|---|
| ) | ( | ) |
| volumen (unidades) |
M . H . M. 5Tema 9 .- Mezclas 2º ESO (FQ)
3. COLOIDES
Las COLOIDES son sistemas materiales que a simple vista parecen homogéneos, pero que al observarse con un microscopio se aprecia que son heterogéneos.
Ejemplo COLOIDE
| Soluto | Disolvente | |
|---|---|---|
| Vidrio | S | S |
| Queso | L | S |
| Nubes de golosina | G | S |
| Gelatina | S | L |
| Leche | L | L |
| Espuma cerveza | G | L |
| Aerosol Covid en aire | S | G |
| Aerosol spray | L | G |
No es necesario usar un microscopio para comprobar que ciertos sistemas aparentemente homogéneos, realmente son coloides. Basta observar si se produce el EFECTO TYNDALL, un fenómeno físico que sucede en sistemas materiales con partículas en suspensión que dispersan la luz:
DISOLUCIÓN (NO se produce el efecto Tyndall)
COLOIDE (Se produce el EFECTO TYNDALL)
DEBERES (en gris los voluntarios): Pág 78 -> 1, 2.
M. H . M. 6Tema 9 .- Mezclas 2º ESO (FQ)
4. MÉTODOS DE SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA
Tal y como hemos aprendido en el tema anterior y en este, podemos escribir las SUSTANCIAS PURAS y las MEZCLAS como:
ÁTOMO + ÁTOMO SUSTANCIA PURA
SUSTANCIA PURA + SUSTANCIA PURA MEZCLA
Pues bien es posible separar los átomos que componen una sustancia pura y las sustancias puras que componen una mezcla:
- Los elementos de las sustancias puras pueden separarse por procedimientos químicos. Aprenderemos cómo en el tema siguiente (REACCINES QUÍMICAS)
- Los componentes de cualquier mezcla pueden separarse por procedimientos físicos. En esta apartado aprenderemos algunos métodos físicos para separar las sustancias puras de una mezcla.
4.1. Separación de sustancias puras en mezclas heterogéneas
Los métodos más usados para separar sustancias puras en mezclas heterogéneas son:
A) FILTRACIÓN B) DECANTACIÓN C) CENTRIFUGACIÓN D) SEPARACIÓN MAGNÉTICA
4.2. Separación de sustancias puras en mezclas homogéneas
Los métodos más usados para separar sustancias puras en mezclas homogéneas son:
A) CRISTALIZACIÓN B) DESTILACIÓN C) CROMATOGRAFÍA
TIC 1 .- Visualiza El siguiente video y completa la tabla. https://www.youtube.com/watch?v=cLkCcO3Qc3M
| MÉTODO DE SEPARACIÓN | TIPO DE MEZCLA | ESTADO DE LAS SUSTANCIAS PURAS | EJEMPLO | PROPIEDAD (que permite separar los componentes) | DESCRICIÓN DEL MÉTODO (gráfica o textual) |
|---|
DEBERES (en gris los voluntarios): Pág 78 -> 15, 16; Pág 79 > 24, 30.
M . H. M. 7Tema 9 .- Mezclas 2º ESO (FQ)
M . H . M. 8