Cadena Transportadora de Electrones y Fosforilación Oxidativa
Diapositivas sobre la cadena transportadora de electrones y fosforilación oxidativa. El Pdf describe las estructuras mitocondriales y sus funciones enzimáticas, incluyendo diagramas de lanzaderas de electrones y la síntesis de ATP, para estudiantes universitarios de Biología.
Ver más17 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Cadena Transportadora de Electrones y Fosforilación Oxidativa
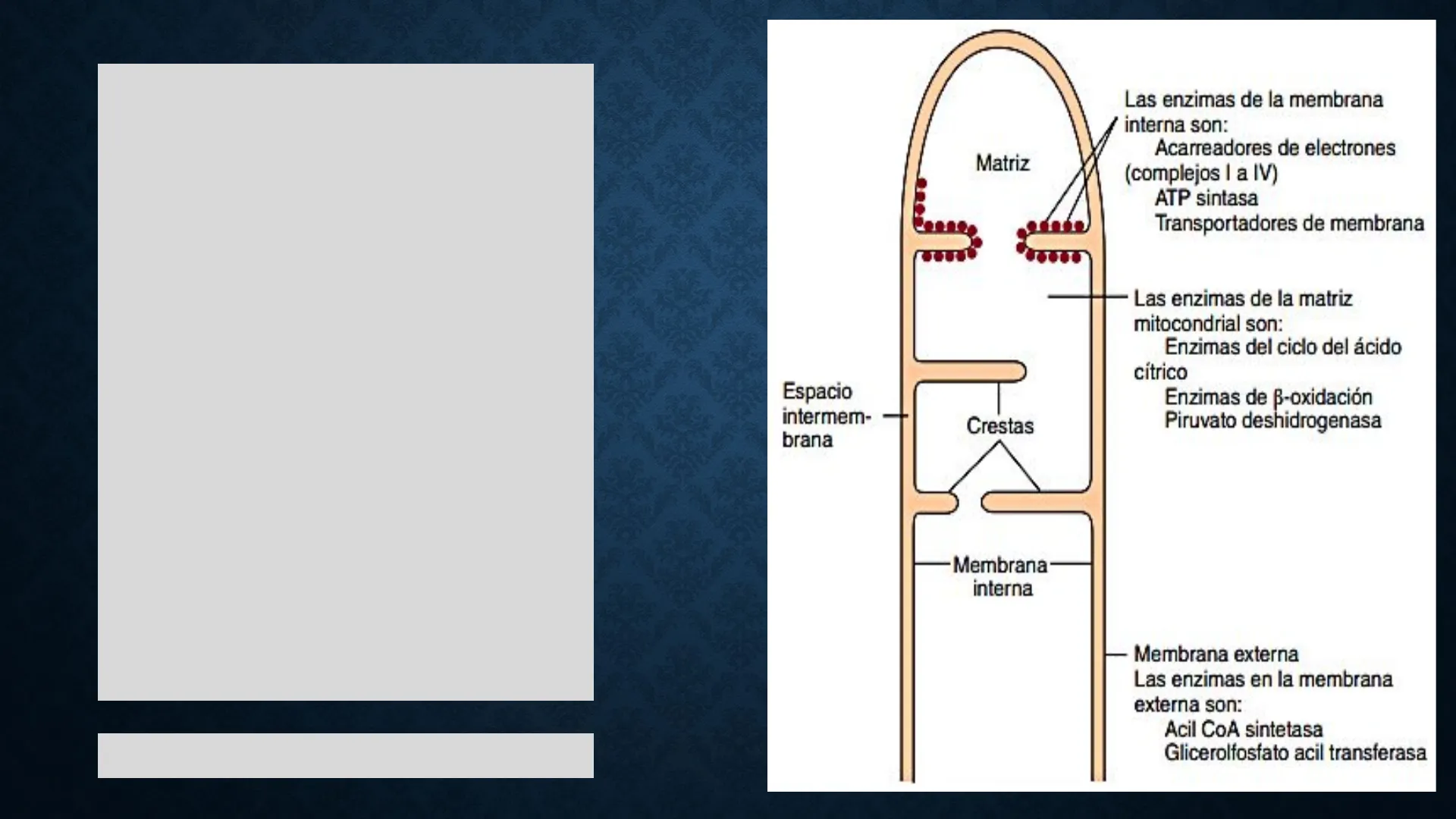
Las mitocondrias están delimitadas por un sistema de dos membranas. La membrana mitocondrial externa contiene enzimas y proteínas de transporte y gracias a la proteína porina (P) formadora de poros es permeable a prácticamente todos los iones, moléculas pequeñas (S) y proteínas de menos de 10.000 Da. Las proteínas grandes deben ser transportadas por los complejos TOM (traslocasa en la membrana mitocondrial externa) y TIM (traslocasas en la membrana mitocondrial interna)
Matriz Mitocondrial
Las enzimas de la membrana interna son: Acarreadores de electrones (complejos | a IV) ATP sintasa Transportadores de membrana
5 Las enzimas de la matriz mitocondrial son: Enzimas del ciclo del ácido cítrico Enzimas de B-oxidación Piruvato deshidrogenasa
Espacio Intermembrana y Crestas
Espacio intermem- brana Crestas -Membrana interna Membrana externa
Las enzimas en la membrana externa son: Acil CoA sintetasa Glicerolfosfato acil transferasa
Rodwell et al., (2016). Bioquímica Ilustrada HarperAlimento
1 ATP Grasa - Digestión y absorción Ácidos grasos + Glicerol ß-Oxidación O2 1 ¥ Carbohidrato > Glucosa, etc. Acetil-CoA Ciclo del ácido cítrico >2H > H20 Cadena respiratoria Proteína Aminoácidos - Mitocondria ADP - Fuentes extramitocondriales de equivalentes reductores
1200 NADH >NAD+ + H H2O 1/2 02 + 2H+ HO HØ ESPACIO ENTRE MEMBRANAS (EXTERIOR) + MEMBRANA INTERNA MATRIZ (INTERIOR) ATP sintasa ATP + H2O ADP + P: H Đ HO
Los organismos aerobios pueden captar una proporción mucho mayor de la energía libre disponible de los sustratos respiratorios que los organismos anaerobios. La mayor parte de este proceso tiene lugar dentro de las mitocondrias, que se han denominado las "centrales de energía" de la célula. La respiración está acoplada a la generación del intermediario de alta energía, ATP
Complejos de la Cadena Respiratoria
Complejo II FADH2 Succinato ubiquinona reductasa H+ H+ H+ 3H+ 1/2 O2 + 2H NADH Complejo I NADH ubiquinona reductasa CoQ Complejo III ubiquinol- citocromo c reductasa CYT c Complejo IV citocromo c oxidasa ATP sintasa H2O H+ H+ H+ 3H ADP + Pi ATP
Función de Transportadores de Electrones en Complejos Multienzimáticos
Los transportadores de electrones de la cadena respiratoria están organizados en complejas membranas supramoleculares incrustadas en la membrana interna mitocondrial. Los complejos I y II catalizan la transferencia de electrones a ubiquinona de dos donantes de electrones diferentes: NADH (Complejo I) y succinato (Complejo II). Complejo III transporta electrones de la ubiquinona reducida al citocromo c, y el complejo IV completa la secuencia transferir electrones del citocromo C al O2.
Glicerol-3-fosfato 1 4H+ 2H+ 4H+ Espacio intermembrana Cit c Cit c Membrana mitocondrial interna Complejo I Fe-S Cit. b - Q FMN Cit. b Cit. c1 Heme a + a3 CUACUB Cit. c1 FAD Fe-S Complejo III Complejo IV Complejo III Matriz mitocondrial 1 NADH + H+ NAD ETF Fumarato Succinato - 1 1/202 + 2H+ H2O Piruvato Ciclo del ácido cítrico Cuerpos cetónicos FAD Acil CoA 4H+ FAD Complejo II Fe-S
Procesos de la Cadena de Transporte de Electrones
La cadena consta de cuatro complejos proteicos;
- La oxidación de NADH o FADH, inicia el transporte de electrones a lo largo de la cadena.
- Los electrones del NADH pasan al complejo I, y los del FADH, van directamente al complejo II. Este se debe a que el FADH, está producido por el succinato deshidrogenasa, una enzima del ciclo de Krebs y que forma parte del complejo II.
- Cada componente de la cadena es, alternativamente oxidado y reducido al pasar os electrones a lo largo de la cadena.
- Finalmente, los electrones se donan al O2 molecular, reduciéndolo a agua.
Succinato Fumarato Complejo II succinato-Q reductasa NADH + H+ 1/202 + 2H+ Q Cit c NAD > H2O Complejo I NADH-Q oxidorreductasa Complejo III Q-cit c oxidorreductasa Complejo IV Cit c oxidasa
Teoría Quimiosmótica de la Fosforilación Oxidativa
La teoría quimiosmótica de la fosforilación oxidativa. Los complejos II, III y IV actúan como bombas de protón, lo que crea un gradiente de protón a través de la membrana, que es negativa en el lado de la matriz. La fuerza motriz de protón generada impulsa la síntesis de ATP conforme los protones fluyen de regreso hacia la matriz por medio de la enzima ATP sintasa. Los desacopladores aumentan la permeabilidad de la membrana a iones, lo que colapsa el gradiente de protón al permitir que el H1 pase sin atravesar la ATP sintasa y, así, desacopla el flujo de electrón a través de los complejos respiratorios, de la síntesis de ATP. (Q, coenzima Q o ubiquinona; cit., citocromo.)
4H+ 4H+ 2H+ H+ Desacopladores H+ H+ H+ H+ Espacio intermembrana + ++++ ++++++ +++ Complejo Complejo IV Fo Q F1 (H+ H+ Matriz mitocondrial NADH + H+ NAD 1/202 + 2H+ H2O ADP + Pi ATP Complejo 11 Succinato Fumarato Cit c Complejo Membrana mitocondrial interna H+2H+ 4H+ 4H+ Cyt c Intermembrane + + + space IV + + 7 + + × H2O + + Fumarate 2 02 + 2H+ 1 Succinate NADH + H+ NAD+ Matrix F1 ATP H+ 1 Chemical potential ApH (inside alkaline) ATP synthesis driven by proton-motive force Electrical potential (inside negative) + ADP + Pi F I I + II Q III + + + + Flujo de electrones a través de los complejos de cadena respiratoria, que muestra los puntos de entrada de equivalentes reductores desde sustratos importantes. Q y cit. son componentes móviles del sistema según se indica por las flechas punteadas. El flujo a través del complejo III (el ciclo Q) (cit, citocromo; ETF, flavoproteína transferidora de electrón; Fe-S, proteína hierro-azufre; Q, coenzima Q o ubiquinona.) I
Complejo de la ATP-Sintasa
Espacio intermembrana H+ H+ H+ H+ H+ Anillo C C a Fo Membrana mitocondrial interna Motor y poro de protón Y H+ - b Matriz F1 ATP sintasa (ATPasa) 8 ATP ADP(+ Pi Complejo de la ATP-sintasa. El complejo de la ATP-sintasa está formado por un motor (F0) y un generador (F1). El poro de protones consta del anillo c y la proteína a. El componente rotatorio es la subunidad G enrollada en espiral, que está unida a la subunidad E y al anillo c. El componente estacionario es la unidad hexamérica A3B3, que es mantenida en su lugar por las proteínas &, b y a. (Baynes y Dominiczak, 2011).
Transducción de Energía y Coenzimas Redox
Transducción de la energía desde las coenzimas reducidas al fosfato de alta energía: Las principales coenzimas redox son NAD+, FAD y FMN Las principales coenzimas de oxidación-reducción (redox) que participan en la transducción de la energía desde los combustibles al ATP son la nicotinamida-adenina-dinucleótido (NAD+), la flavina-adenina-dinucleótido (FAD) y la flavina-mononucleótido (FMN). Durante el metabolismo energético, se transfieren los electrones de los hidratos de carbono y las grasas a estas coenzimas, que pasan a sus formas reducidas (NADH, FADH2 y FMNH2).
H+ H+ H+ H H H+ H+ H+ ATP sintasa Bomba de protones 2H2º H+ H+ H+ H+ H+ ATP ATP H+ Electrones (e-) NADH, FADH2 Proteínas mitocondriales ADP ADP + Pi P H+ CH+ Lanzaderas CO2 H- UCP-H+ Ciclo ATC Oxidación de ácidos grasos ADNmt Grandes proteínas nucleares codificadas Ácidos grasos Piruvato H+ IMM TIM H+ H+ H+ H (H+ TOM OMM Combustibles H+ H+ H+ H+ 02 NADH (T) Matriz H' H+ H+ Transportadores IMS H+ H+Balance energetico del metabolismo anaeróbico y aeróbico de una molécula de glucosa
Balance Energético del Metabolismo de Glucosa
| Ruta metabólica | Producción ATP EC: | ATP Congreso UIB |
|---|---|---|
| Glucólisis | ||
| · 2 ácido piruvico | 6 ATP | 5 ATP |
| · 2 NADH | ||
| · 4 ATP-2 ATP= 2 ATP | 2 ATP | 2 ATP |
| Oxidación del piruvato (2) | ||
| 2 NADH | 6 ATP | 5 ATP |
| Ciclo de Krebs | ||
| · 3 NADH (2) | 18 ATP | 15 ATP |
| · FADH2 (2) | 4 ATP | 3 ATP |
| · GTP (2) | 2 ATP | 2 ATP |
| Sub total | 38 ATP | 32 ATP |
| Lanzadera Malato aspartato | -2 ATP | -2 ATP |
| Total | 36 ATP | 30 ATP |
Inhibidores de la Cadena Respiratoria
Muchos venenos inhiben la cadena respiratoria. Los barbitúricos, como el amobarbital, inhiben el transporte de electrones mediante el complejo I al bloquear la transferencia desde Fe-S hacia Q. En dosificación suficiente, son mortales in vivo. La antimicina A y el dimercaprol inhiben la cadena respiratoria en el complejo III. Los venenos clásicos H2S, monóxido de carbono y cianuro inhiben el complejo IV y, en consecuencia, pueden suspender por completo la respiración. El malonato es un inhibidor competitivo del complejo II.
Malonato Complejo II Succinato FAD Fe-S Carboxina TTFA H2S CO CN" Complejo IV Complejo III NADH FMN, Fe-S Cit b, Fe-S, Cit c, Cit c + 02 Cu Cu 1 O Desacopladores € Piericidina A Amobarbital Rotenona Desacopladores Oligomicina Oligomicina ADP + P; ATP ADP + P; ATP ADP + Pi ATP BAL Antimicina A Complejo I hem a hem a3
Lanzaderas de Electrones
Durante el metabolismo de los hidratos de carbono, en el citosol se produce NADH. EI NADH no puede atravesar la membrana mitocondrial interna y, por tanto, no puede ser oxidado por el sistema de transporte de electrones. Dos lanzaderas redox permiten la oxidación de NADH citosólico sin su transferencia física a la mitocondria. La más sencilla de las dos lanzaderas es la glicerol-3-P transfiere los electrones del NADH desde el citoplasma a la mitocondria reduciendo FAD a FADH,
Lanzadera Glicerol Fosfato
2. Lanzadera glicerol fosfato Citosol Matriz mitocondrial CH,OH 1 NADH + H+ C=0 FADH, QH2 1 CH20-P Glicerol-3-P deshidrogenasa citosólica Glicerol-3-P deshidrogenasa mitocondrial NAD+ CH2OH HO-C-H I FAD CH20-P - Membrana mitocondrial interna
Lanzadera Malato-Aspartato
Lanzadera malato-aspartato a-cetoglutarato + Aspartato Aspartato + a-cetoglutarato AST AST COOH 1 Glutamato Glutamato Oxaloacetato NADH + H+ Complejo | NADH+H+ CH2 C=0 - E Malato deshidrogenasa mitocondrial Oxaloacetato COOH NAD+ Malato NAD+ CH2 HO-C-H 1 COOH Matriz mitocondrial Malato Citosol Membrana mitocondrial interna Fuente: (Baynes y Dominiczak, 2011). Malato deshidrogenasa citoplásmica 3 COOH
Cadena Transportadora de Electrones y Fosforilación Oxidativa
Membrana externa Espacio intermembranal H* H+ H* H+ H H* H* H* H* 4 H* 4 H* H H+ H+ 4 H* H' H H* H' F-S 2e- 2e- C 2e- CoQ C1 Cu++ 2e- 1 2e- P 2e- FP ETF b 81 ADP 4 H* H* 4 H* 2 H* - NAD+ 1 FADH2 H+ H* H+ NADH H* H' H' H+ 1202 H2O COMPLEJO I NAD Deshidrogenasa {Flavoproteínas FPÌ COMPLEJO II Succinato Deshidrogenasa COMPLEJO III Citocromo reductasa [Citocromo b y c) COMPLEJO IV Citocromo Oxidasa [Citocromo a1 y a3) COMPLEJO V ATP sintasa (Fo y F1) H H+ 2 H* F-S 2e- Membrana Interna (Cresta Mit.] 2e- ATP Matriz Mitocondrial 2e-