Hemoglobina: estructura, función y transporte de oxígeno en la sangre
Diapositivas de Unam.mx sobre Hemoglobina: estructura, función y transporte de oxígeno. El Pdf es una presentación didáctica de Biología a nivel universitario, que explora las diferencias entre hemoglobina fetal y adulta, y el impacto de factores externos como el CO.
Ver más18 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
PROTEINAS
HEMOGLOBINA
Medicina Dra. María Fernanda Alves Rosa
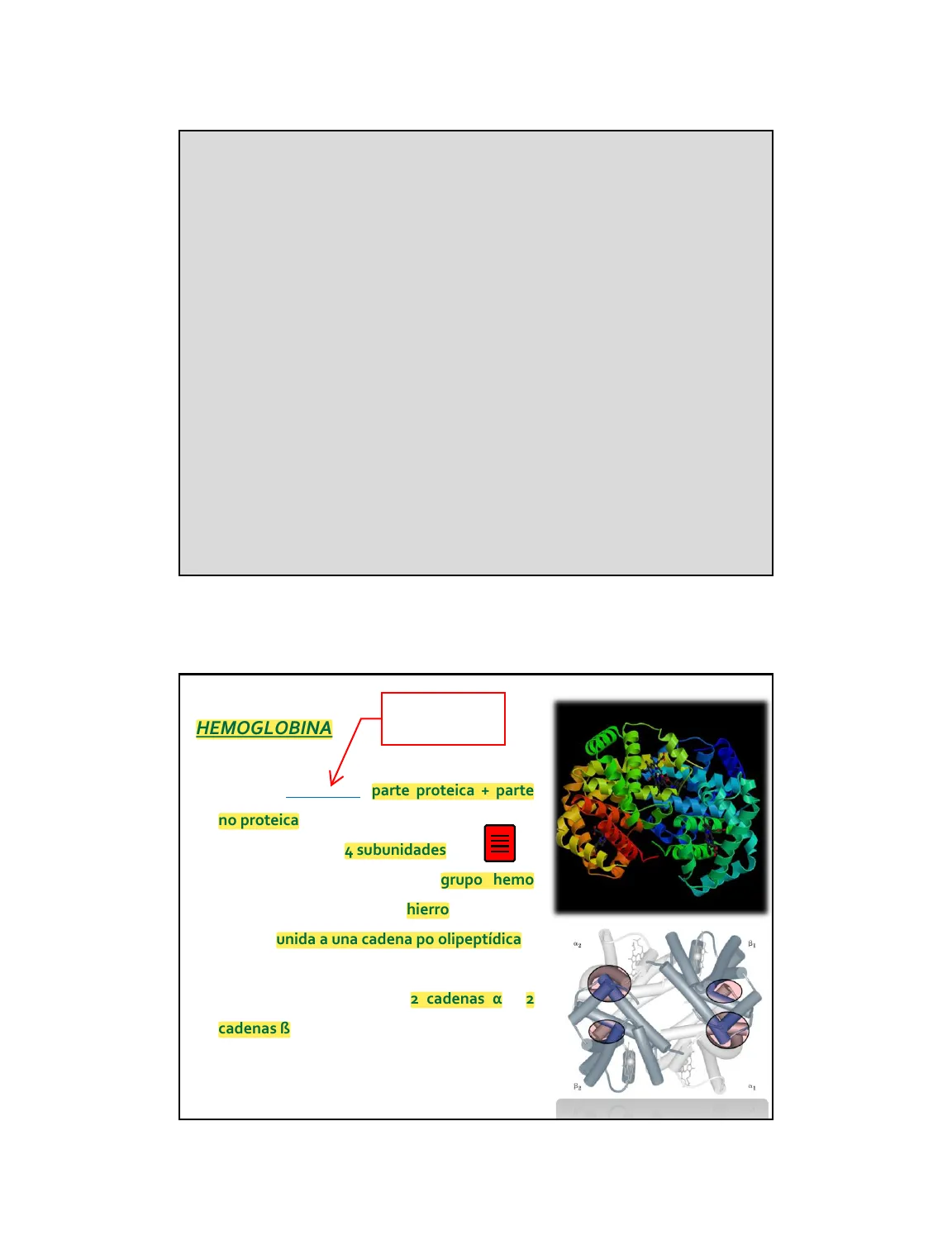
HEMOGLOBINA
Estructura Cuaternaria
Proteína conjugada (parte proteica + parte no proteica) de 64.400 daltons. Está formada por 4 subunidades . Cada subunidad posee un grupo hemo (porfirina) que contiene hierro en estado ferroso unida a una cadena po olipeptídica.
La Hb A -> más del 95% de la Hb normal del adulto está formada por 2 cadenas x y 2 cadenas ß.
₿1 B2 αι 1ß α Grupo HEMO Fe++ ß α
TRANSPORTE DE OXÍGENO POR LA SANGRE
El transporte de oxigeno por la sangre es esencial para un correcto metabolismo celular en todos los tejidos del organismo.
El O2 es transportado bajo dos formas:
- 3% circulación disuelto en el plasma -> solubilidad en plasma es muy baja (0,3 ml de O2 en 100 ml de sangre arterial).
- 97% es transportado en unión reversible con la hemoglobina. . Por lo tanto en condiciones normales -> O2 es transportado en casi su totalidad por la Hb !!!
2Hem B2 ß1 · El Fe del grupo hemo se combina en forma reversible con una molécula de O2 reacción de oxigenación. · Cada molécula de Hb reacciona con 4 moléculas de O2. · Hb -> 2 estructuras estables y distintas: ▪ Oxihemoglobina. Desoxihemoglobina. · Desoxihb o T (tensa) -> conformación -> muchos puentes salinos entre las subunidades y dentro de ellas. · OxiHb o R (relajada) -> a medida que capta sucesivas moléculas de O2, -> ruptura de puentes -> conformación relajada !!
PDB-101: Molecule of the Month: Hemoglobin (rcsb.org) Cambio conformacional de la hemoglobina (uah.es) oxy · Reacciones de unión de O2 a Hb -> ocurren en forma secuencial ->reacción de un hem con O2 -> afecta la estructura que rodea a los hemos restantes produciendo un cambio conformacional. · Así, la unión de la cuarta molécula de O2 es más fácil que la primera. . Esta interacción hem-hem es una expresión de las propiedades alostéricas de la Hb.
3El efecto alostérico T State KT O2 O2 O2 O2 O2 O2 O2 O2 O2 O2 1 1| 1 KR O2 O2 O2 O2 O2 O2 O2 O2 O2 O2 R State R State strongly favored
Comencemos a pensar:
Con respecto al transporte de oxígeno en la sangre, señale la opción correcta:
- El oxigeno presenta alta solubilidad en el plasma, por lo que se transporta principalmente disuelto en el mismo.
- El O2 se transporta únicamente unido a la Hb, ya que no es un gas soluble en plasma.
- Un pequeño porcentaje de O2 se transporta en combinación con la Hb y un 97% aproximadamente disuelto en plasma.
- El O2 es transportado en su mayor parte mediante la combinación de 4 moléculas de oxígeno con los grupos hemo de cada molécula de Hb.
Rta: d
Indique la opción incorrecta:
- La Hb también puede presentarse en estado tenso (T), por uniones electrostaticas entre las cadenas de globina .
- La Hb es una proteina conjugada que tiene la propiedad de combinarse en forma irreversible con 4 moléculas de oxígeno.
- La oxiHb presenta una conformación R (relajada) debido a la ruptura de puentes salinos al captar las moléculas de oxígeno.
- La oxigenación de los hemos de la Hb no se realiza en forma simultánea, sino secuencial.
Rta: b
4 T State strongly favored
ALGUNOS CONCEPTOS IMPORTANTES
Capacidad de O2 de la Hb:
V Def .: Cantidad de O2 que se combina con la Hb a presiones parciales de O2 (PO2) elevadas. v 1 gr de Hb transporta 1,34 ml de O2 v En sangre -> 15 gr Hb / 100ml sangre. ✓ La capacidad será igual a : 1,34 x 15 = 20,1 ml de O2/100 ml de sangre
Porcentaje de saturación de la Hb:
v Def .: Porcentaje de grupos hem unidos a O2. v % de sat. Hb = Q2 combinado con Hb Hb/100mm de sangre x 100 Capacidad de O2 de Hb/100ml de sangre v Veamos un ejemplo .... v Si la saturación de la Hb es del 97% en sangre arterial (PO2 = 95 mmHg) ¿Cuánto será el volumen de O2 combinado con la Hb? v Rta= 19,5 ml de O2/100 ml de sangre v Indica que ocurre en la sangre venosa mixta (PO2=40 mmHg) donde el % de saturación es del 75%.
Coeficiente de utilización de la Hb:
- Fracción de Hb que cede su O2 a los tejidos cuando la sangre pasa por los capilares tisulares.
- En condiciones de reposo ~ el 25%, (Ej .: 20 ml de O2-> Hb cede a los tejidos 5 ml de O2 /100 ml de sangre).
- Durante el ejercicio intenso 1 requerimientos tisulares de O2 -> 1 coeficiente de utilización hasta un 75% (Ej .: 20 ml de O2-> Hb cede a los tejidos 15 ml de O2 /100 ml de sangre) -> aumento 3x veces la oferta de O2.
Apliquemos estos conceptos para responder las siguientes preguntas:
- Un paciente anémico tiene una concentración de Hb de 10 gr./100 ml de sangre, con pulmones normales y una PO2 arterial de 95 mmHg. ¿ Cuál será su capacidad de O2? Rta: 13,4 ml de O2, por cada 100 ml de sangre.
- En el mismo paciente, teniendo en cuenta dicha capacidad y que el % de saturación de la Hb es del 97%, ¿Cuál será el volumen de O2 que es transportado en combinación con la Hb por cada 100 ml de sangre? Rta: 12,99 ml de O2
5
Analicemos:
Con respecto a las siguientes afirmaciones:
A - La Hb es una proteina con propiedades alostéricas. B- La reacción de un grupo hem con el oxígeno afecta la estructura que rodea a los hemos restantes.
- La primera es falsa y la segunda es verdadera.
- Ambas afirmaciones son falsas.
- Ambas afirmaciones son correctas y están relacionadas.
- Ambas afirmaciones son verdaderas y no presentan relación.
Rta: c
Aumenta Afinidad P50 bajo (mover curva izquierda) - pH Alto - Temperatura Baja
Disminuye Afinidad - P50 alto (mueve curva a derecha) pH Bajo - Temperatura Alta
Ahora estamos en condiciones de analizar la curva de disociación de la Hb ... Esta curva nos permite estudiar muchas de las propiedades de la Hb.
100 Zona de 20 a meseta -> Saturación de la hemoglobina (%) 16 V =60 «- Zona de máxima pendiente (zona de descarga) P 50 40 8 20 4 O2 disuelto físicamente 0 20 40 60 80 100 120 140 PO2 (mm Hg) CURVA DE DISOCIACIÓN DE LA HB
¿Cuál será el % de saturación de la Hb es A una PO2 normal en sangre arterial (95 mmHg) EFECTO ALOSTÉRICO
6
Contenido de O2 (ml/100 ml de sangre)
Usemos la curva para seguir la ruta del O2 desde los pulmones a los tejidos ...
Curva -> relación entre la PO2 (eje horizontal) y el % de saturación de la Hb (eje vertical) -> A una PO2 normal en sangre arterial (95 mmHg) el % de saturación de la Hb es del 97%.
Cuando la PO2 aumenta por encima de 100 mmHg, la Hb no puede combinarse con mayor cantidad de O2.
- Ej .: zonas de aire comprimido (profundidad del mar o cámaras presurizadas) -> PO2 alveolar asciende sobre su nivel normal de 104 mmHg.
- Una PO2 entre 100 y 70 mmHg -> pocos cambios en la cantidad de O2 captado por la Hb -> zona plana de la curva. (El descenso de la PO2 disminuye la saturación de O2 en ~5%).
- Ej .: podemos escalar una montaña, volar un aeroplano o vivir a grandes altura sin que resulte alterada significativamente la cantidad de O2 que es transportado por la sangre.
- Con una PO2 entre 40 y 10 mmHg la curva se vuelve descendente, favoreciendo así la liberación de O2 de la Hb en los tejidos.
- Esta PO2 es la que hallamos en tejidos que poseen un metabolismo alto y activo.
100 Saturación de Oxigeno 80 60 40 20 0 0 20 40 60 80 100 PO2 (mm de Hg)
La curva presenta una forma sigmoidea!
¿Por qué sucede ésto?
- La afinidad de la Hb por el O2 no es la misma en todo el rango de PO2.
- Zonas con PO2 bajas -> afinidad por el O2 s baja
- Zonas con PO2 elevada -> afinidad por el O2 es mayor.
Aumenta Afinidad - P50 bajo (mover curva izquierda) - pH Alto - Temperatura Baja
Disminuye Afinidad - P50 alto (mueve curva a derecha) - pH Bajo - Temperatura Alta
¿Qué ventajas fisiológicas piensas que tiene esta situación?
- Parte superior de la curva representa PO2 -> barrera hemato-gaseosa en los pulmones -> Hb capta O2.
- Pequeñas disminuciones de la PO2 del gas alveolar apenas afectan el contenido de O2 de la sangre arterial y en consecuencia, la cantidad de O2 disponible para los tejidos.
- La parte inferior mas "empinada" representa -> tejidos periféricos -> baja PO2 -> tejidos pueden obtener (extraer) gran cantidad de O2 -> Hb cede O2.
100 20 Zona de meseta -> a 80 16 V 60 12.9 «- Zona de máxima pendiente (zona de descarga) 8 3 20 4 O2 disuelto fisicamente 0 20 40 60 80 100 120 140 PO2 (mm Hg) Figura 21-5. Curva de disociación de la hemoglobina. a, arterial; v, venosa; P50, presión parcial de oxígeno necesaria para saturar el 50 % de la hemoglobina con oxígeno.
Saturación de la hemoglobina (%)
40
Contenido de O2 (ml/100 ml de sangre)
7
Alveolo Aorta- Bronquio Bronquiolos Alveolo Aire que penetra en el alveolo Tráquea Arterias pulmonares Vena cava superior Difusión de CO2 Difusión de oxígeno Red de capilares
Hora de pensar:
De las características de la curva se deduce que:
- La afinidad de la Hb es la misma en todo el rango de PO2
- Entre una PO2 de 100 y 70 mmHg, la zona plana de la curva, disminuye la saturación de oxigeno de la Hb en un 50%.
- A bajas presiones parciales de O2 la Hb tiende a mantener su estado de oxihemoglobina
- Los tejidos con metabolismo aumentado facilitan la liberación de oxígeno por parte de la Hb.
Rta: d
8
La Pro es un indicador del estado de la curva.
- Es la PO2 a la cual la Hb esta saturada al 50% con O2.
- Su valor en condiciones normales de reposo es de 27 mmHg.
- Aplicación práctica: Mayor valor -> menor sera la afinidad de la Hb por el O2/
- Menor valor -> mayor sera la afinidad de la Hb por el O2.
100 Saturación de Oxígeno 80 60 P 50=27 mmHg 40 20 P 50 0 0 20 40 60 80 100 pO2 (mm de Hg)
Aumenta Afinidad - P50 bajo (mover curva izquierda) - pH Alto - Temperatura Baja
Disminuye Afinidad - P50 alto (mueve curva a derecha) - pH Bajo - Temperatura Alta
Pensemos un poquito mas ...
Conocer el valor de P50 es útil porque:
- Indica si hay una cantidad de hemoglobina normal.
- Relaciona el porcentaje de saturación de la Hb - O2 con respecto a la PCO2.
- Las variaciones de su valor indican variaciones en la afinidad de la Hb por el oxígeno.
- El aumento de su valor es un índice de que los tejidos están recibiendo menos O
Rta:c
9
¿Que implica un desplazamiento de la curva hacia la derecha o la izquierda de la grafica?
- Podemos hablar de: Y Desplazamiento de la curva a la derecha.
- Desplazamiento de la curva a la izquierda.
100 Saturación de Oxigeno 8 8 60 40 20 0 0 20 40 60 80 100 PO2 (mm de Hg)
- Desplazamiento a la derecha -> afinidad de la Hb por el O2 ha disminuido -> Hb cede más O2.
- Desplazamiento sea a la izquierda -> afinidad ha aumentado-> a una misma PO2 la saturación de la Hb es mayor y por lo tanto en esta situación se libera menos O2.
Entonces: las Propiedades ideales de la Hb como Transportador de O2 se basan en que su afinidad aumenta cuando tiene que tomar O2, (ej .: ? ), y que ésta disminuye cuando tiene que cederlo (ej .: ? ).
FACTORES PROVOCAN CAMBIOS EN LA CURVA DE DISOCIACIÓN DE LA Hb
- PpCO2 Y PH v Temperatura V Concentración de 2,3 difosfoglicerato v Caso especial: CO
10