Regulación ácido-base y control respiratorio y renal del pH, UNAM
Documento de la Facultad de Medicina, UNAM sobre Regulación ácido-base y control respiratorio y renal del pH. El Pdf, de Biología para Universidad, explica los mecanismos fisiológicos, definiciones de protón, ácido y base, y sistemas de compensación, incluyendo una tabla de pH y H+.
Ver más12 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Regulación Ácido-Base
Facultad de Medicina UNIVERSIDAD NACIONAL A Departamento de Fisiología, Facultad de Medicina, UNAM Unidad temática II: Sesión IX Regulación ácido-base Control respiratorio y renal del pH.
Resultado de Aprendizaje
Analiza los mecanismos que regulan el pH en el organismo, en la resolución de un problema.
Introducción a la Regulación del pH
1. Introducción El mantenimiento del pH del medio interno, dentro de unos límites estrechos, es de vital importancia para los seres vivos. Es una de las constantes que el organismo trata de mantener con más tenacidad, por ser fundamental en la actividad enzimática y otras funciones vitales. Diariamente el metabolismo intermedio va a generar una gran cantidad de ácidos, pese a lo cual, la concentración de hidrogeniones [H+] libres en los distintos compartimentos corporales va a permanecer fija dentro de unos límites estrechos. Ello es debido a la acción de los amortiguadores fisiológicos que van a actuar de forma inmediata impidiendo grandes cambios en la concentración de hidrogeniones, y a los mecanismos de regulación pulmonar y renal, que son en última instancia los responsables del mantenimiento del pH.
Protón
Núcleo electropositivo del átomo de hidrógeno ordinario. Partícula elemental y estable. Cuando se disuelve el hidrógeno en agua se ioniza en H+ y un electrón. Los núcleos de todos los elementos contienen un número de protones señalado por el número atómico del elemento.
Ácido y Base
Siguiendo la definición de Bronsted, un ácido es aquella sustancia capaz de ceder iones H+ y una base es aquella capaz de captar iones H+. Existen dos clases de ácidos importantes en fisiología: Ácido carbónico (H2CO3) y Ácidos no Carbónicos. Hacer esta distinción es importante debido a las diferentes tasas de producción y rutas de eliminación de estos ácidos. Los ácidos y bases se pueden clasificar en fuertes y débiles. Son ácidos y bases fuertes aquellos para los que, en concentraciones ordinarias, prácticamente todas sus moléculas están disociadas. Los ácidos y bases débiles tienen constantes de ionización pequeñas, de forma que cuando se disuelven con concentraciones ordinarias de agua gran parte de sus moléculas se mantienen sin disociar.
Acidez de una Solución
Depende de su concentración en H+ con independencia de la sustancia disociada que lo libera
Constante de Disociación
La constante de disociación ácida K se puede definir como una relación entre las concentraciones de ácido disociado y sin disociar. Kc= ([A] . [B]) / [AB]Facultad de Medicina UNIVERSIDAD NACIONAL AUTONOMA B Departamento de Fisiología, Facultad de Medicina, UNAM En los ácidos fuertes K adquiere mayor valor, dado que las concentraciones de A y B serán altas y la concentración AB (ácido sin disociar) será baja. Si el valor de K para un ácido es bajo, esto significa que es un ácido débil, se disocia escasamente, por lo tanto, las concentraciones de A y B serán bajas, y la concentración de AB será elevada. Por lo tanto, podemos decir que la constante de disociación ácida K, es una medida cuantitativa de la fuerza de un ácido. Una sustancia disociable en solución libera electrolitos, alcanza siempre un nivel en el que se estabiliza una fracción disociada y otra sin disociar. En ese momento la velocidad de disociación y la de reconstrucción son idénticas.
Ley de Acción de Masas
La ley de acción de masas postula que la velocidad de una reacción es proporcional al producto de las concentraciones de sus reactantes. Conforme se va agotando la sustancia disminuye la velocidad de disociación hasta igualar a la reconstrucción. Por ejemplo: el agua puede disociarse en hidrógeno e hidroxilo: H20 H+ + OH
pH
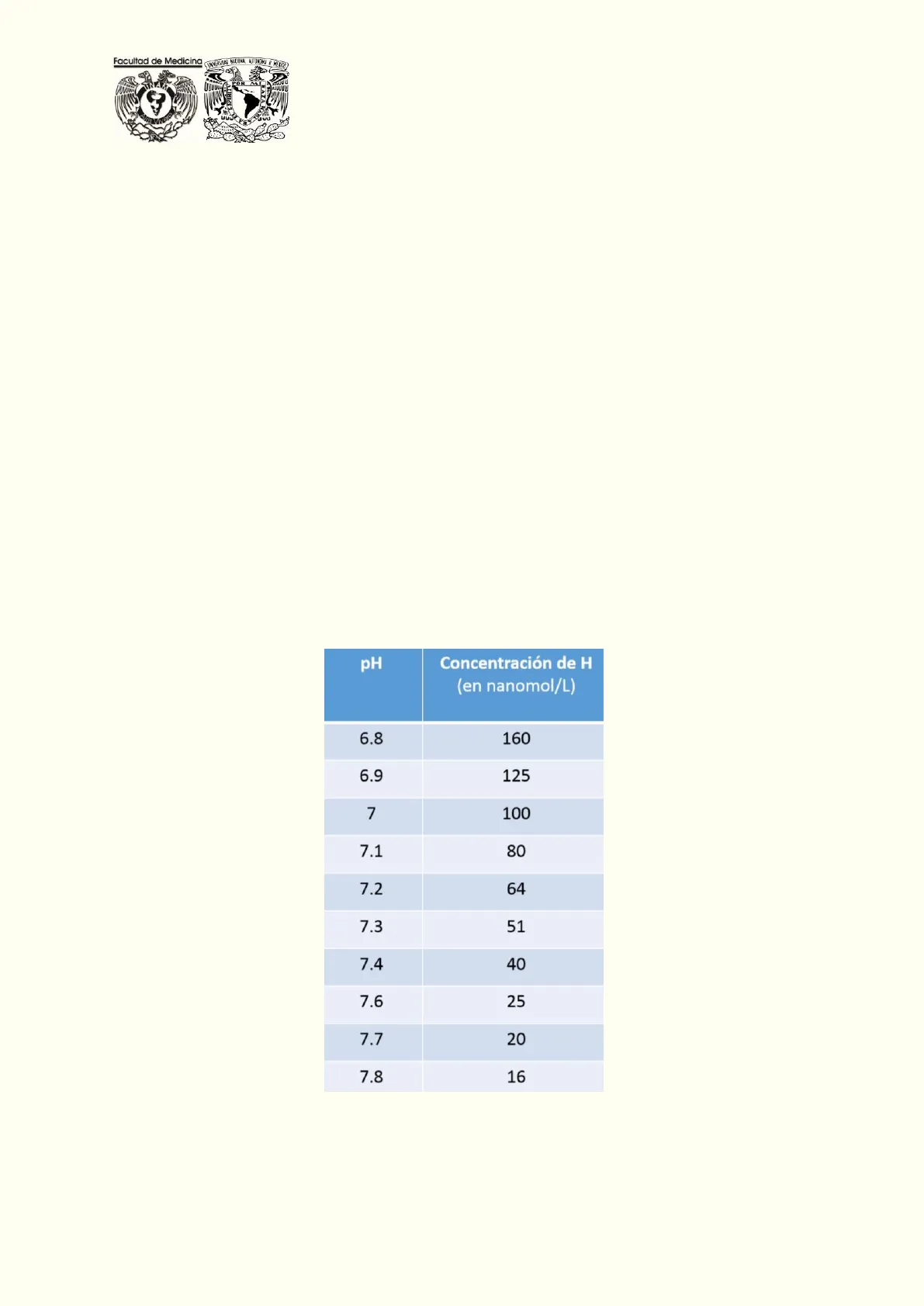
Logaritmo inverso de la concentración de hidrogeniones, expresa la cantidad de H+ de una solución. Expresar cifras tan bajas de concentración (nanogramos) es incómodo por lo que la obtención de su logaritmo negativo proporciona cifras de más fácil comprensión y por tanto más fácil manejo.
pH Concentración de H (en nanomol/L) 6.8 160 6.9 125 7 100 7.1 80 7.2 64 7.3 51 7.4 40 7.6 25 7.7 20 7.8 16 Tabla 1. Relación entre el pH arterial y la concentración de H+
Anión Gap
Para mantener la electroneutralidad, las cargas positivas (cationes) deben igualar a las cargas negativas (aniones); si no ocurre así, aparece un anión gap cuyo valor normal es de 8 a 16 mEq/l y que se calcula con la siguiente ecuación:Facultad de Medicina UNIVERSIDAD NACIONAL AJTINUM. IMA B Departamento de Fisiología, Facultad de Medicina, UNAM Anión Gap = Na+ - (Ct + HCO3-) Tendemos a la acidosis: el metabolismo diario genera 13000-15000 mmol/d de CO2 que podría generar 13.000 mEq de H+ cada día y otros ácidos aportados, por ejemplo, por la dieta (aporta ácidos orgánicos, aminoácidos azufrados, residuos fosfato y sulfato) que aportan unos 70 mEq de H+ también cada día. En condiciones normales la concentración de H+ del líquido extracelular es baja (de unos 40 nEq/l). A pesar de ello, pequeñas fluctuaciones de esta van a tener repercusiones importantes sobre determinados procesos vitales. Por ello, existen unos límites relativamente estrechos entre los cuales la concentración de H+ es compatible con la vida. Dichos valores oscilan entre 16 y 160 nEq/l, lo que equivale a un valor de pH de 7.80 a 6.80 (Tabla 1). El principal producto ácido del metabolismo celular es el dióxido de carbono (CO2) que viene a representar un 98% de la carga ácida total. Aunque no se trate de un ácido, pues el CO2 no contiene H+, se trata de un ácido potencial ya que su hidratación mediante una reacción reversible catalizada por la anhidrasa carbónica (A.C.) va a generar ácido carbónico. CO2 + H20 <> H2CO3 <> H+ + HCO3- Al ser un gas, el CO2 va a ser eliminado prácticamente en su totalidad por los pulmones sin que se produzca una retención neta de ácido, por lo que se denomina ácido volátil. Por otra parte, el metabolismo va a generar una serie de ácidos no volátiles, también denominados ácidos fijos que representan de un 1-2% de la carga ácida y cuya principal fuente es el catabolismo oxidativo de los aminoácidos sulfurados de las proteínas. Estos ácidos fijos no pueden ser eliminados por el pulmón siendo el riñón el principal órgano responsable en la eliminación de estos.
Alteración del pH
Las desviaciones de la normalidad del pH pueden ser hacia la acidosis o hacia la alcalosis. Tanto una como otra pueden depender de variaciones del bicarbonato o de la presión parcial de CO2. En el primer caso el trastorno se califica metabólico y en el segundo respiratorio. Por otra parte, la anormalidad puede estar compensada o descompensada, lo primero cuando los sistemas controladores del pH no afectados por la causa del trastorno consiguen que se mantenga el pH dentro de límites normales y lo segundo cuando no lo logran por haber sido desbordados.
Cambio Primario Compensación. Descompensacion. TRASTORNO pCO2 Bicarbonato pCO2 Bicarbonato [H+] PCO2 Bicarbonato Acidosis Respiratoria Î L 1 Acidosis Metabólica - L - 1 T 1 Alcalosis Respiratoria Alcalosis Metabólica Tabla 2. Compensacion y Caracterizacion de los Trastornos del equilibrio Ácido-BaseFacultad de Medicina UNIVERSIDAD NACIONAL A Departamento de Fisiología, Facultad de Medicina, UNAM Las consecuencias de la alteración del equilibrio ácido-base son la alteración de la distribución de los iones en los espacios intra y extracelular, lo que modifica la actividad de numerosas enzimas, se producen cambios estructurales en las macromoléculas y alteraciones en equilibrios químicos. Si los trastornos son graves comprometen la vida.
Sistemas de Compensación del pH
Es tan importante el mantenimiento del pH que hay varios sistemas de compensación que funcionan de forma alternativa, de forma que la disfunción de alguno de ellos debe ser compensada por otro; unos son de actuación inmediata y otros lenta pero definitiva. Existen unos sistemas de compensación inmediatos que se denomina amortiguación y que se produce en segundos; posteriormente entra en funcionamiento el sistema de compensación pulmonar cuya acción se produce en horas y finalmente se produce la compensación renal que puede tardar varios días en corregir la sobrecarga.
Amortiguadores Fisiológicos
Amortiguadores extracelular célula medio o R P fosfato inorgánico P o o R P o o proteínas P P bicarbonato P P P fosfato orgánico Fig. 1. Distribución de los sistemas "Buffer" También denominados sistemas tampón o "buffer" (almohadilla o muelle). Representan la primera línea de defensa ante los cambios desfavorables de pH gracias a la capacidad que tienen para captar o liberar protones de modo inmediato en respuesta a las variaciones de pH que se produzcan. Un sistema tampón es una solución de un ácido débil y su base conjugada: H (ácido) <> H+ + A- (base) o o PFacultad de Medicina UNIVERSIDAD NACIONAL A TUNGMA 8 Departamento de Fisiología, Facultad de Medicina, UNAM El valor de pH en el cual el ácido se encuentra disociado en un 50% se conoce como pK. El pK representa el valor de pH en el que un sistema tampón puede alcanzar su máxima capacidad amortiguadora. Por tanto, cada sistema buffer tendrá un valor de pK característico. Cuando ingresan radicales ácidos en el medio interno se combinan con el catión de la sal y la consecuencia es la disminución de ésta y el aumento del ácido, pero como éste último es débil, (lo que significa que está poco disociado) el resultado final es que un ácido fuerte que aportaría muchos hidrogeniones se transforma en uno débil y apenas varía el pH.
Amortiguador Proteína
Las proteínas intracelulares con sus grupos ionizables con diferentes valores de pK contribuyen de forma importante en el mantenimiento del pH, mediante el intercambio de H+ con iones unidos a proteínas que se desplazan al medio extracelular para mantener la neutralidad eléctrica. Especial mención merece el sistema amortiguador hemoglobina, es un tampón fisiológico muy eficiente debido tanto al cambio de pK que experimenta al pasar de la forma oxidada a la reducida, como a la gran abundancia de esta proteína en la sangre (15% del volumen total sanguíneo) y al hecho de que actúa dentro de los hematíes: HbH+ <> Hb- + H+ Las propiedades amortiguadoras de la hemoglobina desempeñan un papel fundamental en el transporte sanguíneo del CO2 tisular hasta su eliminación pulmonar. En el interior del hematíe, por acción de la Anhidrasa Carbónica, el CO2 se va a convertir en ácido carbónico que se disocia dando un H+ que rápidamente será tamponado por la hemoglobina, y bicarbonato que saldrá del hematíe en intercambio con iones cloro.
Amortiguador Fosfato
Ejerce su acción fundamentalmente a nivel intracelular, ya que es aquí donde existe una mayor concentración de fosfatos y el pH es más próximo a su pK (6.8). Interviene junto a las proteínas celulares de manera importante en la amortiguación de los ácidos fijos: PO4 H2 <>PO4 H + H+
Amortiguación Ósea
El hueso interviene en la amortiguación de la carga ácida captando los H+ en exceso o liberando carbonato a la sangre por disolución del hueso mineral. El papel más importante del hueso en la amortiguación ocurre en situaciones de acidosis crónica tales como en los casos de insuficiencia renal crónica en la que la parathormona juega un papel fundamental. Este sistema de amortiguación también va a intervenir en presencia de una carga básica a través del depósito de carbonato en el hueso.
Amortiguador Carbónico/Bicarbonato
Poco potente desde el punto de vista químico, (pK =6.1). Es el tampón más importante en la homeostasis del pH porque: • Está presente en todos los medios tanto intracelulares como extracelulares. En el medio extracelular la concentración de bicarbonato es elevada (24 mEq). • Es un sistema abierto: la concentración de cada uno de los dos elementos que lo componen son regulables: el CO2 a nivel pulmonar y el bicarbonato a nivel renal. • La suma de las concentraciones del ácido y de la base no es constante, lo cual aumenta muchísimo su capacidad amortiguadora. La relación existente entre el ácido y la base nos viene dada por la ecuación de Henderson-Hasselbalch: pH = pK + Log [HCO3 ] / [H2 CO3] pH = pK+ Log [ HCO3] / [ PaCO2] o