Chimica Farmaceutica II: chemioterapici antibatterici e chinoloni
Slide di Chimica Farmaceutica II sui chemioterapici antibatterici e i chinoloni. Il Pdf, adatto per lo studio universitario di Chimica, esplora la struttura, il meccanismo d'azione e la resistenza batterica ai chinoloni, con schemi esplicativi.
Mostra di più26 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Chemioterapici Antibatterici
L'altra volta abbiamo parlato dei sulfamidici, della prima classe di chemioterapici antibatterici entrati in terapia, e ancora oggi vediamo impiegati in terapia alcuni di questi. Oggi parliamo di un'altra classe che si è sviluppata successivamente, siamo sempre nell'ambito dei chemioterapici antibatterici di sintesi, quindi molecole che sono state sviluppate esclusivamente per sintesi e non a partire da un prototipo di origine naturale.
Chinoloni
Questi chinoloni hanno in parte soppiantato, sostituito, i sulfamidici. Uno dei motivi per cui oggi i sulfamidici vengono usati meno, è proprio il fatto che i chinoloni e altre classi, sono state sviluppate e hanno dato origine ad alcuni farmaci che hanno caratteristiche migliori e possono essere utilizzati con maggiori vantaggi. Ovviamente anche i chinoloni hanno dei limiti.
La cosa che vedremo è come è avvenuto o sviluppo di questi farmaci, a partire dal prototipo, oggi conosciamo quattro generazioni di chinoloni. Quindi significa gruppi di farmaci che si sono sviluppati uno dopo l'altro e di cui la generazione successiva rappresenta un miglioramento di quello precedente. Se noi seguiamo questo percorso, vedendo quali sono state le modifiche strutturali che sono state apportate per passare da una generazione all'altra, noi avremo la possibilità di fare un quadro, delle sar, che è valido tutt'ora per tutta la classe dei chinoloni.
I chinoloni, vedete dal titolo, che meno frequentemente vengono chiamate oxacine o ossacine. Oxacina sarà il suffisso che noi troveremo nei nomi di quasi tutti i chinoloni. Solo nei primi composti di questa classe il nome è un po' diverso.
Cominciamo a vedere una struttura generale dei chinoloni, ci sono caratteristiche comuni che noi troveremo in tutti i componenti.Chinoloni
Caratteristiche Strutturali dei Chinoloni
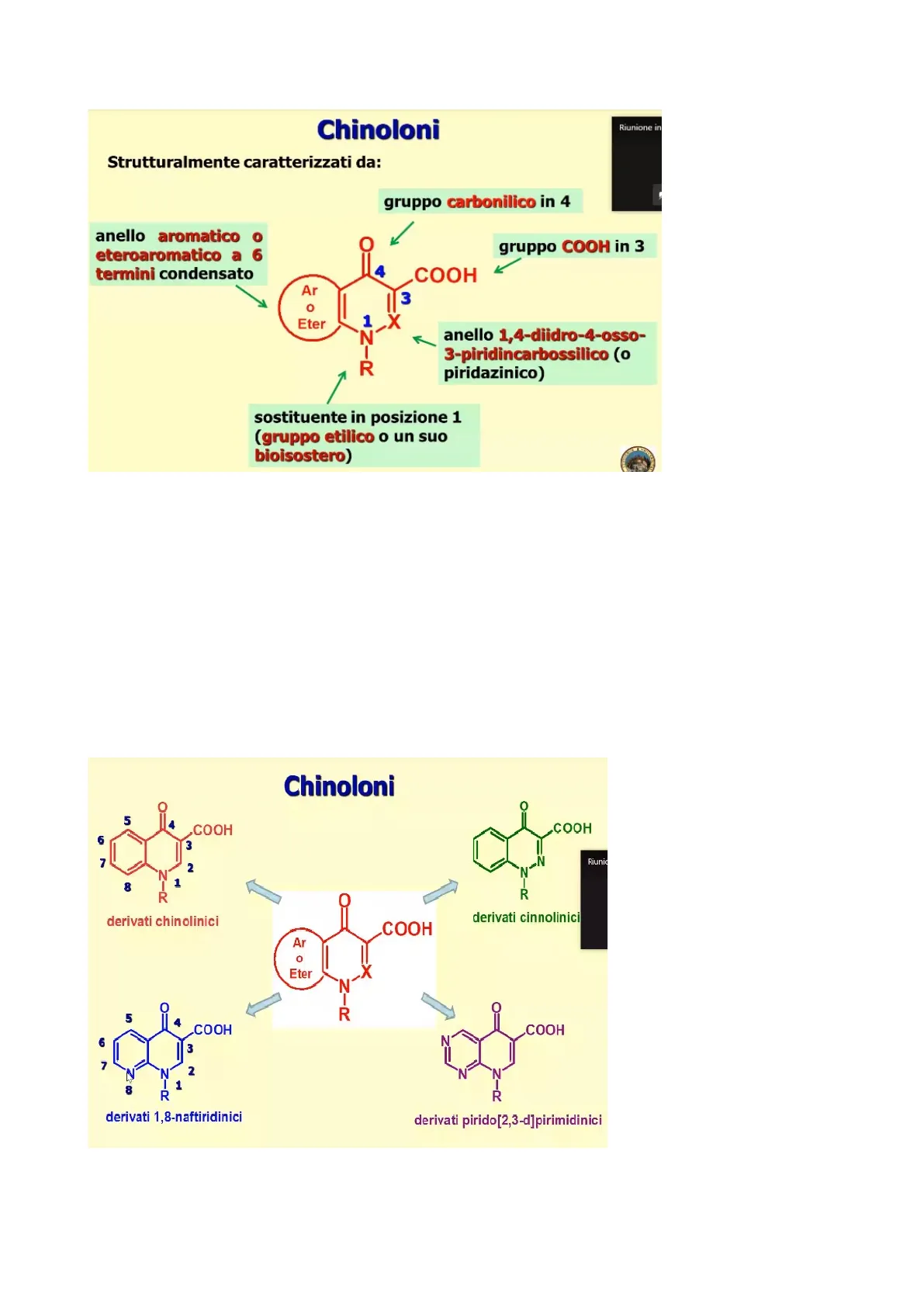
Quello che noi troveremo in tutti i chinoloni è la presenza di questo sistema biciclico, vedete che c'è quest'anello piridincarbossilico, piridinonico, appunto è un anello diidropiridinico che in posizione 4 ha un gruppo carbonilico e in posizione 3 ha un gruppo carbossilico. Questi elementi strutturali li ritroveremo in tutti i chinoloni, così come in tutti i chinoloni troveremo in posizione 1 di quest'anello, un azoto che poi avrà un sostituente caratteristiche di questo sostituente. Condensato a questo primo anello c'è un secondo anello che vedremo, è sempre di natura aromatica e può essere o un arile, cioè un anello benzenico oppure può essere un eteroaromatico in un numero più limitato di casi. Dopodiché vedremo che proprio su questo anello aromatico o etero aromatico a sei termini, condensato al primo vedremo che proprio qui andremo ad inserire dei sostituenti che saranno fondamentali per migliorare il profilo di attività sotto diversi aspetti. Quindi Nell'evoluzione noi vedremo ora come questa struttura di base poi è stata modificata. Parlando del sistema biciclico abbiamo detto che può esserci un anello aromatico o eteroaromatico.
Sistemi Biciclici dei Chinoloni
In questa slide sono raggruppati tutti i vari sistemi B ciclici che noi possiamo trovare nei chinoloni. Quindi, si parte da derivati 1,8-naftiridinici, vedremo che il prototipo di questa classe di farmaci immessi in terapia aveva questo tipo di struttura. 1,8-naftiridinico significa che in posizione 8 noi abbiamo un secondo atomo di azoto e che quindi questo anello condensato è un eteroaromatico. Vedete la numerazione, cominciamo a focalizzare perché poi parleremo dei sostituenti 1, 6, 7 eccetera. Si parte per la numerazione dall'azoto, quello che sarà sempre presente e poi si va in senso antiorario. Quindi in posizione tre abbiamo sempre un gruppo carbossilico, in posizione quattro abbiamo sempre un gruppo carbonilico. Poi vedremo nelle altre posizioni che sostituenti possiamo avere.
Per quanto riguarda il sistema biciclico, oltre al sistema 1,8-naftiridinico, noi possiamo avere dei derivati chinolinici, vedremo poi che molti di quelli più recenti sono derivati chinolinici, perché se pensate alla struttura della chinolina (è un sistema aromatico biciclico, due anelli aromatici con un atomo di azoto). Questi derivati che hanno questa struttura, un secondo anello condensato semplicemente un anello benzenico, non eteroaromatico, sono dei derivati chinolinici ( anche se questa non è una vera e propria chinolina, ma è modificata).
Se invece in posizione 2 c'è un atomo di azoto questo sistema di base sarebbe una cinnolina, e quindi si chiamano derivati cinnolinici. Sono poco frequenti, soprattutto nell' ultima generazione.
Poi c'è quest'altro tipo di sistema biciclico, che è un sistema in cui al primo anello è stato condensato un secondo anello di natura pirimidinica. Vedete una pirimidina e guardate la nomenclatura, sono derivati pirido 2,3 dipirimidinici. Pirido si riferisce al primo anello che in origine era una piridina e poi ovviamente è stata modificata, perché questa porzione non è aromatica. 2,3 si riferisce al fatto che se andiamo a numerare questo anello di origine piridinica, da qui 1,2,3,4,5,6. Quindi gli atomi di carbonio interessate alla condensazione col secondo anello sono quelli in posizione due e tre. L'anello pirimidinico va a condensarsi col primo con il lato D perché si vanno ad indicare con delle lettere. Avremo un lato A,B,C quindi in questo modo questi numeri e queste lettere che sono fra parentesi quadra ci indicano quali lati e quali posizioni dei due anelli sono condensati tra di loro, quindi ci dice esattamente come è costituito il sistema biciclico.
Acido Nalidissico
Possiamo cominciare a vedere il primo termine della nostra classe di farmaci che è l'acido nalidissico.
Vedete che qui il nome non c'entra con quello che vi ho detto prima virgola non c'è il suffisso Oxacina. Noi dobbiamo sempre pensare che dietro un farmaco c'è la ricerca, bisogna avere prontezza dei passaggi che hanno portato a sviluppare una certa classe di farmaci. Qui come vedete siamo all'inizio degli anni 60, eraun periodo in cui ancora molti farmaci venivano trovati casualmente, o venivano trovati perché venivano fatti degli screening a tappeto su determinati gruppi di farmaci. Questo farmaco è stato trovato perché sono andati a testare l'attività antibatterica di intermedi di sintesi della cloridina, che è un farmaco che studieremo come antimalarico. Tra gli intermedi che avevano mostrato attività c'era l'acido nalidissico. Diciamo che non c'è una progettazione razionale. Una volta trovato quest' acido nalidissico, questa scoperta ha aperto la strada allo sviluppo di tutti i chinoloni. Vediamo la struttura, vedete che il sistema biciclo e un sistema 1,8 naftiridinico, già presenta quei due elementi strutturali fondamentali, che sono due elementi farmacoforici, lo vedremo poi (il gruppo carbossile in posizione tre e il gruppo carbonile qui posizione quattro, insieme all'azoto in posizione uno e in questo caso ha come sostituente l'etile).
L'acido nalidissico in un periodo immaginario in cui ancora non erano tantissimi i farmaci antibatterici, si era già avviata la ricerca degli antibiotici però certamente non erano così numerosi come adesso. Quindi anche l'acido nalidissico in quei suoi limiti che ora vedremo, aveva la sua importanza. Quali Sono i limiti dell'acido nalidissico? Innanzitutto in un discorso di spettro d'azione, cioè dei batteri o comunque microrganismi su cui queste molecole risultano attive. Nel caso dell'acido nalidissico, e attivo soprattutto sui Gram (-) e neanche tutti perché il famoso P. Aeuruginosa su cui tante volte ci soffermeremo, Gram negativo responsabile di infezioni anche gravi, spesso ospedaliere, non viene assolutamente attaccato dall'acido nalidissico. E quindi anche i gran positivi erano esclusi dallo spettro di questo farmaco. Un altro problema era che per quanto sia un chemioterapico orale, può essere somministrato per via orale e viene assorbito per via orale, però una volta all'interno dell'organismo c'è un problema di farmacocinetica. Anziché distribuirsi su tutti i tessuti, siccome una molecola molto idrofila, tende ad essere facilmente eliminata per via renale, quindi ha una durata d'azione relativamente breve, ma soprattutto non va a interessare infezioni che possono riguardare i tessuti, come quelli per esempio dell'apparato respiratorio ho dei tessuti molli o della cute. Ma un tipo di infezioni su cui si potevano utilizzare erano le infezioni renali perché, eliminando soprattutto per questa via, chiaramente veniva ad avere una concentrazione sufficiente per svolgere la sua azione sulle vie urinarie. Quindi era fondamentalmente un disinfetta per così dire, delle vie urinarie, antibatterico. Quindi ovviamente da un lato c'era la possibilità di somministrarlo per via orale, non dava gravi effetti tossici quindi era un farmaco interessante. Dall'altra parte c'erano questi limiti che chiaramente hanno stimolato la ricerca, perché a quel punto avendo il prototipo, il modello, i ricercatori sono stati in grado, attraverso una serie di modifiche successive, modifiche strutturali virgola di migliorare il profilo di questi farmaci. Ora una classe abbastanza numerosa di chinoloni.
Questa è una molecola abbastanza idrofila, da che cosa deriva l'drofilia? Soprattutto dal gruppo carbossilico e dal carbonile, gruppo carbossilico a pH fisiologici sarà prevalentemente deprotonato, ionizzato, quindi noi avremo un anione cabossilato che facilmente viene eliminato per via renale. In buona parte viene eliminato tal quale, si ci sono dei metaboliti, poi li vedremo.
Obiettivi delle Ricerche sui Chinoloni
- attività sistemica
- maggiore efficacia antibatterica
- spettro di azione allargato ai batteri Gram(+) e a germi difficili come P. aeruginosa
Attualmente si conoscono quattro generazioni di chinoloni