Tecniche spettroscopiche: interazione tra radiazione elettromagnetica e materia
Slide di Università su Tecniche Spettroscopiche. Il Pdf, utile per lo studio della Chimica a livello universitario, esplora le tecniche spettroscopiche, focalizzandosi sull'interazione tra radiazione elettromagnetica e materia, le transizioni elettroniche UV-Vis e l'interpretazione degli spettri di assorbimento.
Mostra di più28 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Tecniche Spettroscopiche
Le tecniche spettroscopiche si differenziano dalle tecniche spettrometriche di massa per una caratteristica peculiare ovvero un'interazione tra la radiazione elettromagnetica e la materia. Quando la radiazione elettromagnetica incontra la materia, qualunque essa sia, possono accadere due fenomeni:
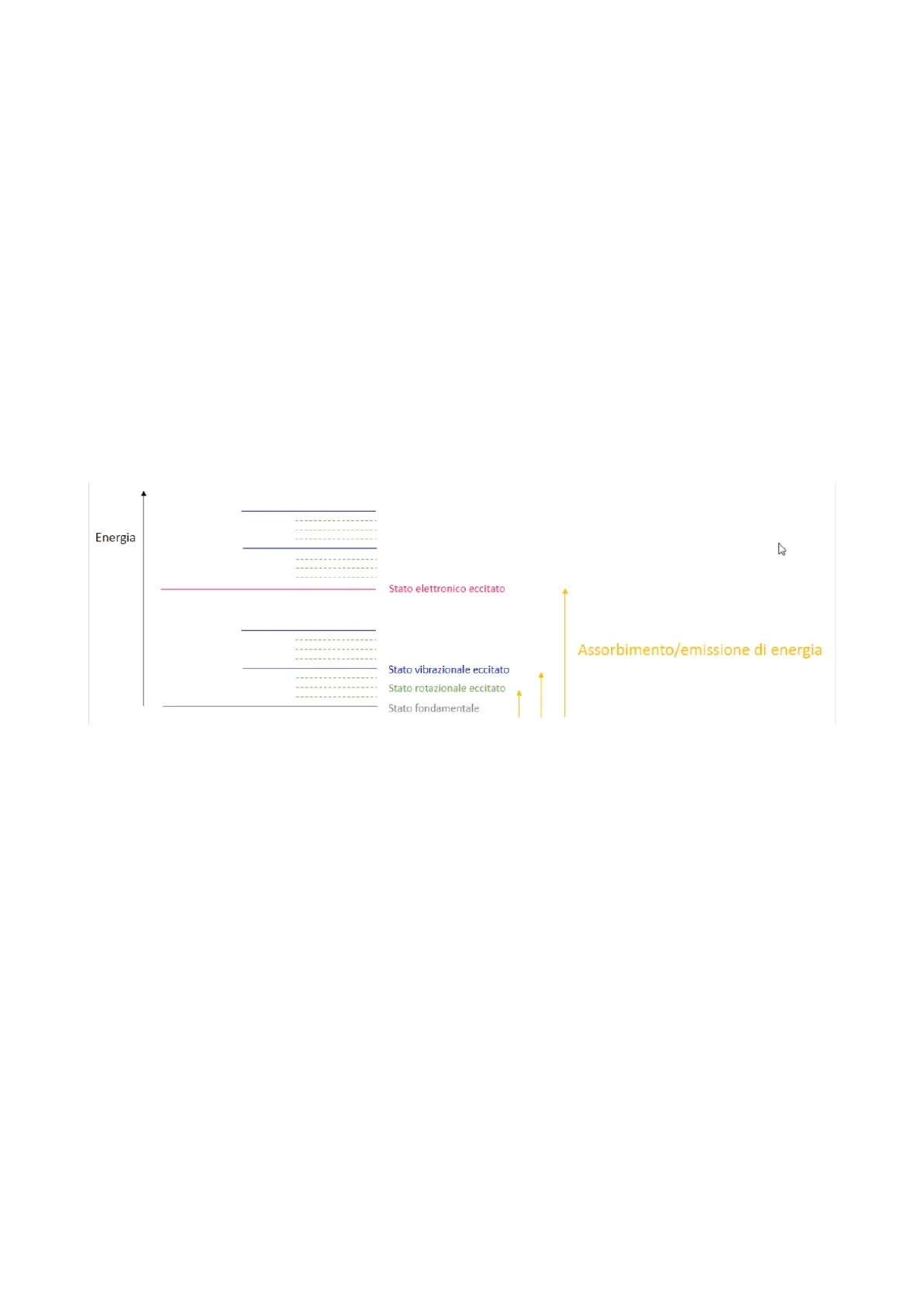
- Il primo riguarda una transizione tra livelli energetici a partire dallo stato fondamentale, in cui la materia si trova in assenza di interazioni, fino ad arrivare ad uno degli stati eccitati che possono essere rotazionali, vibrazionali o elettronici-eccitati. Questo salto energetico avviene perché la materia assorbe la radiazione elettromagnetica che incontra;
- Il secondo riguarda la variazione nella direzione di propagazione della radiazione stessa, fenomeno definito scattering.
Energia Stato elettronico eccitato Assorbimento/emissione di energia Stato vibrazionale eccitato Stato rotazionale eccitato Stato fondamentale
Caratteristiche della Radiazione Elettromagnetica
La radiazione elettromagnetica ha un comportamento dualistico, può essere vista come:
- Onda
- Corpuscolo
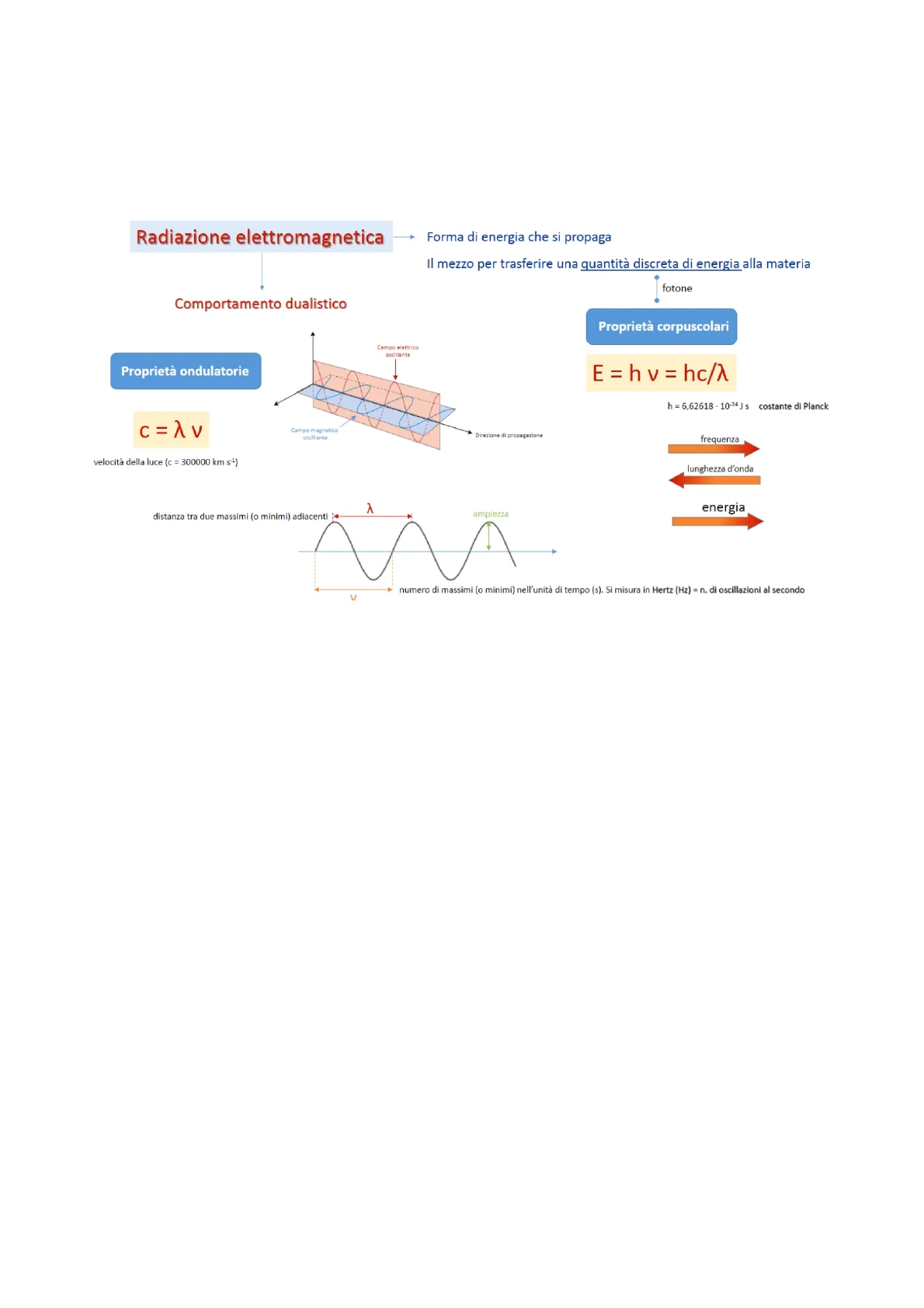
Come onda è costituita da un campo magnetico oscillante ed un campo elettrico oscillante tra di loro perpendicolari che si propagano lungo la direzione di propagazione. Nel vuoto la velocità della luce, della radiazione elettromagnetica è costante, viene indicata come la lettera c ed è data dal prodotto della lunghezza d'onda per la frequenza. Per capire cosa sono la lunghezza d'onda e la frequenza consideriamo l'onda riportata in basso nella slide, che si propaga lungo la direzione di propagazione:
- La lunghezza d'onda (1) corrisponde alla distanza tra due massimi o tra due minimi l'uno adiacente all'altro, essa presenta come unita di misura i sottomultipli del metro, in genere indicata con nanometri o micrometrio La frequenza (v) è definita come il numero di massimi e di minimi presenti in un'unità di tempo che in genere viene misurato in secondi. La frequenza si misura in Herz, il quale per definizione rappresenta il numero di oscillazioni al secondo.
Radiazione elettromagnetica Forma di energia che si propaga Il mezzo per trasferire una quantità discreta di energia alla materia fotone Comportamento dualistico Proprietà corpuscolari Campo elettrico oscillante Proprietà ondulatorie E = h v = hc/2 h = 6,62618 . 10-34 J s costante di Planck frequenza lunghezza d'onda energia distanza tra due massimi (o minimi) adiacenti ampiezza numero di massimi (o minimi) nell'unità di tempo (s). Si misura in Hertz (Hz) = n. di oscillazioni al secondo V In maniera complementare è possibile considerare la radiazione elettromagnetica come un corpuscolo, la luce è considerata una forma di energia che si propaga e costituisce il mezzo per trasferire una quantità di energia fissa alla materia, in particolare essa viene trasferita sotto forma di fotoni. L'energia (E) è uguale al prodotto della frequenza e la costante di Planck (h), ma può essere anche indicata sostituendo alla frequenza la sua espressione derivante dalla definizione della velocità della luce in cui v= c/ 1; per cui l'energia può anche essere espressa come il rapporto della costante di Planck e c/ 1. La frequenza e la lunghezza d'onda sono due caratteristiche della radiazione elettromagnetica inversamente proporzionali, più aumenta la frequenza più diminuisce la lunghezza d'onda e viceversa. Al contrario frequenza ed energia sono direttamente proporzionali, di conseguenza parlare di aumento della frequenza equivale a parlare di un aumento dell'energia. I fotoni nel vuoto hanno tutti la stessa velocità, ma possono avere frequenza diversa, da questa assunzione deriva lo spettro elettromagnetico in cui la radiazione elettromagnetica viene divisa secondo energia o secondo lunga d'onda crescente. Nella tabella riportata è possibile vedere i vari intervalli di lunghezza d'onda a cui sono presenti diversi tipi di radiazioni.
- Partendo dai raggi gamma, raggi a lunghezza d'onda più bassa nell'ordine dei picometri, quindi al del nanometro; essi hanno la minima lunghezza d'onda e la massima energia ( per la proporzionalità inversa prima descritta;
C=AV Campo magnetico oscillante Direzione di propagazione velocità della luce (c = 300000 km s:1)ad essi seguono
- I raggi X ;
poi ci sono
- I raggi UV a loro volta suddivisi in ultravioletto lontano e vicino
- È poi presente l'intervallo di lunghezze d'onda del visibile, chiamato così perché è l'unico intervallo di lunghezze d'onda a cui il nostro occhio è sensibile per la visione dei colori;
- Al visibile segue l'infrarosso a sua volta diviso in vicino, medio e lontano
- Infine, abbiamo le microonde e le onde radio. Queste ultime hanno la lunghezza d'onda maggiore e di conseguenza la frequenza, perciò l'energia, minore.
Lo spettro elettromagnetico può essere rappresentato dall'immagine riportata di seguito a dx. I fotoni possono avere frequenza diversa! Lo spettro elettromagnetico
Tipi di Radiazione e Lunghezza d'Onda
Tipo di radiazione Lunghezza d'onda Raggi gamma < 1 pm Raggi X 1 nm - 1 pm Ultravioletto lontano 200 nm - 1 nm Ultravioletto vicino 400 nm - 200 nm Visibile 750 nm - 400 nm Infrarosso vicino 2,5 um - 750 nm Infrarosso medio 50 um - 2,5 um Infrarosso lontano 100 pm - 50 μm Microonde 0,1 cm - 100 cm Onde radio > 1 mm Energia crescente Lunghezza d'onda crescente Frequenza (Hz) 1024 1022 1020 1018 1016 1014 1012 1010 108 106 104 Raggi gamma Raggi X UV Infrarossi Microonde Onde radio 10-16 10-14 10-12 10-10 10-8 -10-6 10-4 10-2 100 102 104 Lunghezza d'onda (m) Visibile λ. = 390 450 500 550 600 650 700 760 nm In spettroscopia IR si usa spesso il numero d'onda Inverso della lunghezza d'onda espresso in cm-1 espressa in um 1 10000 Numero d'onda = λ 10ª = λ Ciò che distingue una tipologia di radiazione dell'altra è la lunghezza d'onda, quando parleremo di spettroscopia ad infrarossa invece si prende in considerazione non la lunghezza d'onda ma il numero d'onda dato dall'inverso della lunghezza d'onda ed espresso in cm -1. Abbiamo detto che nel vuoto la luce ha sempre la stessa velocità, ma quando essa attraversa un mezzo differente dal vuoto la sua velocità cambia, in particolare diminuisce. La velocità diminuisce ma l'energia di un fotone resta costante, per cui la frequenza direttamente correlata all'energia non varia; ciò significa che quando la luce attraversa un mezzo diverso dal vuoto cambierà la sua lunghezza d'onda. La diminuzione della velocità della luce, in mezzi diversi dal vuoto, viene quantificata con un parametro chiamato indice di rifrazione indicato con la lettera n; esso è uguale al rapporto tra la velocità della luce nel vuoto (c) e la velocità della luce in un mezzo diverso dal vuoto (v). ilvalore di n è sempre maggiore di uno, poiché nel vuoto la velocità sarà sempre maggiore, rispetto alla velocità di quel fotone in qualsiasi altro mezzo.
Indice di Rifrazione e Velocità della Luce
La diminuzione della velocità è quantificata dall'indice di rifrazione n n = c/v c = velocità della luce nel vuoto v = velocità della luce in un altro mezzo mezzo n* aria 1,0003 acqua 1,333 50% saccarosio in acqua 1,420 disolfuro di carbonio 1,628 quarzo 1,544 1,553 diamante 2,417 *misurate utilizzando luce a 589.3 nm n è sempre > 1 essendo la velocità della luce più alta nel vuoto che in qualsiasi altro mezzo. La tabella riportata mostra diversi esempi di mezzi diversi dal vuoto attraversati dalla luce, osserviamo come passando dall'aria all'acqua, l'indice di rifrazione aumenta, fino ad arrivare al massimo nel caso del diamante. Graficamente è possibile esprimere l'indice di rifrazione tramite il grafico riportato. Abbiamo detto che la frequenza è costante, al diminuire dalla velocità della radiazione elettromagnetica diminuirà la lunghezza d'onda, quindi in altre parole diminuisce la distanza tra due massimi e due minimi. Se osserviamo l'onda che si propaga prima nell'aria, poi attraverso il vetro per poi ritornare nell'aria, anche intuitivamente è possibile capire come la lunghezza d'onda nell'aria sia maggiore rispetto a quella del vetro. In qualsiasi mezzo diverso dal vuoto la velocità della luce è V = c/n n è l'indice di rifrazione del mezzo v = 6,0x 1014 Hz A = 500 nm 1 = 6,0 x 1014 Hz λ = 330 nm v = 6,0×1014 Hz λ = 500 nm Ampiezza, A 0 Aria Vetro Aria Distanza NB: la frequenza è una grandezza caratteristica di una vibrazione luminosa e pertanto è indipendente dal mezzo in cui avviene la propagazione. Quando la luce attraversa due mezzi con n diverso, la sua frequenza rimane invariata ma la A cambia
Interazione Radiazione-Materia e Aumento di Energia
Quando c'è un'interazione tra la radiazione elettromagnetica e la materia, quest'ultima può assorbire parzialmente o totalmente la radiazione che incontra, essa assorbe energia, questo assorbimento determina un aumento globale dell'energia interna posseduta dalla materia. Per semplicità consideriamo la materia come una molecola, l'energia da essa posseduta in seguito all'assorbimento della radiazione elettromagnetica aumenta. Una molecola possiede diversi tipi di energia la cui somma determina l'energia completa da essa posseduta. I vari tipi di energia possono essere schematizzati così come riportato in slide:
- L'energia traslazionale rappresenta l'energia necessaria per lo spostamento della molecola nello spazio:
- L'energia rotazionale rappresenta l'energia correlata al moto rotazionale della molecola;
- L'energia vibrazionale fa riferimento alle vibrazioni degli atomi che nel loro insieme costituiscono la molecola, queste vibrazioni, che sono normalmente presenti, sono amplificate dall'assorbimento energetico:
- L'energia elettronica rappresenta l'energia legata alla transizione degli elettroni da livelli energetici più bassi a livelli energetici più alti.
Energia vibrazionale Energia traslazionale energia correlata allo spostamento delle molecole nello spazio, funzione del moto termico della materia energia associata alle vibrazioni degli atomi che costituiscono le singole molecole E = Etrasl + Erot + Evib + Eel Energia posseduta da una molecola Energia elettronica energia legata all'energia di transizione degli elettroni Energia rotazionale energia legata al moto rotazionale di una singola molecola Per sapere se c'è stata un'interazione tra la radiazione e la materia, con un aumento dell'energia interna della molecola, è possibile:
- misurare l'assorbimento di quella radiazione;
- misurare l'emissione di quella radiazione;
- misurare l'emissione di una radiazione dopo che ne è stata assorbita un'altra;
- se la direzione di propagazione della radiazione che incontra la materia cambia e si possono misurare gli effetti di dispersione o scattering.