Materiali per l'ottica: fasi della materia e diagrammi di stato
Slide dall'Università Roma Tre su Materiali per l'Ottica. Il Pdf esplora le fasi della materia e i diagrammi di stato, illustrando come le sostanze cambiano stato in base a pressione e temperatura, con un esempio dettagliato per l'acqua. Questo materiale di Fisica è pensato per studenti universitari.
Mostra di più28 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
MATERIALI PER L'OTTICA
Docente: prof. Armida Sodo Come Raggiungermi:
- e-mail: armida.sodo@uniroma3.it
- stanza: n. 148,Dipartimento di Scienze, Via della Vasca Navale 84
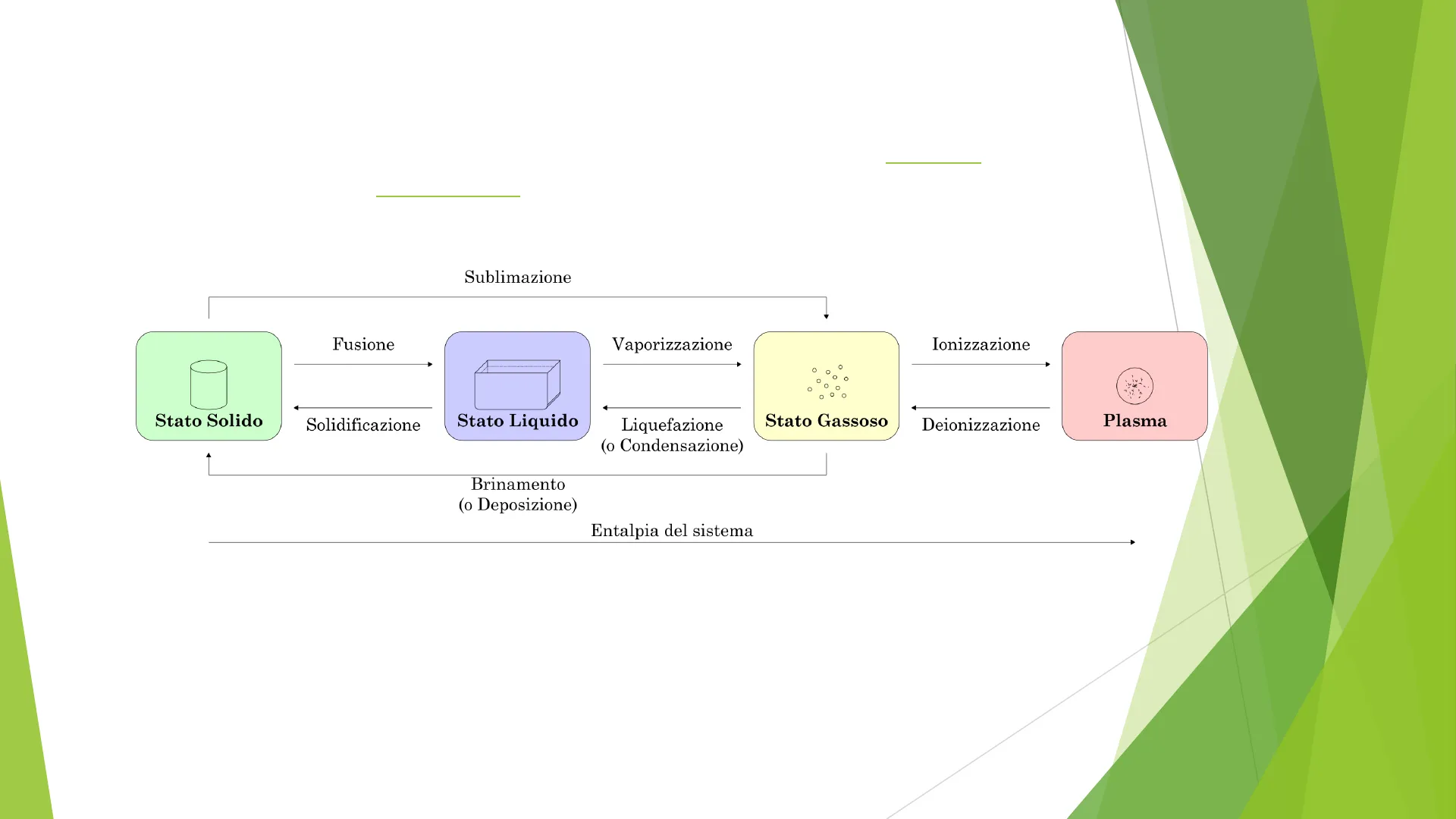
FASI (o STATI) della MATERIA
Con stato della materia (o stato di aggregazione delle molecole) si intende una classificazione convenzionale degli stati che può assumere la materia a seconda delle proprietà meccaniche che manifesta. Una fase è una porzione omogenea di un sistema che ha caratteristiche chimiche e fisiche uniformi.
Sublimazione Fusione Vaporizzazione Ionizzazione Stato Solido Solidificazione Stato Liquido Stato Gassoso Deionizzazione Plasma Liquefazione (o Condensazione) Brinamento (o Deposizione) Entalpia del sistema
Le proprietà della materia nei suoi stati di aggregazione sono essenzialmente determinate dal tipo e dall'entità delle forze di interazione fra le particelle.In condizioni di temperatura e pressione atmosferica le molecole della maggior parte dei gas sono così distanti le une dalle altre da non interagire significativamente tra loro Allo stato liquido e solido (FASI CONDENSATE), le particelle sono più vicine ed interagiscono tra loro. Anche se è possibile descrivere le proprietà dei liquidi e dei solidi, queste non possono essere razionalizzate attraverso semplici equazioni matematiche od un' unica equazione di stato.
TABELLA 13-1 Alcune caratteristiche dei solidi, dei liquidi, e dei gas
Solidi
- Hanno un forma definita (resistono alle deformazioni)
- Sono praticamente incompressibili
- Generalmente hanno una densità maggiore dei corrispondenti liquidi
- Non sono fluidi
- Diffondono solo molto lentamente negli altri solidi
- Le particelle che li costituiscono sono disposte nello spazio in modo regolare, molto vicine le une alle al- tre e possono solo oscillare attorno alle loro posizioni d'equilibrio
Liquidi
- Non hanno forma definita: assumono quella del contenitore in cui si tro- vano
- Hanno un volume definito, sono in- fatti solo moderatamente compressi- bili
- Hanno densità elevate
- Sono fluidi
- Diffondono in altri liquidi
- Le particelle che li costituiscono, che sono piuttosto vicine le une alle altre e formano degli aggregati disordinati, si muovono casualmente nelle tre di- rezioni dello spazio
Gas
- Non hanno forma definita: occu- pano tutto lo spazio disponibile
- Sono comprenssibili
- Hanno densità basse
- Sono fluidi
- Diffondono rapidamente
- Le particelle che li costituiscono, che sono generalmente molto lon- tane le une dalle altre, si muovono molto rapidamente ed in modo ca- suale nelle tre direzioni dello spazio
LIQUIDI
- Forze intermolecolari medie (gas/solidi)
- Ecin intermedia (gas/solidi)
Principali caratteristiche dei liquidi
- Volume proprio e assenza di forma
- Ordine a corto raggio/disordine a lungo raggio
- Densità
- Bassa comprimibilità
- Espansibilità
- Diffusibilità
- Viscosità
- Bagnabilità
VISCOSITA'
La viscosità è la resistenza che un liquido incontra a fluire. Perché un liquido scorra, le sue molecole devono poter scivolare le une sulle altre. In generale, più forti sono le attrazioni intermolecolari, più il liquido è viscoso.
- Le sostanze che hanno un'elevata tendenza a formare legami a idrogeno hanno di solito un'elevata viscosità.
- Analogamente, all'aumentare delle dimensioni dell'area superficiale delle molecole si osserva un aumento della viscosità a causa dell'aumento delle forze di dispersione.
- Più lunghe sono le molecole, più punti di interazione esistono fra di esse e più difficilmente queste scorrono le une sulle altre.
Viscosità e scorrimento
Quando si verifica una condizione di scorrimento relativo tra due elementi di un fluido compare lungo l'area di contatto una forza tangenziale di attrito detta forza di attrito interno con verso sempre contrario a quello della velocità relativa.
1 V2 Velocità V1>V2 Si trova sperimentalmente che il modulo della forza di attrito interno dF dipende da: dF = ndS dv dn dS = area di contatto dv/dn = variazione del modulo della velocità in direzione normale a dS h = viscosità del fluido (dipende dal fluido e dalla temperatura T La viscosità nei liquidi diminuisce con l'aumentare della temperatura (nei gas aumenta con T) Unità di misura: kg/(ms) oppure Poise=0.1 kg/(ms) Esempi: H2O n(T=0℃)~0.018 poise, H2O n(T=20℃)~0.010 poise
Viscosità e temperatura
La viscosita non e costante ma varia con la temperatura: decresce all'aumentare della T
1 × 10-3 0 1 Glycerine Helium 2 Hydrogen 1 × 10-4 0 3 Glycerine 2 1 × 10-2 8 2 Carbon dioxide 1 X 10-5 0 Crude oil (SG = 0.86) Kerosene 1 × 10-6 Benzene Ethyl alcohol = Carbon tetrachloride Gasoline (SG = 0.68) 1 × 10-7 Mercury n 1 -20 0 20 40 60 80 100 120° TEMPERATURE, ℃ 7 2 1 × 10-1 6 4 Castor oil KINEMATIC VISCOSITY, m2/s 1 Air and oxygen Crude oil (SG = 0.86) 2 Mercury 1 × 10-3 Ethyl alcohol 3 Gasoline (SG = 0.68) 1 × 10-4 5 4 -Air Helium 2 Carbon dioxide 1 × 10-5 Hydrogen 8 6 -20 -0 0 20 40 60 80 100 120 TEMPERATURE. ºC ABSOLUTE VISCOSITY, Pa.s 4 Kerosene Aniline Carbon tetrachloride Benzene Water 2 11 1 Water 4 25
TENSIONE SUPERFICIALE
v Le molecole che si trovano all'interno della massa di un liquido sono soggette a forze attrattive da parte delle molecole circostanti in ogni direzione e la risultante di tutte queste forze è nulla. V Al contrario, le forze che agiscono sulle molecole dello strato superficiale non sono distribuite in tutte le direzioni (al di sopra della superficie le molecole sono in numero decisamente minore), per cui la risultante delle forze sarà non nulla e diretta verso l'interno. Le molecole interne si trovano quindi ad avere energia inferiore rispetto a quelle in superficie, per cui il liquido tende a mantenere una superficie esterna minore possibile: la goccia rappresenta la forma geometrica con il più piccolo rapporto tra volume e area superficiale.
12.15 Una molecola sulla superficie del liquido, oltre a essere attratta dalle altre molecole in superficie, è attratta verso l'in- terno del liquido, e questo risulta in una ri- duzione dell'area superficiale. Le molecole in un liquido sono attratte dalle molecole vicine In superficie, l'attrazione non è bilanciata e questo causa la "resistenza" della superficie verso l'estensione Molecole del liquido Le molecole all'interno sono attratte in tutte le direzioni dalle molecole vicine
TENSIONE SUPERFICIALE: Energia e Bagnabilità
La tensione superficiale è l'energia richiesta per aumentare l'area superficiale di un liquido, portando molecole interne alla superficie, cioè ad un livello di energia più elevato. Il fatto che i liquidi tendano a contrarre la loro superficie è una manifestazione della tendenza tipica di ogni sistema ad assumere lo stato con minore contenuto possibile di energia. Si dice che un liquido bagna una superficie se si allarga su di essa formando un film. Tale fenomeno è legato all'equilibrio tra le forze di COESIONE (interazioni tra molecole simili) e le forze ADESIVE (interazioni tra molecole diverse).
12.14 La superficie dell'acqua si com- porta come una membrana in tensione, per- mettendo a questo insetto di "camminare sull'acqua". T
TENSIONE SUPERFICIALE: Definizione Meccanica
In particolare, la tensione superficiale è definibile nel modo più elementare dal punto di vista meccanico come la forza per unità lineare che tiene uniti i lembi di un ipotetico taglio praticato sulla superficie libera del fluido, ovvero: Y = dFs/d l dove d l è la lunghezza di un tratto infinitesimo del taglio e dFs è la forza infinitesima perpendicolare al taglio giacente sulla superficie. Si può ricavare la stessa definizione tenendo conto del fatto che una lamina liquida tende spontaneamente a raggiungere la configurazione di minima superficie, per cui la tensione superficiale si definisce come: Y = dW/d A dove d W è il lavoro elementare compiuto contro le forze di tensione superficiale per ottenere un aumento infinitesimo d A della superficie della lamina.
TENSIONE DI VAPORE
I liquidi ed alcuni solidi (quelli molecolari) subiscono un processo continuo di evaporazione. Le molecola sono trattenute nel corpo del liquido da una forza netta di attrazione verso l'interno. Le molecole con maggiore energia cinetica possono pero sfuggire dalla superfice.
Tipica molecola all'interno del liquido Molecola di superficie
EVAPORAZIONE
Temperatura bassa Temperatura alta Frazione di molecole che possiedono una data energia Energia cinetica minima necessaria affinché le molecole possano sfuggire alla fase liquida cinetica Energia cinetica L'evaporazione è il processo attraverso il quale le molecole sulla superficie di un liquido passano alla fase gassosa. L'energia cinetica delle molecole costituenti il liquido è funzione della temperatura. Minore è la T più bassa è la frazione di molecole che hanno E sufficiente per sfuggire alla fase liquidi, quindi l'evaporazione è più lenta e la tensione di vapore all'equilibrio più bassa. Una molecola che si trova in fase di vapore può urtare la superficie del liquido e rimanerne intrappolata + CONDENSAZIONE.La pressione parziale del vapore sovrastante il liquido aumenta progressivamente e con essa aumenta il numero di molecole presenti in fase vapore e, allo stesso tempo, la probabilita che molecole del vapore collidano con la superficie del liquido e ricondensino in fase liquida.
Molecules in vapor state Molecules undergoing vaporization Molecules undergoing condensation (a) (b) (c) Quando la velocità di condensazione diventa uguale alla velocita di evaporazione si raggiunge uno stato di equilibrio dinamico di equilibrio fra la fase liquida e il vapore
Tensione di vapore e temperatura
La pressione parziale esercitata dal vapore in condizioni di equilibrio con il suo liquido e chiamata tensione di vapore. Lo stato di equilibrio e una funzione di stato: non dipende dalla forma del recipiente, dalla quantita di liquido, ecc. La tensione di vapore di una sostanza dipende dalla temperatura. Al crescere della temperatura aumenta l'energia cinetica molecolare e quindi la tendenza delle molecole a sfuggire dal liquido. Di conseguenza la tensione di vapore aumenta all'aumentare della temperatura.
1000 800 760 mm Hg Pressione (mm Hg) 600 Alcol etilico, p.e. normale 78,5 °℃ 400 Etere dietilico, p.e. normale 34,6 °℃ H2O p.e. normale 100 °C 200 0 -20° 20° 40° 60° 80° 100 ° 120 ° Temperatura (°C)