Materiali per l'ottica: vetri e lenti fotocromatiche, Uniroma3
Slide da Uniroma3.it su Materiali per l'Ottica. Il Pdf, utile per lo studio universitario di Fisica, esplora i materiali ottici, i vetri Crown, Flint, al Titanio e alle Terre Rare, e le lenti fotocromatiche.
Mostra di più29 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Materiali per l'Ottica
Docente: prof. Armida Sodo
Come Raggiungermi
- e-mail: armida.sodo@uniroma3.it
- stanza: n. 148,Dipartimento di Scienze, Via della Vasca Navale 84
E poi c'è .... IL VETRO Ricorda: Il vetro e un solido che non possiede ordine atomico a lungo raggio e che, al riscaldamento, rammollisce progressivamente fino a giungere allo stato fuso.
Vetro di Silice
Formula chimica: SiO2 Nella struttura solida : Si è circondato in media da 4 atomi di O, tetraedro
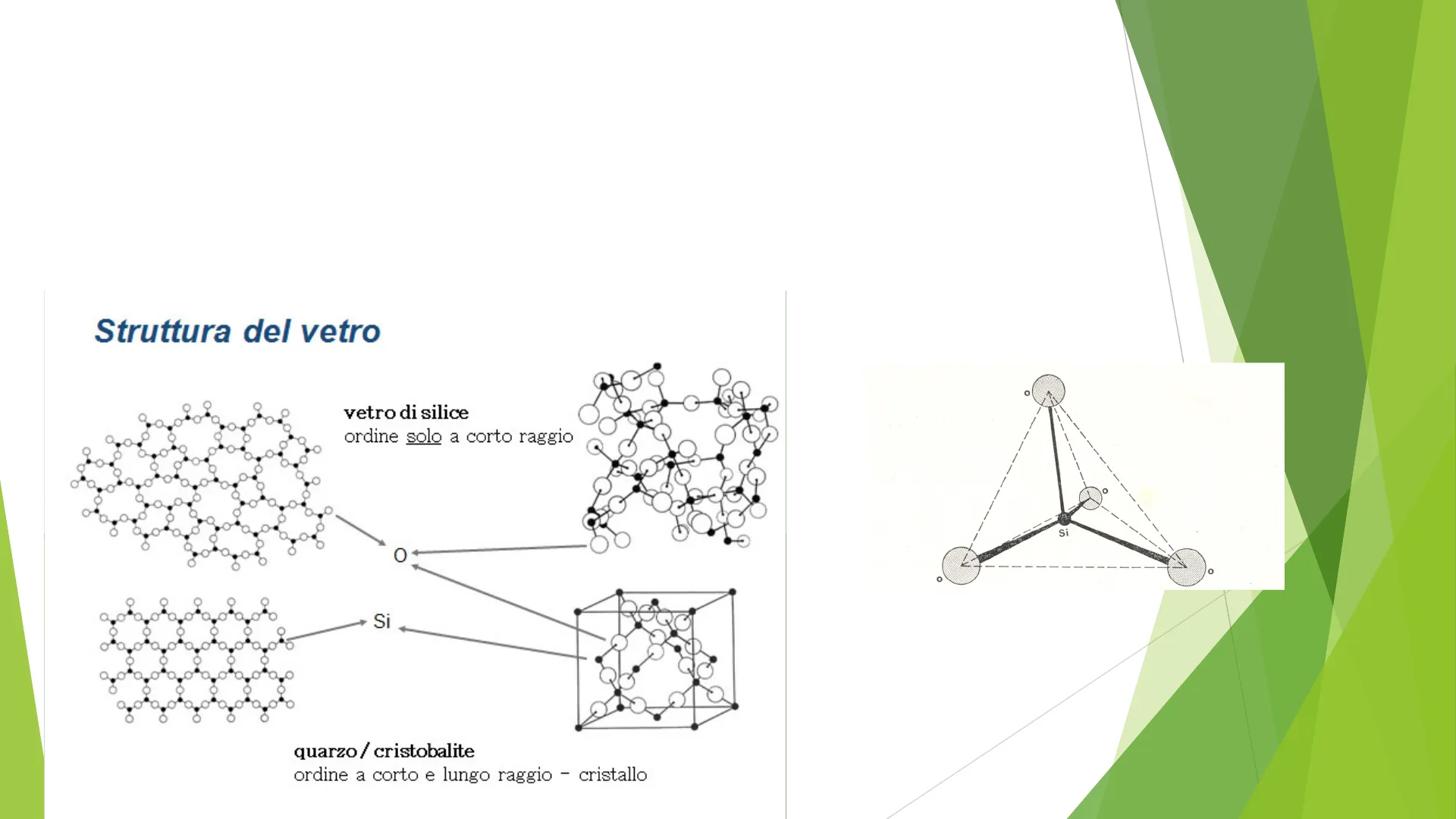
Struttura del Vetro
vetro di silice ordine solo a corto raggio
0 0 Si O Si O Distanza Si-O= 1.6Å
quarzo / cristobalite ordine a corto e lungo raggio - cristallo
I vetri sono caratterizzati da due aspetti:
· strutturale: non hanno ordine a lungo raggio (Long Range Order, LRO)
· dinamico: nella trasformazione da liquido a vetro, cessa la capacita della
struttura di rilassarsi (=scorrelarsi) completamente; la diffusione si arresta e la
viscosita tende all'infinito
-. Gas Intensity Liquid Intensity Glass Intensity . Crystal Intensity 0 angle diffrazione prodotta da una sostanza monoatomica in diversi stati u Proprieta strutturali e dinamiche sono collegate
Il Vetro: Struttura (Silice)
Nei cristalli il modello strutturale si imposta su geometria e simmetria, che sono
indipendenti dal tipo di legame.
Nei vetri, invece, si usano modelli strutturali diversi a seconda del tipo di legami:
· composti covalenti: modello a reticolo disordinato infinito (Continuous Random
Network, CRN)
· composti metallici e ionici: modello a massimo impaccamento locale (Random Close
Packing, RCP)
Nel 1932, Zachariasen tento di spiegare perche alcuni ossidi formano facilmente vetri e altri no, considerando le strutture locali (geometrie di coordinazione) presenti nei corrispondenti cristalli. Dato che i vetri hanno proprietà meccaniche, densità e energie di formazione simili ai corrispondenti cristalli, ipotizzo che le strutture locali fossero uguali nei due casi.
Il Vetro: Struttura (Silice) - Teoria di Zachariasen
Energia devetrificazione vetro cristallo configurazione TEORIA DI ZACHARIASEN (1932) Si arguisce che la differenza in energia tra vetro e cristallo della stessa composizione è molto piccola (altrimenti rapida devetrificazione): metastabilità prossima a stabilità Tipo di legami e motivo strutturale (ad es. tetraedro silicico) devono esser identici perché l'energia interna è funzione essenzialmente della energia di coesione Dato però che non si osserva ordine a lungo raggio, mentre nel cristallo le unità strutturali si ripetono periodicamente nello spazio, nel vetro le unità strutturali di dispongono in modo casuale distorcendo i legami ma mantenendo le "rete" del vetro continua Accordo con i dati XRD ma non spiega l'esistenza di vetri non costituiti da ossidi e non giustifica la presenza di gruppi OH- riscontrati nel vetro
Il Vetro: Struttura (Silice) - Teoria di Porai-Koshits
TEORIA DI PORAI-KOSHITS (1959) La struttura del vetro è costituita da domini nanocristallini (D=10-100Å) Ciascun dominio può anche avere una composizione diversa 1 Zone con regolare disposizione delle unità strutturali collegate da zone esterne altamente disordinate 1 In accordo con i dati XRD, con la presenza di gruppi OH E' compatibile con la presenza di stati vetrosi in materiali non ossidi e con la trasparenza del vetro
Il Vetro: Struttura (Silice) - Confronto Teorie
Confronto tra le due teorie (tra le molte esistenti ... ) a) ৳) Zachariasen Porai-Koshits
Differenze tra Solido Vetroso e Cristallino
- Il passaggio dallo stato liquido al solido avviene in modo progressivo (assenza di calore latente di fusione)
- I materiali vetrosi hanno una velocità di raffreddamento al di sotto del punto di fusione maggiore della velocità di cristallizzazione: gli atomi si "congelano" in posizioni fuori dall'equilibrio
- I materiali che esistono nello stato vetroso sono dotati di viscosità elevata in prossimità del punto di solidificazione
- Lo stato vetroso non è termodinamicamente stabile (il vetro tende ad evolvere verso la cristallizzazione, energeticamente più favorevole).
Caratteristiche Fisiche del Vetro
- La densita e in funzione della composizione: da 2,2 g/cm3 per i vetri al silicio a 4,8 per quelli al piombo.
- Buon isolante, nel vetro in silice, la conducibilita termica e di 1,3 W/m°C.
- Resistenza agli agenti chimici con l'esclusione dell'acido fluoridrico che aggredisce la silice (la corrosione in presenza di acidi e di 0,05 mm/anno e di 0,3 in presenza di basi).
- Elevata trasparenza
- La costante dielettrica relativa nei vetri comuni e inversamente proporzionale alla temperatura.
- Bassa conducibilità elettrica.
Caratteristiche Meccaniche del Vetro
- Bassi valori di elasticità con conseguente notevole fragilita.
- Nei vetri normali non avviene alcuna deformazione prima della frattura (modulo elastico: 70 GPa)
- Elevata resistenza alla compressione 1000MPa § Bassa resistenza agli sbalzi termici.
Produzione del Vetro
Per la realizzazione dei vetri sono necessari:
Formatori
Formatori: formano il vetro senza l'introduzione di altri ossidi (network formers): SiO2, B2O3, P205, AS2O3. Esistono formatori parziali ovvero ossidi che formano il vetro con l'introduzione di almeno un altro ossido: TeO2, SeO2, MoO3, WO3
Modificatori
Modificatori: modificano la struttura del vetro 'rompendo' il network (network modifiers): Na2O, K2O, Li2O, CaO, PbO etc La presenza di network modifiers comporta: - aumento della mobilità e diminuzione della viscosità (diminuzione della temperatura di formazione del vetro) - modifica delle proprietà del vetro a seconda della composizione
Stabilizzanti
Stabilizzanti: Hanno la proprietà di rendere il vetro stabile migliorandone la resistenza meccanica e chimica. Modificando le proprietà basilari degli ossidi che formano il reticolo con essi è possibile intervenire su caratteristiche che vanno dalla viscosità alle proprietà elettriche, dalla resistenza chimica al coefficiente di dilatazione (K2O, Na2O, BaO). Alcuni ossidi svolgono la doppia funzione, a seconda della composizione , sia di vetrificanti che di stabilizzatori; si tratta di ossidi intermedi. (Al2O3, ZnO, TiO2 )
Produzione del Vetro: Processo di Fusione
La silica (SiO2) fonde a 1800℃ , per ottimizzare il processo di fusione vengono aggiunti i cosiddetti fondenti, che hanno la proprietà di abbassare il punto di fusione sino a 800℃ e allungando l'intervallo di solidificazione. I più utilizzati sono il carbonato di sodio e il carbonato di potassio. Nella fase di produzione possono venire aggiunti anche:
Affinanti
Affinanti: Sono composti riducenti (triossido d'arsenico, nitrati alcalini e nitrati d'ammonio) che a temperature elevate (1200℃) liberando bolle di ossigeno che, risalendo nel fuso, assorbono le bollicine che incontrano sino a raggiungere la superficie. Attraversando le stratificazioni di vetro a diversa densità, le bolle svolgono anche un'azione di omogeneizzazione del fuso. > hanno l'essenziale funzione di favorire l'eliminazione delle inclusioni gassose (bolle) della massa del vetro in fusione.
Decoloranti
Decoloranti Fe e Cr sono sempre presenti anche se in piccolissima quantità. Il vetro, così ottenuto, non e perfettamente trasparente ed incolore quindi si utilizza una miscela di elementi come il selenio, il cobalto e terre rare. Per ottenere un vetro "bianco" (incolore) i coloranti devono essere totalmente assenti anche in piccolissime concentrazioni. Quando volutamente utilizzati provocano un assorbimento selettivo per le diverse lunghezze d'onda dello spettro visibile, conferendo quindi al vetro una tinta del colore complementare.
Produzione del Vetro: Coloranti e Opacizzanti
Ma quando i coloranti sono volutamente utilizzati, provocano un assorbimento selettivo per le diverse lunghezze d'onda dello spettro visibile, conferendo quindi al vetro una tinta del colore complementare. Abbiamo perciò
Coloranti
Coloranti: affinche i vetri risultino colorati e necessario introdurre sostanze minerali contenenti metalli di transizione che nella loro forma ionica conferiscono varie colorazioni al campione. FeO per avere tonalita verde- azzurra, Fe203 per verde bottiglia, Cu2O per il rosso, CuO per blu-verde, CrO3 per verde-giallo, CoO per blu scuro, Au per il rosso rubino.
Opacizzanti
Opacizzanti: sono formati da fosfati o fluoruri di Na o Ca, da talco o da ossido di stagno che persistono nella massa vetrosa sotto forma cristallina diminuendone la trasparenza, in quanto la riflessione della luce avviene all'interno del vetro stesso, a causa del diverso indice di rifrazione delle sostanze opacizzanti cristalline.
Vetri più Comuni
vetro SiO2 Na2O K2O CaO B2O3 Al2O3 altri proprietà 1 silicico 99.5+ Difficile da lavorare, ottime resistenza shock termici 2 96% silice 96.3 <0.2 <0.2 2.9 0.4 3 sodico-calcico 71-73 12-14 10-12 0.5-1.5 MgO, 1-4 Facile da lavorare 4 silicato di piombo 63 7.6 6 0.3 0.2 0.6 PbO, 21 MgO, 0.2 Facile da fondere e fabbricare 5 alto piombo 35 7.2 PbO, 58 6 borosilicato 80.5 3.8 0.4 12.9 2.2 Bassa espansione e buona resistenza shock termici 7 bassa perdita elettrica 70 0.5 28 1.1 PbO, 1.2 8 alluminoborosilicato 74.7 6.4 0.5 0.9 9.6 5.6 B2O, 2.2 Durabilità chimica 9 bassi alcali (vetro E) 54.5 0.5 22 8.5 14.5 Compositi a fibre di vetro 10 alluminosilicato 57 1 5.5 4 20.5 MgO, 12 11 vetro-ceramica 40-70 10-35 MgO, 10-30 TiO2, 7-15
Tabella 13.1: Composizione e Caratteristiche Vetri Commerciali
Tabella 13.1 Composizione e caratteristiche di alcuni comuni vetri commerciali Composizione (% in peso) Tipo di vetro SiO2 Na20 CaO Al2O3 B2O3 Altri Caratteristiche e applicazioni Silice fusa >99.5 Alte temperature di fusione, bassis- simi coefficienti d'espansione ter- mica (resistente agli shock termici) Silice 96% 96 4 Resistenza chimica ed agli shock (Vycor™M) termici - vetreria di laboratorio Borosilicato 81 3.5 2.5 13 Resistenza chimica ed agli shock (Pyrex TM termici - vetreria per forno Contenitore 74 16 5 1 4MgO Basse temperature di fusione, lavo- (calce - sodico) rabile facilmente, durevole Fibre di vetro 55 16 15 10 4MgO Facilmente estrudibile in fibre compositi in vetroresina Vetro per lenti 54 1 37PbO, 8K2O Alta densità ed alto indice di rifra- zione - lenti ottiche Vetro-ceramici (Pyroceram™M) 43.5 14 30 5.5 6.5TiO2, 0.5As2O3 Fabbricabile facilmente; resistente; resistente agli shock termici vetreria per forno