Proprietà Colligative delle soluzioni: abbassamento tensione vapore
Slide sulle Proprietà Colligative. Il Pdf illustra le proprietà colligative delle soluzioni, come l'abbassamento della tensione di vapore e l'innalzamento ebullioscopico, con formule matematiche. Questo documento di Chimica per l'Università è ideale per comprendere i concetti fondamentali della chimica fisica delle soluzioni.
Mostra di più30 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
PROPRIETA' COLLIGATIVE
Sono proprietà delle soluzioni, che non dipendono dalla natura chimica del soluto, ma solo dalla concentrazione di particelle (m=molalità moli di soluto/Kg di solvente); i indica n moli totali di ioni liberati nel caso di elettroliti (per NaCl in acqua i=2).
- l'abbassamento della tensione di vapore;
- l'innalzamento del punto di ebollizione (innalzamento ebullioscopico) ATeb = Keb x m x i;
- l'abbassamento del punto di congelamento (abbassamento crioscopico) ATc = Kc x m x i;
- la pressione osmotica : TV = nRT x i, detta equazione di van't Hoff, nella quale nt è la pressione osmotica, V il volume, T la temperatura assoluta, n il numero di moli e R la costante universale dei gas.
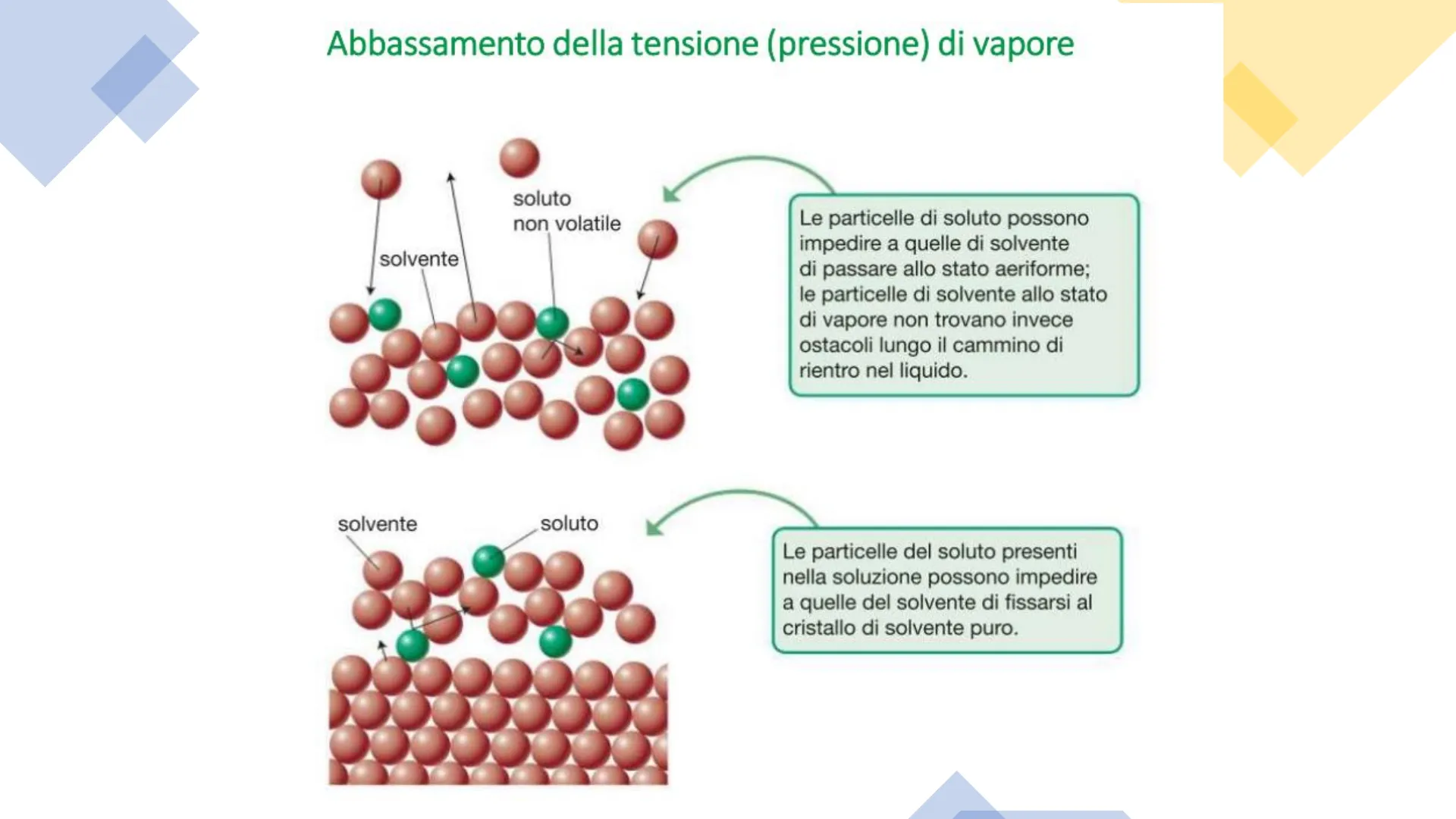
Abbassamento della tensione (pressione) di vapore
soluto non volatile solvente Le particelle di soluto possono impedire a quelle di solvente di passare allo stato aeriforme; le particelle di solvente allo stato di vapore non trovano invece ostacoli lungo il cammino di rientro nel liquido.
solvente soluto 1 Le particelle del soluto presenti nella soluzione possono impedire a quelle del solvente di fissarsi al cristallo di solvente puro.
ABBASSAMENTO DELLA TENSIONE DI VAPORE: LA LEGGE DI RAOULT
Solvente da solo Solvente + soluto Pº - PA PºA XB Una sostanza che ha pressione di vapore non misurabile si dice non volatile. Le p di vapore dei solventi puri sono sempre più alte delle p di vapore delle loro soluzioni. Tanto più soluto c'è, tanto più si abbassa p di vapore. PA = XAPºA XA frazione molare del solvente PºAp di vapore del solvente puro La legge è valida se le interazioni solvente- solvente sono identiche a quelle soluto- solvente. Le soluzioni che seguono la legge di Raoult si chiamano SOLUZIONI IDEALI AH =0
Solution vapor pressure Vapor pressure of pure solvent uJos 0 1 Mole fraction of solvent Xsolvent
Tensione di vapore delle soluzioni
LEGGE di RAOULT: Nelle soluzioni liquide ideali le pressioni parziali dei costituenti volatili della soluzione sono proporzionali alla loro frazione molare nella miscela liquida Pi = x; PIº Pi: tensione di vapore del componente i nella soluzione = pressione parziale del componente i nella miscela gassosa P.º: tensione di vapore del componente i puro x: frazione molare del componente i nella soluzione Legge di Dalton: P = PA + PB Legge di Raoult: PA= XAPA° PB = XBPB P = XAPA° + XBPB
Tensione di vapore
Po PAtes Pa = Xg På Xx~1 x=0 *A-0 *g=1
Ricordando che
x0= 1-x1 possiamo riarrangiare P=Poro nel seguente modo: P= Po(1-x1)=Po -Pox1 Po-P = Pox] => AP= Por1 L'abbassamento della pressione di vapore del solvente (AP) di una soluzione è direttamente proporzionale alla frazione molare del soluto (x1).
Innalzamento della temperatura di ebollizione
La presenza di un soluto in una soluzione innalza la temperatura di ebollizione della soluzione. L'innalzamento ebullioscopico rappresenta la differenza tra la temperatura a cui inizia a bollire la soluzione e la temperatura di ebollizione del solvente puro. ATeb= Keb.m keb è caratteristica di ogni solvente ed è pari al numero di gradi di cui è innalzato il punto di ebollizione del solvente per la presenza di una mole di soluto non volatile in 1000g di solvente.
Abbassamento della temperatura di congelamento
Quando un soluto è aggiunto ad un solvente, la soluzione così ottenuta congela ad una temperatura inferiore a quella del solvente puro. AT _= ker ; m Dove k_ è la costante crioscopica caratteristica di ciascun solvente ed è indipendente dalla natura del soluto e m è la concentrazione della soluzione espressa in molalità.
Costanti crioscopiche ed ebullioscopiche
Come esempio vengono riportate le temperature di ebollizione e di fusione di alcuni solventi e le relative K.
| solvente | nome convenzionale | Teº | Ke | Tfº | Kf |
| H2O | acqua | 100,0 | 0,512 | 0,00 | 1,86 |
| CH 3COCH3 | acetone | 56,5 | 1,73 | - | - |
| C2H5OH | etanolo | 78,5 | 1,22 | -117,3 | 1,99 |
| CH3COOH | acido acetico | 118,9 | 3,10 | 16,6 | 3,90 |
| C6H6 | benzene | 80,1 | 2,53 | 5,5 | 4,90 |
| CHCI3 | cloroformio | 61,2 | 3,63 | - | - |
| (C2H5)20 | etere etilico | 34,5 | 1,19 | - | - |
| C6H5NO2 | nitrobenzene | - | - | 5,7 | 6,90 |
| C6H12 | cicloesano | 80,7 | 2,69 | 6,5 | 20,0 |
| canfora | canfora | 178,4 | 37,7 |
Fig.03.2-2 Costanti crioscopiche ed ebullioscopiche per i solventi più comunemente usati nelle determinazione del peso molecolare e relative temperature di fusione e di ebollizione.
Esercizio
Calcola la temperatura di ebollizione di una soluzione di glucosio, C6H1206 (MM = 180,16), ottenuta sciogliendo 50,00 g del composto in 750,00 g di acqua.
Esercizio
Calcola la massa (g) di glicerolo, C3H803 (MM = 92,097) che, sciolto in 150,00 mL di acqua provoca un innalzamento ebulliscopico di 0,12 ℃.
Esercizio
Una soluzione contiene 150,00 g di glucosio (MM= 180,16) in 1,00 kg di acqua. Calco- la la temperatura di congelamento della soluzione.
Esercizio
Quale percentuale (% p/p) di glicol etilenico, C2H6O2 (MM = 62,07) deve contenere una soluzione acquosa anticongelante per automobile perché il suo punto di congelamento sia tsol sz = - 8,0 ℃.
Pressione Osmotica
Concetto di diffusione. La diffusione in sistemi non omogenei è il trasferimento netto di particelle da regioni a più alta concentrazione verso quelle a più bassa concentrazione. Essa avviene molto velocemente nelle miscele gassose, più lentamente nei sistemi liquidi anche se i componenti si muovono sempre dalle regioni a concentrazione maggiore verso quelle a concentrazione minore. La diffusione in fase liquida è alla base dell'osmosi, che si verifica quando in una soluzione liquida alcuni componenti possono diffondere liberamente rispetto ad altri che non possono farlo. OSMOSI : si verifica quando due soluzioni a concentrazione diversa vengono separate da una membrana semipermeabile. Questa membrana si lascia attraversare dal solvente ma non dal soluto, la cui diffusione quindi non può avvenire liberamente. La membrana, infatti, funziona come un setaccio lasciandosi attraversare solo dal solvente e da soluti di piccole dimensioni (ioni, urea, amminoacidi, glucosio). Non esistono membrane permeabili solo al solvente LIQUIDI Il solvente (H2O) passa dalla soluzione meno concentrata a quella più concentrata.
Soluzione meno concentrata Soluzione più concentrata H,O Membrana semipermeabile Situazione Iniziale Situazione Finale
Pressione Osmotica
soluzione solvente puro soluto membrana
- Conseguenza dell'osmosi si ha un passaggio di solvente dalla soluzione meno concentrata a quella più concentrata e il dislivello che si osserva tra i due rami del recipiente quando viene raggiunto l'equilibrio rappresenta la pressione osmotica della soluzione.
- La pressione osmotica può quindi anche essere definita come quella pressione che bisogna esercitare sulla soluzione più concentrata per evitare il trasferimento netto di solvente dalla soluzione più diluita a quella più concentrata. LIQUIDI
Pressione osmotica Quando si raggiunge l'equilibrio, tra i due rami si crea un dislivello di pressione idrostatica che è la pressione osmotica
Osmotic pressure
Applied pressure needed to prevent volume increase Pure solvent -Solution Net movement of solvent Semipermeable membrane Solute molecules Solvent molecules I I I I I A I B C I
Pressione osmotica di una soluzione
la pressione osmotica di una soluzione è proporzionale alla sua molarità T . V=n . R . T i vari parametri hanno il medesimo significato che avevano nell'equazione di stato dei gas ideali T= n . R . T V T = M . R . T Per 2 stati diversi della soluzione vale TV1 M2V2 T1 T2 Volumi uguali di soluzioni diverse ma aventi tutte la stessa pressione osmotica contengono alla stessa temperatura lo stesso numero di particelle di soluto.
Pressione osmotica
Soluzione ipertonica Soluzione isotonica Soluzione ipotonica
La membrana cellulare si comporta come una membrana semipermeabile
A) in una soluzione ipotonica, la cellula as- sorbe acqua per osmosi e si gonfia; B) in una soluzione ipertonica, l'acqua esce dalla cellula, che si raggrinzisce. O 0 O O D A Bla "tonicità" delle soluzioni in biologia Le proprietà osmotiche sono importanti nei fenomeni biologici: tutte le cellule sono circoscritte da membrane semipermeabili, attraverso le quali passano molecole o ioni piccoli, ma non le proteine. Alcune membrane biologiche sono estremamente selettive, tanto da poter discriminare, per esempio, tra ioni Na+ (raggio ionico 0,97 Å) e ioni K+ (raggio ionico 1,33 Å). Sono ovviamente importanti anche nel campo medico: per esempio, quando si effettua una fleboclisi (immissione di soluzioni nutritive o medicinali nel sangue), è necessario che la soluzione sia isotonica (cioè con la stessa II) con quella del sangue; se essa fosse ipotonica (minore II per la soluzione), il solvente tenderebbe a penetrare nelle cellule fino anche alla rottura della membrana; se invece fosse ipertonica (II maggiore), il solvente uscirebbe dalle cellule, facendole raggrinzire e contrarre fino ad impedirne l'attività.
Flusso di liquido nel capillare
All'entrata del capillare arterioso la pressione idrostatica del sangue è maggiore della pressione osmotica del liquido interstiziale, ciò provoca fuoriuscita di liquido dal capillare. Man mano che il sangue scorre nel capillare la pressione idrostatica si abbassa all'estremità venosa del capillare la pressione osmotica del sangue è maggiore della pressione idrostatica del sangue e si ha il rientro del liquido nel capillare venoso
Cellule dei tessuti Pressione osmotica Pressione osmotica Estremità arteriosa del capillare Estremità venosa del capillare Pressione del sangue Pressione del sangue Liquido interstiziale Pressione di filtrazione Pressione di riassorbimento Il punto in cui il flusso di liquido in entrata è maggiore di quello in uscita è il limite tra il capillare arterioso e quello venoso
Comportamento della cellula in soluzione
Cellula in soluzione isotonica. Se una cellula si trova in una soluzione con una concentrazione di soluti pari a quella intracel- lulare, il flusso di acqua in uscita è pari a quello in entrata (situazione definita "equilibrio dinamico"). Cellula in soluzione ipertonica. Una cellula posta in una soluzione con una concentrazione di soluti maggiore rispetto a quella intracellulare, vedrà i suoi fluidi uscire all'esterno e "raggrinzirà" (shrinkage). Cellula in soluzione ipotonica. Se una cellula è posta in una soluzione ipo- tonica, l'acqua tenderà a entrare nella cellula e a gon- fiarla (swelling). Se la soluzi- one è eccessivamente ipo- tonica, la cellula si gonfierà fino a "scoppiare".