Il trasporto di membrana, reticolo endoplasmatico e giunzioni cellulari
Documento di Biologia sul trasporto di membrana, che include endocitosi ed esocitosi, e descrive la struttura e le funzioni del reticolo endoplasmatico (RER e REL), dei perossisomi e dei vacuoli. Il Pdf dettaglia le diverse tipologie di giunzioni cellulari (strette, ancoranti, comunicanti) e la comunicazione cellulare, arricchito da schemi e diagrammi.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Il trasporto di membrana
Il processo d'importazione e di esportazione di sostanze di grandi dimensioni è detto: endocitosi ed esocitosi; durante questi processi le sequenze sono definite vie di endocitosi ed esocitosi.
Sono formate da diversi organuli, tra cui il reticolo endoplamatico, l'apparato di golgi, gli endosomi e i lisosomi.
Reticolo endoplasmatico
È un organulo disposto vicino al nucleo, infatti viene detto peri nucleare. In molte cellule come, ad esempio, nei linfociti T è l'organulo più voluminoso.
È formato da diversi acculi appiattiti e tubuli delimitati da membrana; lo spazio interno del reticolo viene detto lume (contiene enzimi che catalizzano diverse reazioni chimiche).
Il reticolo può essere suddiviso in:
- Ruvido o granulare: perche hanno dei ribosomi attaccati alla membrana. Possono essere di due tipi: legati alla membrana esterna del RER che sintetizzano tutte le glicoproteine, le proteine transmembrana e quelle destinate ad essere secrete. Oppure liberi ovvero che sintetizzano le proteine destinate a rimanere dentro la cellula. Entrambi i RER sono strutturalmente e funzionalmente identici.
- Transizione: permette di far avvenire il passaggio dal RER al REL quando avviene la gemmazione delle vescicole.
- Liscio: ha diverse funzioni, come sintesi dei lipidi e degli steroidi, degradazione del glicogeno, detossificazione di sostanze dannose per l'organismo (alcool etilico, farmaci) ed infine sequestro e rilascio di ioni calcio +.
Le funzioni del REL
- Sintesi dei lipidi e degli steroidi: partono dal precursore che è il colesterolo nelle vie metabolche nella biosintesi degli ormoni steroidei.
- Detossificazione: per organismo tramite certi enzimi che non sono sempre presenti, ad esempio per la degradazione dell'alcol etilico: il rel non sempre riesce a demolirlo fino ai 21 anni (concentrazione di alcol determinata dalla quantità di alcol che viene assunta), perche il tasso di assorbimento dipende da diversi fattori: concentrazione , quantità, quantità del cibo presente nello stomaco e la modalità di assunzione.
Le funzioni del RER
- Sintesi delle proteine di membrana e glicosilazione: la traduzione degli mRNA inizia sempre nel citoplasma e possono restare nel citoplasma oppure essere trasferite nel nucleo nei mitocondri, nei plastidi e nei parossismi. Possono essere trasferite attraverso la co-traduzione: avviene un segnale di riconoscimento (sequenza segnale) -> indirizza il complesso ribosomi-mRNA a traslocare sul RER, oppure post-tradizionale sequenza segnale post tradizionale-> indirizza la proteina sintetizzata verso il compartimento di destinazione.
Le sequenze segnale sono formate da 30 aminoacidi 6-12 aminoacidi idrofobici seguiti da aminoacidi carichi negativamente.
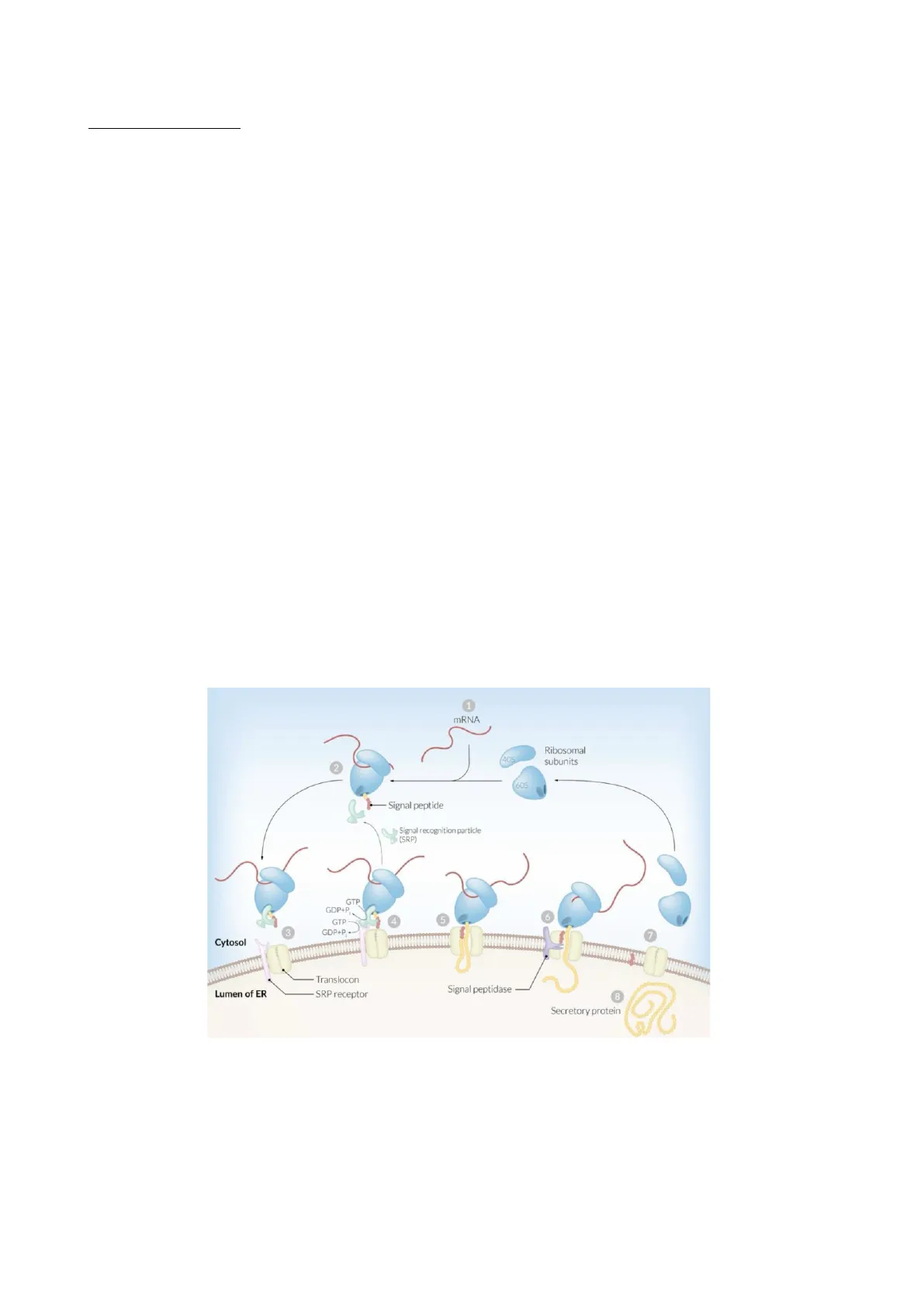
La co-traduzione inizia la traduzione-> citoplasma, la presenza della sequenza segnale -> i ribosomi si associano al RER dove continueranno la sintesi della specifica proteina. Quando il peptide segnale emerge dal ribosoma viene riconosciuto e legato dalla particella SRP. Il legame blocca la sintesi proteica e il complesso ribosomi-mRNA-SRP, si lega ad un recettore di SRP sulla membrana del RER.
Il legame permette l'adesione del complesso ad una struttura multiproteica detta traslocone forma un canale attraverso cui avviene la traslocazione della proteina nascente all'interno del lume del RER.
Il peptide segnale viene tagliato via durante la traduzione da una peptidasi del segnale, la proteina matura è rilasciata nel lume del RER immediatamente dopo la sua sintesi.
1 mRNA Ribosomal subunits 405 2 60S Signal peptide Signal recognition particle (SRP) GTE GDP+P 6 GTP 4 6 3 GDP+P - Cytosol Translocon Signal peptidase Lumen of ER SRP receptor 8 Secretory protein
Apparato di Golgi
L'apparato è stato descritto nel 1906 da Camillo Golgi in una cellula nervosa, inizialmente viene evidenziato come un reticolo peri nucleare chiamato "apparato reticolare interno". Oggi viene chiamato Apparato di Golgi.
La sua morfologia di questo è formata da cisterne appiattite non intercomunicanti tra di loro, perché ognuna di esse ha una costituzione indipendente con all'interno i propri enzimi. È presente in tutti gli organismi eucarioti e dal punto di vista morfologico è formato da tre zone:
- CIS: verso il nucleo
- Trans: verso esterno della cellula
- Porzione mediana: è una porzione centrale che connette il cis e trans
Il movimento delle proteine avviene sempre da cis verso al trans.
- Le reti del Trans-golgi (TNG) è lontano dal RER, qui le proteine e i lipidi lasciano il golgi in vescicole di trasporto chegemano continuamente.
- Cisterne mediane costituiscono le cisterne interposte tra le cs e trans, dove avviene il processamento delle proteine.
- Cis-golgi (CGN) continu al RER da cui riceve microvescicole, contenti lipidi e proteine che si fondono con le cisterne:
Secretory vesicles TEM TRANS Polarità del movimento INTERMEDIE icles riving from ER CIS
Le funzioni
Ha la capacità di ricevere, elaborare e smistare le glicoproteine, le riceve tramite le microvescicole di trasporto provenienti dal reticolo endoplsmatco di transizione. Con lo stesso meccanismo di trasporto il Golgi trasmetterà le proteine negli altri compartimenti cellulari.
La glicosilazione è una modificazione post-tradizionale, in cui vengono aggiunti zuccheri alla catena peptidica. Nel golgi ha una seuenzialita ed avviene tramite certi organuli: ha delle cisterne chiuse, degli enzimi specifici che marcano una certa posizione nel golgi. Ciò permette di dare una certa sequenzialità degli eventi che si svolgono a carico delle proteine.
Gli enzimi modificano le glicoproteine, rimuovendo o aggiungendo gruppi glucidici durante il loro trasporto nelle cisterne in direzione cis-trans, passando da cisterne in cisterne.
Il passaggio delle proteine ha dei problemi perché le cisterne sono divise, per questo esistono due teorie:
- le vescicole, ritengono che la cellule producono delle vescicole gemmando da una parte del golgi all'altra insieme alle proteine che devono glicosilare ma si trascinerebbero delle parti del lume. Per questo pensano che ci sia anche una via retrograda che riportano gli enzimi al proprio posto.
- la prima cisterna del cis prende le proteine del reticolo endoplasmatico le glicosila matura e trasformano la costerna successiva fino alla cisterna possibile terminale e da li ci sarà la gemmazione della cisterna trans che permetterà le diverse destinazioni.
A secondo del tipo di modifiche avranno una destinazione diversa: ai lisosomi, vescicole di secrezione o alla membrana plasmatica; ciò va in base all'involucro delle vescicole che hanno.
gradiente di ph neutro debolmente acido acido proteina solubile residente nell'ER gruppo - vescicolare tubulare KDEL recettore del KDEL vuoto VIA IN AVANTI - 0 D recettore.&C del KDEL rivestimento di COPI JA) VIA DI RECUPERO rivestimento di COPI proteina residente- nell'ER ER (B) pile reticolo del Golgi del Golgi cis reticolo del Golgi trans
Nell'immagine possiamo vedere che facendo un movimento anterogrado è presente un gradiente di ph (neutro in prossimità del reticolo endoplasmatico poi subisce un'acidificazione nelle cisterne del golgi) che serve alla cellula per capire se attuare la via anterogrado e retrogrado.
Avviene la glicosilazione perché:
- Ripiegamento: funzione
- Protezione: aumenta la solubilità della molecola proteica (maggiore stabilita)
- Permette la cellula di scartare le proteine che non sono correttamente ripiegate. Il principio di riconoscimento avviene sulla base della presenza o meno di un particolare residuo di glucosio sulla struttura glucosidi a
- Riconoscimento ad adesione cellula-cellula e cellula-matrice
Avvengono due diversi tipi di glicosilazione che differiscono per meccanismo d'azione, compartimento cellulare in cui si svolgono e il sito d'attacco delle catene glucosidiche:
proteina Lo secretoria rivestimento di COPIIN-GLICOSILAZIONE O-GLICOSILAZIONE meccanismo di azione Generico nel RER (aggiunta serie di zuccheri), proteina-specifico nel Golgi (modifiche degli zuccheri). altamente specifico, L'aggiunta riguarda un singolo carboidrato alla volta; solitamente il numero di zuccheri legati durante questo processo è limitato a pochi residui. compartimento cellulare ha inizio nel RER, prosegue (in modo proteina-specifico) nel Golgi Apparato del Golgi (cis) sito di attacco catena glucidica standard a livello dell'atomo di azoto di una catena laterale di asparagina zuccheri legati a livello dell'atomo di ossigeno delle catene laterali di serina, treonina o idrossilisina. (N-linkage) Asparagine CH,OH HN -O H N-C-CH2-C O C=o HO NH 0=C N-acetylglucosamine linked to asparagine ČH3 (O-linkage) Serine CH,OH -0 HO Q-CH2-CH Č=o H NH N-acetylgalactosamine linked to serine CH3
Glicosilazione N-linked
Nel RER inizia con 'aggiunta di un precursore contenete 14 residui glucidici all'atomo di azoto di una asparagina. Il precursore contiene molecole di glucosio, mannosio e N-acetil glusammina.
L'enzima glicosiltransferasi attacca la catena oligosaccarida alla catena latarele di una asparagina facente parte di una certa sequenza-> è un qualsiasi amminoacido diverso dalla prolina.
La proteina modificata:
- Assume la corretta conformazione
- Viene traslocata nell'apparato di Golgi dve verranno rimossi i residui di mannosio
- Subirà altre glicosilazioni però O-Linked
NH NH2 ER ruvido CITOSOL dolicolo dolicolo P LUME DELL'ER Asn catena polipeptidica in crescita Asn oligosaccaride legato a lipide Glycoprotein z S/T N-glycans O-glycans lumen/extracellular cytosol OH -0-0-
Glicosilazione O-Linked
È un processo altamente specifico che marca le proteine per la loro destinazione futura, tutto ciò si svolge completamente nell'apparato di Golgi (cisterna CIS).
L'inizio avviene quando gli zuccheri vengono legati al peptide a livello dell'atomo di ossigeno delle catene laterali di serina, treonina o idrossilisina
Per questa glicosilazione valgono le due teorie dette in precedenza per il fatto che le cisterne sono tutte separate.
Dopodiché sappiamo che c'è un'intenso traffico di vescicole all'interno delle cellule, ma non è caotico poiché vengono guidati da:
- Elementi del citoscheletro che fungono da binari
- Organizzato in modo da mantenere le dimensioni della membrana, perche ogni volta che le vescicole si staccano portano via una parte dell membrana che dopo viene rigenerata per non far perdere la funzionalità del'organulo.
- Strutturato in modo da garantire il ruolo di veicolatori delle vescicole
Le vescicole possono contenere del materiale nel proprio lume che viene riversato nel lume dell'organo bersaglio.
CITOSOL LUME COMPARTIMENTO DONATORE FUSIONE - COMPARTIMENTO BERSAGLIO GEMMAZIONE
Formazione della vescicola con la clatrina
La membrana nel suo stato è stabile, infatti la sua alterazione avviene attraverso l'operazione degli enzimi che applicano su di essa una forza.
Il primo enzima che applica questa forza è la clatrina, che è composta da 6 catene polipeptidiche (tre grandi e tre piccole), esse formano delle strutture note come triskelion, essendo delle strutture rigide quando si polimerizzano formano elementi esagonali e pentagonali. Questi elementi poi si agganceranno alla membrana, fino ad arrivare alla formazione di una struttura circolare, che in seguito subirà una strozzatura e si staccherà dalla membrana formando la vescicola stessa.
Esterno della cellula Citoplasma Molecole di clatrina Vescicola rivestita Una sostanza specifica si lega a proteine recettore Fossetta rivestita Le molecole di clatrina (una proteina) rivestono la faccia citoplasmatica della membrana in una fossetta rivestita. I contenuti inglobati dall'endocitosi vengono a trovarsi all'interno di una vescicola rivestita di clatrina.