Amminoacidi: struttura, elastina e amminoacidi non proteici
Slide dall'Università San Raffaele su Amminoacidi. Il Pdf, utile per lo studio universitario di Biologia, esplora la struttura generale degli amminoacidi, la formazione dell'elastina e il ruolo degli amminoacidi non proteici come ornitina e citrullina.
Mostra di più35 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Università San Raffaele Roma
Docente Sara Baldelli
Lezione AmminoacidiU Università San Raffaele Roma Sara Baldelli
Struttura amminoacidi
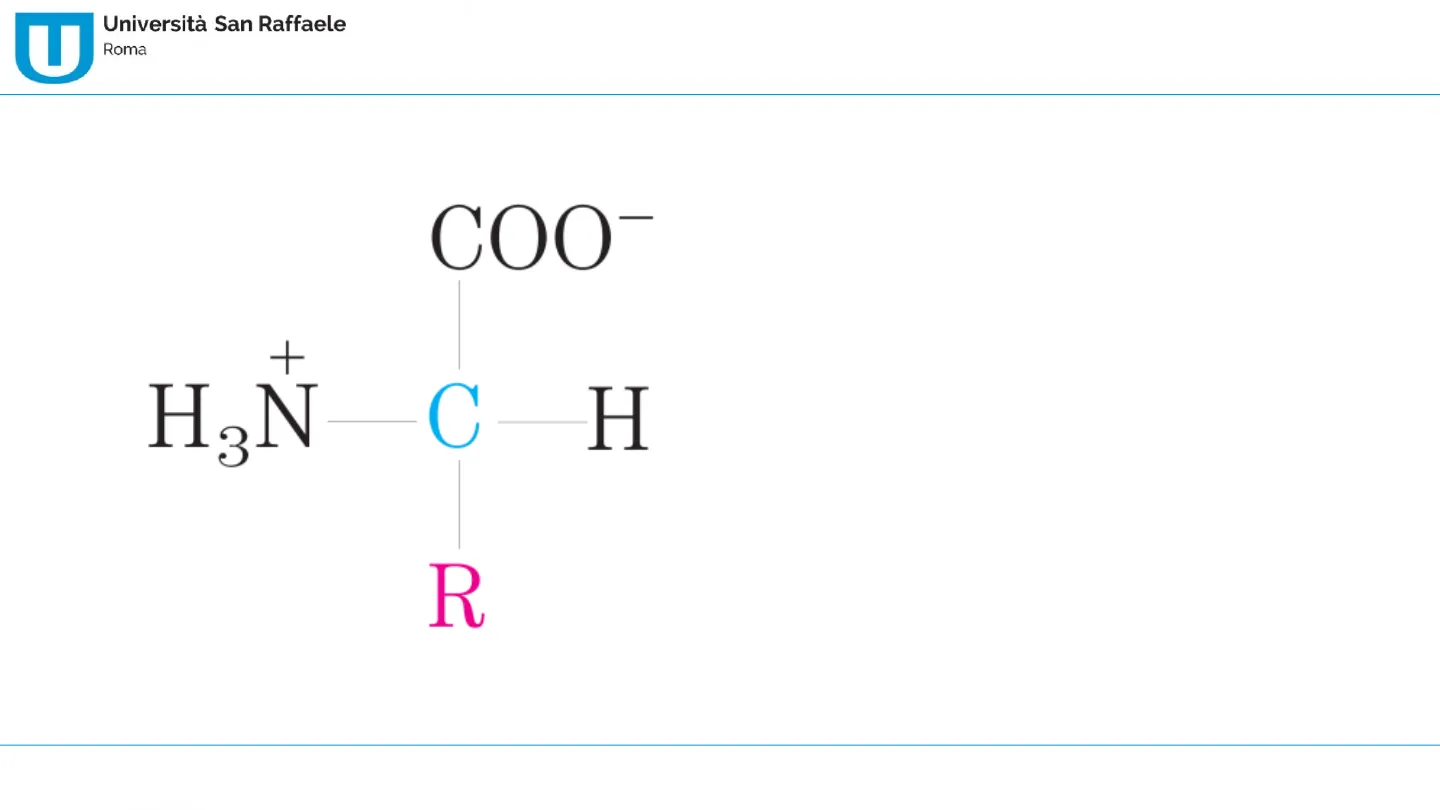
COO- HON 3 + C H R Struttura generale di un a-amminoacido R = catena laterale Il carbonio alfa è il cuore della struttura degli amminoacidi. Attorno a questo carbonio vi sono quattro sostituenti: il gruppo carbossilico in alto, il gruppo amminico a sinistra, l'idrogeno a destra e la catena laterale R in basso (diversa per ogni amminoacido). Amminoacidi 2 di 35U Università San Raffaele Roma Sara Baldelli
Struttura amminoacidi
Dato che gli amminoacidi si legano tra loro per formare catene lineari (chiamate peptidi se sono corte o proteine se superano le 50 unità), è più conveniente disegnarli con una proiezione di Fischer modificata ponendo a sinistra il gruppo amminico e a destra il gruppo carbossilico. In questo modo la catena laterale R si trova in alto e l'idrogeno in basso come è mostrato qui sotto per un L-amminoacido generico. Infatti, invertendo tra loro due sostituenti in una struttura di Fischer, si inverte la configurazione, quindi si devono fare due inversioni per tornare alla configurazione iniziale iniziale. COOH HUN-C-H : R COOH invertire He COOH H HON-C-COOH invertire HeR H2N-C-H R L-amminoacido struttura 3D L-amminoacido proiezione di Fischer standard D-amminoacido H R HẸN-C-COOH 1 R L-amminoacido proiezione di Fischer modificata Amminoacidi 3 di 35U Università San Raffaele Roma Sara Baldelli
Tabella degli amminoacidi
Tabella degli aminoacidi
| Sigla a tre lettere | Sigla a una lettera | Nome |
| Gly | G | Glicina |
| Ala | A | Alanina |
| Val | V | Valina |
| Leu | L | Leucina |
| Ile | 1 | Isoleucina |
| Met | M | Metionina |
| Cys | C | Cisteina |
| Pro | P | Prolina |
| Phe | F | Fenialalanina |
| Trp | W | Triptofano |
| Tyr | Y | Tirosina |
| Thr | T | Treonina |
| Ser | S | Serina |
| Asn | N | Asparagina |
| Gin | O | Glutammina |
| Asp | D | Acido aspartico o Aspartato |
| Glu | E | Acido Glutamminico o Glutammato |
| His | H | Istidina |
| Lys | K | Lisina |
| Arg | R | Arginina |
Amminoacidi 4 di 35U Università San Raffaele Roma Sara Baldelli
Amminoacidi cellulari
- Gli amminoacidi presenti nella cellula possono essere:
- il prodotto di idrolisi delle proteine (aAA proteici o standard; aAA rari o non standard)
- o metaboliti liberi (AA non proteici).
Amminoacidi 5 di 35U Università San Raffaele Roma Sara Baldelli
AA proteici o standard
COO- COO- + H3N 3 C H H C + NH3 CH3 CH3 L-Alanine D-Alanine Le proteine naturali sono costituite esclusivamente da L-amminoacidi Amminoacidi 6 di 35U Università San Raffaele Roma Sara Baldelli
Famiglie di AA
- Gli amminoacidi che costituiscono le proteine sono 20 e sono codificati a livello del genoma. Sulla base della natura della catena laterale sono raggruppati in 5 famiglie:
- ALIFATICA NON POLARE
- POLARE NON CARICA
- AROMATICA
- CARICA POSITIVAMENTE (BASICA)
- CARICA NEGATIVAMENTE (ACIDA)
Amminoacidi 7 di 35U Università San Raffaele Roma Sara Baldelli
Non polare, gruppo R alifatico
COO- I COO- COO- 1 H C + H2N CH 2 H2C CH2 Glycine Alanine Proline COO- COO- I + H3N-C-H H-C-CH3 CH CH3 CH3 CH2 1 CH3 Leucine Isoleucine H3N-C-H 1 CH2 CH2 I S 1 CH3 Methionine COO- I H3N-C-H CH / CH3 CH3 Valine COO" I + + I H3N-C-H CH2 H3N-C-H H3N-C-H 1 CH3 H Amminoacidi 8 di 35U Università San Raffaele Roma Sara Baldelli
Polari, gruppo R non carico
COO" COO COO" H3N-C-H I H3N-C-H CH 2OH H-C-OH - CH2 1 SH Serine Threonine Cysteine coo- coo" - 1 H3N-C-H 1- H CH2 N. I H H N. s H HỌC H 2N O Cisteina Ossidazione + 2 H+ + 2 e" Riduzione S H CH2 H CH2 H N H H Cisteina Cistina CH2 1 C CH2 1 HỌC H2N O C H Asparagine Glutamine S Amminoacidi 9 di 35 H3N-C-H - H3N-C-H I CH3U Università San Raffaele Roma Sara Baldelli
Gruppo R aromatico
COO I -H COO" COO" I + H3N-C-H H3N-C-H 1 CH2 CH2 CH2 C=CH NH OH Phenylalanine Tyrosine Tryptophan Phe, Trp non polari Tyr polare non carica Amminoacidi 10 di 35 I + H3N-C-HU Università San Raffaele Roma Sara Baldelli
Gruppo R positivamente carico
COO" 1 COO- + H3N-C-H CH2 CH2 I CH2 CH2 I C-NH CH 11 C-N H CH2 I + NH3 + C=NH2 NH2 Lysine Arginine COO- H3N-C-H + 1 H3N-C-H -H CH2 1 CH2 1 CH2 1 NH Histidine Amminoacidi 11 di 35U Università San Raffaele Roma Sara Baldelli
Gruppo R negativamente carico
COO- 1 H3N-C-H + COO" H3N-C-H I + CH2 COO- CH2 2 I CH2 2 1 COO" Aspartate Glutamate Amminoacidi 12 di 35U Università San Raffaele Roma Sara Baldelli
AA raggruppati in base al gruppo R
Non polari
- Glicina Gly G
- Alanina Ala A
- Valina Val V
- Leucina Lau L
- Isoleucina Ile I
- Metionina Met M
Polari, non carichi
- Serina Ser S
- Prolina Pro P
- Treonina Th T
- Cisteina Cys C
- Asparagina Asn N
- Glutammina Gin Q
Aromatici
- Fenilalanina Phe F
- Tirosina Tyr Y
- Triptofano Trp W
Carichi positivamente
- Lisina Lys K
- Istidina His H
- Arginina Arg R
Carichi negativamente
- Acido aspartico Asp D
- Acido glutammico Glu E
Aminoacidi. Tabella degli aminoacidi raggruppati in base alle caratteristiche chimiche del gruppo R. E' indicato il nome per esteso ed i codici internazionali a tre lettere ed a singola lettera. Amminoacidi 13 di 35U Università San Raffaele Roma Sara Baldelli
Altre classificazioni degli AA
Altre classificazioni degli amminoacidi:
- AA acidi glutammato e aspartato: (AA monoamminodicarbossilici)
- AA basici arginina e lisina (AA diamminomonocarbossilici) istidina (anello imidazolico)
- AA solforati cisteina e metionina
- AA aromatici fenilalanina, triptofano e tirosina
Amminoacidi 14 di 35U Università San Raffaele Roma Sara Baldelli
Tavola degli AA
Idrofobicità 0.067 5,97 3 2.77 1 -Punto isoelettrico Gly G Glicina Alifatico Contiene Gruppo OH Sigla a 3 lettere Asp D Ac. Aspartico o Aspartato 115 133 1 6.01 Il gruppo NH dell aa è legato alla catena laterale dello stesso. Contiene gruppo COO- 57 75 Glu E Aromatico Contiene gruppo NH3 Ac. Glutammico o Glutammato 71 89 129 147 2.3 5,97 -1.7 7,59 R His NH H NH H Senza carica netta H V Valina Istidina 99 117 137 155 2.2 5.98 1.1 5.47 2.5 5.48 -0.75 5,87 -2.7 5,41 -4.6 9,74 Leu Met Phe Thr Asn Lys L M Metionina F T N K Leucina Fenilalanina Treonina Asparagina Lisina 113 131 131 149 147 165 101 119 114 132 128 146 3,1 6.02 0.17 5,07 0,29 6.48 1.5 5.89 0.08 5.67 -1.1 5,68 -2.9 5,65 -7,5 10,76 Ile Cys C Pro Trp Ser Gln Arg I P W S Q Isoleucina Cisteina Prolina Triptofano Tirosina Serina Glutammina R Arginina 113 131 103 121 97 115 186 204 163 181 87 105 128 146 156 174 Idrofobici Idrofilici Amminoacidi 15 di 35 57 75 Contiene Zolfo Contiene il gruppo: C G Glicina Nome -2.6 3.22 Ala A Alanina Massa monoisotopica del residuo amminoacidico R OH H-N H Val Massa monoisotopica 0,067 5,97 Gly Sigla ad 1 lettera HN Tyr YU Università San Raffaele Roma Sara Baldelli
AA non standard
Derivano dai 20 AA standard mediante modificazione chimica post-traduzionale H HO-C- - CH2 I H2C CH-COO" N H H 4-Hydroxyproline Proteine della parete cellulare, delle cellule vegetali e nel collageno non idrossilazione: scorbuto H3N-CH2 -CH -CH2-CH2 -CH -COO" I OH 1 + NH3 collageno 5-Hydroxylysine CH3-NH-CH2-CH2-CH2-CH2-CH-COO" miosina + NH3 6-N-Methyllysine Amminoacidi 16 di 35U Università San Raffaele Roma Sara Baldelli
AA non standard
COO" "OOC-CH-CH2-CH-COO" I + NH3 nella protrombina y-Carboxyglutamate non carbossilazione: emorragia HSe -CH2-CH-COO" I + NH3 dalla serina nella glutatione perossidasi Selenocysteine Amminoacidi 17 di 35U Università San Raffaele Roma Sara Baldelli
Elastina
H3N COO" CH I (CH2)3 H3Ň NH3 CH-(CH 2)2 (CH2)2-CH - "OOC coo" N (CH2)4 - CH H3Ň COO" Desmosine L'elastina è una proteina caratteristica della pelle, alla quale garantisce elasticità e possibilità di deformarsi quando sottoposta a tensioni meccaniche. Prodotta dai fibroblasti del derma, l'elastina è in grado di allungarsi e contrarsi entro certi limiti senza subire danni. In termini quantitativi, rappresenta il 2% del peso del derma; secreta sotto forma di monomero (tropoelastina), concorre insieme alle microfibrille di fibrillina a formare un reticolo tridimensionale che conferisce alla cute una certa elasticità. Deriva dall'unione di quattro residui di lisina ad un anello aromatico Amminoacidi 18 di 35U Università San Raffaele Roma Sara Baldelli
AA non proteici
H3N-CH2-CH2-CH2-CH-COO" + NH 3 Ornithine H2N-C-N-CH2-CH2-CH2-CH-COO" - O H + NH3 Citrulline H 1+ H-N. H CH2 HERE. C- O H Componente dell'acido pantotenico 8-alanine L'ornitina è un derivato aminoacidico con caratteristiche basiche, prodotto dal nostro organismo a partire dall'arginina, per intervento dell'enzima arginasi con conseguente produzione di urea. L'ornitina rappresenta l'aminoacido iniziatore del ciclo dell'urea, grazie alla possibilità di interagire con il carbamil-fosfato (veicolatore del primo gruppo amminico) per originare citrullina, la quale - fuoriuscendo dalla matrice mitocondriale - potrà garantire il proseguimento del ciclo stesso. Amminoacidi 19 di 35U Università San Raffaele Roma Sara Baldelli
Gruppi ionizzabili
Tutti gli amminoacidi contengono almeno due gruppi ionizzabili, il gruppo carbossilico ed il gruppo amminico (a-imminico per la prolina). Questi gruppi sono acidi e basi deboli, quindi non completamente ionizzati. Per il fatto di possedere sia un gruppo acido che un gruppo basico gli amminoacidi sono definiti molecole ANFOTERE. O= HO-C H2N-C-H I R Nonionic form 0 ǁ "0-C + H3N-C-H I R Zwitterionic form Amminoacidi 20 di 35U Università San Raffaele Roma Sara Baldelli
Isomeri De L
(A) (B) R R CH,OH CHỊOH H H H H Co 03 Co COOH NH2 NH2 COOH CHO OH OH CHO D-amminoacido L-amminoacido D-gliceraldeide L-gliceraldeide Quando il gruppo R e quello amminico sono legati al Co, quest'ultimo possiede 4 differenti gruppi funzionali (-NH2, -COOH, -Re un atomo di idrogeno) e viene definito stereocentro. Quando ciò accade la molecola presenta attività ottica e sulla base di questa attività, si possono identificare gli L-a-amminoacidi e gli D-a- amminoacidi. I primi sono quegli amminoacidi che compongono tutte le proteine degli esseri viventi e per tale motivo vengono definiti amminoacidi proteinogenici. Gli D-a-amminoacidi possono talvolta entrare a far parte delle glicoproteine di alcuni esseri viventi, come accade nei procarioti, ma generalmente hanno funzioni differenti e per tale motivo rientrano nel grande gruppo di amminoacidi non proteinogenici. Amminoacidi 21 di 35