Produzione di aminoacidi: struttura, stereoisomeria e processo industriale
Documento di Università sulla produzione di aminoacidi, esplorando la struttura e la stereoisomeria degli alfa-aminoacidi. Il Pdf, utile per lo studio della Chimica a livello universitario, approfondisce la presenza degli aminoacidi come ioni dipolari e il processo di produzione industriale, con focus sul ciclo dell'acido citrico e l'influenza della biotina.
Mostra di più16 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Richiami Teorici sugli Aminoacidi
Struttura Generica di un Alfa-Aminoacido
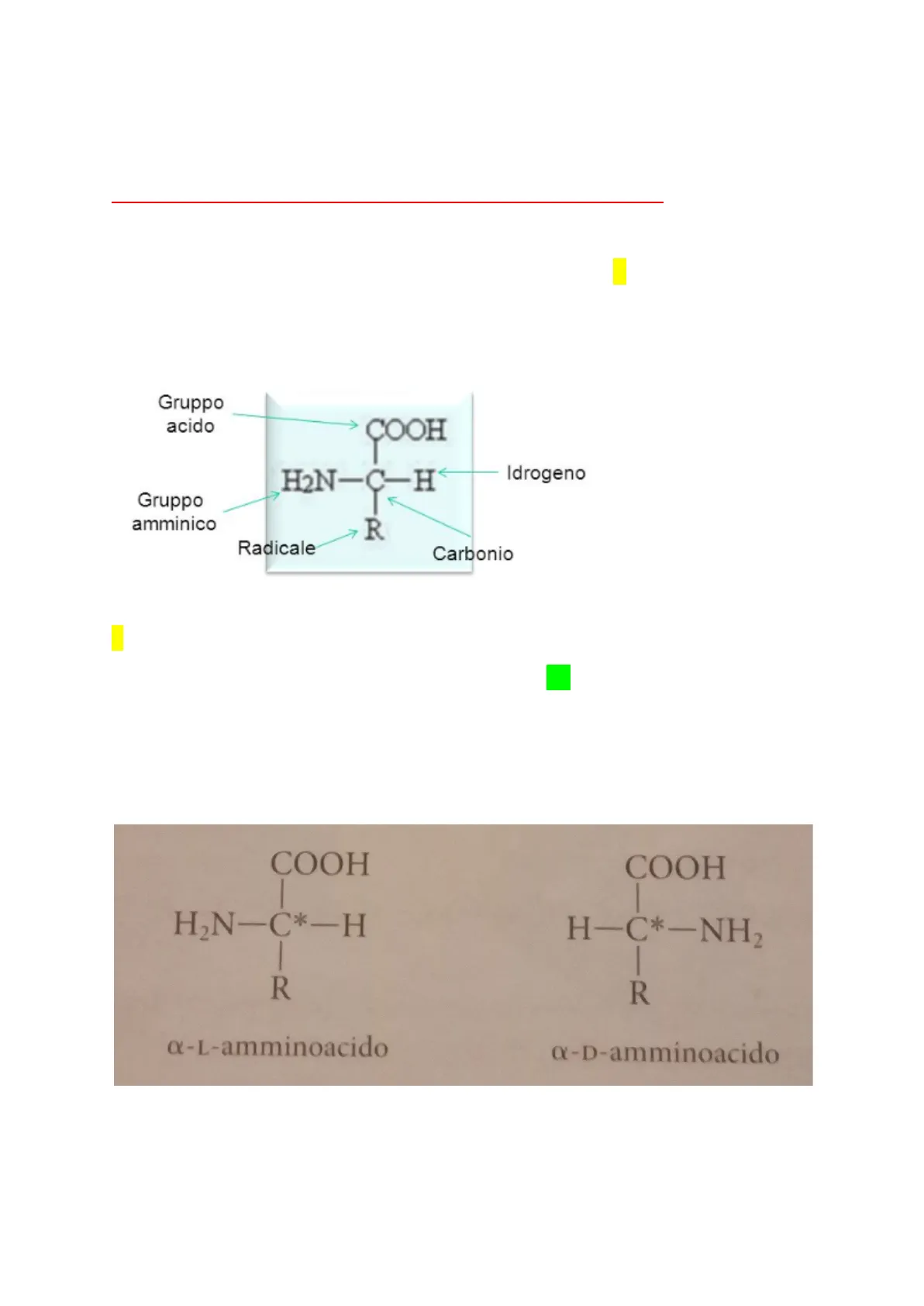
Prima di iniziare ALCUNI RICHIAMI TEORICI: A) Struttura generica di un a-aminoacidoº (conformazione L, biologicamente attiva): Gruppo acido COOH H2N-C-H Idrogeno F Gruppo amminico R 7 Radicale Carbonio
'Gli aminoacidi sono molecole chirali che si presentano sotto forma di due isomeri ottici (enantiomeriºº) diversi (D, L). Quasi tutti gli aa naturali hanno configurazione L. COOH H2N-C *- H COOH H-C *- NH2 1 R R a-L-amminoacido a-D-amminoacidoGli isomeri sono composti che, pur presentando la stessa formula bruta, mostrano una formula di struttura diversa o una diversa disposizione degli atomi nello spazio (stereoisomeria). L'entantiomeria, o isomeria ottica, è un tipo di stereoisomeria, tipica di quei composti in cui il carbonio presenta legami con 4 atomi o gruppi atomici diversi tra loro (come negli alfa-aminoacidi!). Il carbonio in questione viene chiamato stereocentro (o carbonio asimmetrico e si indica con C*) Enantiomeri (o isomeri ottici) sono due molecole con diversa disposizione spaziale degli atomi o gruppi atomici legati al C* e che sono l'una l'immagine speculare dell'altra, cioè non sono tra loro sovrapponibili nè per rotazione nè per traslazione nel piano. Tutto ciò è molto importante perché l'attività biologica degli enantiomeri può essere molto diversa.
Ioni Dipolari (Zwitterioni)
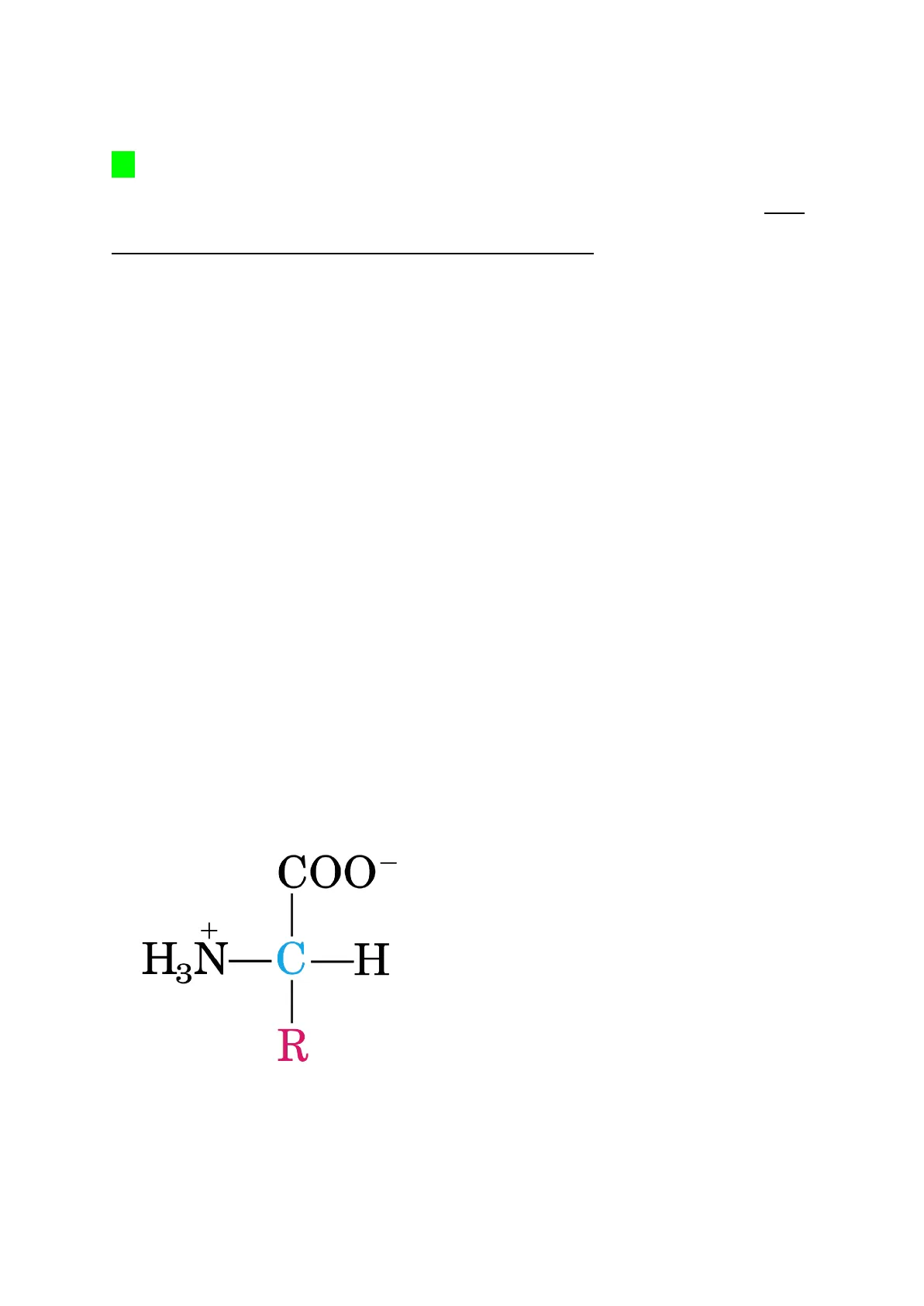
B) Gli aminoacidi, a PH fisiologico, sono presenti come ioni dipolari (zwitterioni): COO- + H3N-C-H I R
Produzione Industriale di Aminoacidi
Usi e Scopi degli Aminoacidi
La produzione industriale di aminoacidiUsi e scopi. Gli aminoacidi prodotti industrialmente trovano impiego sia in campo alimentare, come integratori, sia in campo farmaceutico che cosmetico. Gli aminoacidi di maggior interesse commerciale sono L-lisina, D- e L-metionina, L-fenilalanina, L-triptofano e L-tirosina, amminoacidi essenziali (non sintetizzabili dall'organismo) che spesso sono aggiunti, soprattutto nei paesi in via di sviluppo, alle proteine vegetali per integrarne il valore nutritivo. È importante anche l'acido glutammico, usato principalmente come aromatizzante.
Tipi di Processi Produttivi
Tipi di processi. Possono essere ottenuti sia per via biologica che per via chimica:
- per idrolisi delle proteine (da materiali proteici di scarto);
- fermentazione (in senso ampio);
- bioconversione enzimatica;
- sintesi chimica.
La produzione biologica presenta diversi vantaggi rispetto a quella chimica, nonostante la sintesi chimica sia di per sé più conveniente.Ciò perchè microrganismi ed enzimi sono specifici per la produzione di L-aminoacidi (la forma biologicamente attiva), mentre con la sintesi chimica si ottengono miscele racemiche* delle forme L e D, che richiederebbero alti costi per la loro separazione. Solo la metionina può essere ottenuta vantaggiosamente anche per sintesi chimica, perché ambedue le forme L e D sono assimilabili dall'organismo umano e animale.
Processi Produttivi dei Principali Amminoacidi
Tabella 7.2 Processi produttivi dei principali amminoacidi
Amminoacido Tipo di processo L-lisina Chimico e microbiologico D- e L-metionina Chimico L-fenilalanina Chimico e microbiologico (bioconversione) L-triptofano Chimico e microbiologico L-tirosina Chimico e microbiologico Acido glutammico Microbiologico Acido aspartico Microbiologico (bioconversione)
(* è detto racemo un miscuglio al 50% di due enantiomeri. Gli enantiomeri sono stereoisomeri che risultano l'uno l'immagine speculare dell'altro, e che presentano attività ottica opposta).
Substrati Utilizzati
Substrati. I substrati usati variano in relazione ai tipi di processi.Processo Substrato Sintesi chimica sostanze organiche Idrolisi di proteine materiali proteici di scarto Produzioni biotecnologiche (fermentazioni e bioconversioni) melasso + composti azotati organici e inorganici
Microrganismi Produttori
Microrganismi produttori. Gli aminoacidi sono normalmente presenti nei vari batteri, che li usano nella sintesi delle loro proteine, ma in quantità così piccole da non essere sfruttabili industrialmente. Nel caso delle fermentazioni, si ricorre allora a ceppi mutanti, modificati geneticamente.
Tra i miglioramenti genetici apportati ai batteri produttori di amminoacidi si sottolineano: -la ricombinazione genetica ottenuta mediante fusione protoplasti, grazie alla quale si sono selezionati ceppi ibridi con caratteristiche dei mutanti auxotrofi e dei mutanti resistenti; -l'ingegneria genetica, grazie alla quale si sono potuti clonare i geni e quindi ottenere grandi quantità di enzimi regolatori di diverse vie metaboliche al fine di modificare opportunamente le vie metaboliche stesse.Per ottenere una trasformazione efficiente (cioè più frequente) e quindi ceppi mutanti alto-produttori si interviene, inoltre, sui processi di permeabilizzazione delle membrane cellulari. Il microrganismo più usato è Corynebacterium glutamicum, ma vengono usati anche Brevibacterium falvum, Escherichia coli, Bacillus licheniformis, e i lieviti Candida humicola e Saccharomyces cerevisiae.
Si tratta in seguito e in dettaglio la produzione di due tra gli amminoacidi sopra citati: la lisina e l'acido glutammico.
Produzione di L-Lisina
Caratteristiche e Utilizzo della L-Lisina
E' un aminoacido essenziale, mal distribuito in alimenti importanti come i cereali. E' utilizzato come integratore sia nell'alimentazione animale (mangimi) che umana; ad esempio in Giappone viene addizionata al pane, essendo la lisina scarsamente presente nel frumento. La lisina viene inoltre usato come additivo alimentare, poiché migliora la qualità degli alimenti aumentando l'assorbimento degli altri aminoacidi.
Sintesi della L-Lisina
La produzione della L-lisina può avvenire sia per sintesi chimica che, soprattutto, per sintesi biologica. Si utilizzano ceppi mutanti di Brevibacterium favum o di Corynebacterium glutamicum (vedi immagini sotto), un Gram-positivo non patogeno, anaerobio facoltativo.sanitarieAt 45 5 2 um EHT = 3.00 kV WD = 12.5 mm Signal A = SE2 Mag = 10.00 K X ZEISS
Il Corynebacterium glutamicum metabolizza il glucosio attraverso la glicolisi e il ciclo di Krebs producendo L-lisina Un intermedio del ciclo di Krebs (l'acido ossalacetico) viene trasformato in acido aspartico (vedi immagine sotto). O= O O O GOT O C-C-CH2-C + C-CH (CH2} C 2 HO OH HO OH HO NH2 acido ossalacetico acido glutammico acido aspartico acido a-cheto glutarico 0 O 0 O + C-C(CH2} C 2 C-CH-CH2-C 1 OH HO OH NH2
L'acido aspartico, a sua volta, viene trasformato in semialdeide aspartica in seguito ad altre reazione enzimatiche (vedi immagine sotto, a). http://www.biology101.org/Acido aspartico Aspartato chinasi Ac. fosfoaspartico 1 Semialdeide aspartica Omoserina- deidrogenasi Lisina Omoserina a) Treonina Metionina
La semialdeide aspartica può seguire due vie: - può essere trasformata in omoserina che, a sua volta, può essere poi trasformata negli aminoacidi metionina o in treonina; - può essere trasformata in lisina tramite una serie di reazioni (infatti, la semialdeide aspartica può reagire con l'acido piruvico attraverso una reazione di condensazione formando l'acido 2,6-diidropicolinico (DHDP). II DHDP viene poi trasformato in acido diaminopimelico (DAP) che a sua volta viene trasformato in L-lisina).
La contemporanea presenza di L-lisina e L-treonina può portare a inibizione a feedback della aspartato chinasi e quindi dell'intera via di produzione della L-lisina.Per questo motivo, nella produzione di L-Lisina, in genere, si cerca di usare ceppi auxotrofi di C. glutamicum che siano incapaci di sintetizzare omoserina (perchè privi dell'enzima omoserina deidrogenasi) e quindi L-treonina (immagine sotto, b). In questo modo viene prodotta solo lisina che così si accumula nella cellula.
Sarà però necessario aggiungere al terreno quantità minime di L-treonina e L-metionina in quanto sono necessarie per permettere la sintesi delle proteine e di conseguenza per la riproduzione cellulare. Acido aspartico 1 Aspartato chinasi Ac. fosfoaspartico 1 Semialdeide aspartica Omoserina- deidrogenasi Lisina Omoserina b) Treonina Metionina
Processo Produttivo della L-Lisina
Il processo produttivo si realizza in fermentatori di tipo STR con agitazione air-lift in coltura sommersa. Può essere utilizzato sia un processo discontinuo o semicontinuo, e il processo può durare da 2 a 7 giorni. Il pH è compreso tra 6-8,mentre la temperatura è di 30-37ºC. Il processo richiede la presenza di ossigeno perché in anaerobiosi si accumulano acidi organici indesiderati. La resa è di circa il 30-40%.
Il terreno può essere così composto:
- melasso (fonte di C);
- composti azotati organici e inorganici (fonte di N);
- agenti antischiuma;
- quantità minime di treonina e metionina.
Il recupero del prodotto viene eseguito in questo modo:
- La brodocoltura viene filtrata per rimuovere la biomassa.
- La soluzione viene acidificata con acido cloridrico (HCl) per facilitare l'assorbimento degli aminoacidi alla resina a scambio ionico.
- Purificazione con resina a scambio ionico. Gli aminoacidi, e altre sostanze cationiche, interagiscono con la resina.
- I prodotti (aminoacidi e altre sostanze) legati resina vengono eluiti (riportati in soluzione) con l'aggiunta di idrossido di ammonio (NH4OH). Per purificare ulteriormente il prodotto possono essere effettuate successive purificazioni con resine a scambio ionico.
- La soluzione ottenuta viene ulteriormente concentrata e filtrata.
- L'aminoacido viene cristallizzato ed essiccato.
Acido Glutammico
Introduzione e Impiego dell'Acido Glutammico
Introduzione. Pur non essendo un amminoacido essenziale, l'acido glutammico è l'aminoacido prodotto in maggiore quantità dato il suo largo impiego nelle industrie, soprattutto quelle alimentari che lo adoperano come esaltatore di sapidità: viene infatti impiegato sotto forma di glutammato monosodico (E621) per esaltare l'aroma, per esempio, nei dadi da brodo. Viene inoltre utilizzato per la preparazione di sostanze impiegate per trattare il cuoio.
Produzione e Sintesi dell'Acido Glutammico
La produzione di acido glutammico avviene quasi esclusivamente per via microbiologica, impiegando soprattutto colture di batteri Gram+ non sporigeni aerobi. L'acido glutammico viene sintetizzato a partire dall'a-chetoglutarato, un intermedio del ciclo di Krebs; in condizioni normali, però, l'a-chetoglutarato viene trasformato in succinato dall'enzima a-chetoglutarato deidrogenasi (KDH) (vedi immagine sotto).