Geometria molecolare, legami intermolecolari e stato solido
Slide dal Liceo Artistico Statale Aldo Passoni Torino su geometria molecolare, legami intermolecolari e stato solido. Il Pdf esplora la teoria VSEPR, il legame a idrogeno e i solidi cristallini, con definizioni e illustrazioni per la chimica nella scuola superiore.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Liceo Artistico Statale Aldo Passoni Torino
Lezione 10 Geometria molecolare, legami intermolecolari, stato solido (prima parte). Docente: Di Pierro Alessandro 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Teoria V.S.E.P.R.
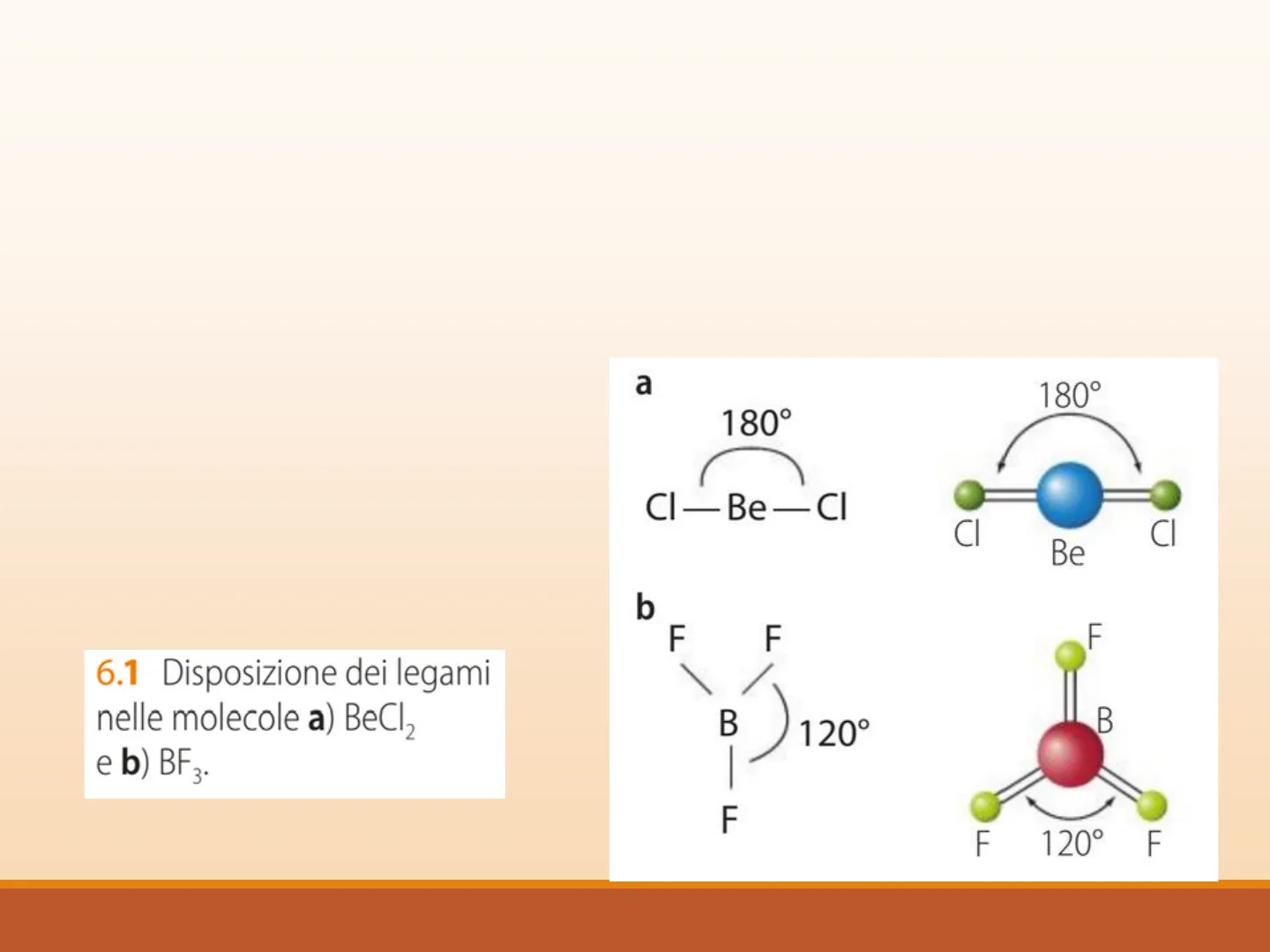
1Teoria V.S.E.P.R. V.S.E.P.R .: Valence Shell Electron Pair Repulsion Gli elettroni che appartengono al livello di valenza, sia che partecipino alla formazione di un legame, sia che non partecipino alla formazione di legame, esercitano repulsione reciproca (sono tutte cariche negative). Gli atomi rappresentati in verde subiscono repulsione reciproca e si mantengono alla massima distanza permessa dal legame 6.1 Disposizione dei legami nelle molecole a) BeCl2 e b) BF3. a 180° 180° CI-Be-CI CI CI Be b F F F B 120° F F 120° F Libro Pag.66 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Molecole planari e geometrie tetraedriche
2 BTeoria V.S.E.P.R. Le molecole appena viste sono planari, ovvero occupano lo spazio mantenendo i legami su uno stesso piano spaziale/cartesiano. Nel piano, gli angoli di 180° e 120° permettono di massimizzare le distanze tra gli atomi di cloro (Cl) e di fluoro (F), rispettivamente. Quattro doppietti elettronici massimizzano la loro distanza formando molecole non più planari ma assumendo geometrie tetraedriche: 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Geometria tetraedrica: metano, ammoniaca e acqua
3Teoria V.S.E.P.R. La geometria tetraedrica è propria ad esempio del metano, dell'ammoniaca e dell'acqua. La presenza di doppietti elettronici non condivisi riduce gli angoli di legame del metano, che ha tutti gli elettroni impegnati nei legami C-H, da 109,5° a 107,3 nell'ammoniaca (con un doppietto solitario) e 104,5 nell'acqua (con due doppietti solitari). H H-C-H H H H 1 H H 109,5° H-N-H 1 H ammoniaca H H 107,3º H H H H 104,5° H 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Comportamento polare della molecola
4Teoria V.S.E.P.R. La geometria molecolare ci permette di determinare il comportamento polare della molecola. La presenza di dipoli può infatti essere compensata dall'orientamento spaziale degli atomi 6.2 La molecola CO2 è apolare, quella dell'acqua è polare. 8 O 8+ 8+ H H 8- 8+ 8- O C O la polarità è distribuita simmetricamente, perciò la molecola risulta apolare la polarità è distribuita in modo asimmetrico, perciò la molecola risulta polare: sull'ossigeno si ha una parziale carica negativa, mentre su ciascun atomo di idrogeno c'è una parziale carica positiva 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Polarità e orientamento spaziale degli atomi
5Teoria V.S.E.P.R. La geometria molecolare ci permette di determinare il comportamento polare della molecola. La presenza di dipoli può infatti essere compensata dall'orientamento spaziale degli atomi 6.2 La molecola CO2 è apolare, quella dell'acqua è polare. 8 O 8+ 8+ H H 8- 8+ 8- O C O la polarità è distribuita simmetricamente, perciò la molecola risulta apolare la polarità è distribuita in modo asimmetrico, perciò la molecola risulta polare: sull'ossigeno si ha una parziale carica negativa, mentre su ciascun atomo di idrogeno c'è una parziale carica positiva 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Polarità e simmetria molecolare
6Teoria V.S.E.P.R. La geometria molecolare ci permette di determinare il comportamento polare della molecola. La presenza di dipoli può infatti essere compensata dall'orientamento spaziale degli atomi 8+ 4 8- 8+ 8+ 8+ CH 4 8- 8- 8+ 8- 4 8+ 8- 8+ 8+ 8+ CCI4 4 CH, CI 3 6.3 La polarità dipende dalla simmetria: il CH4 e il CCI4 sono simmetrici, perciò sono apolari; il CH3Cl è asimmetrico, perciò è polare. 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Legami intermolecolari
7Legami intermolecolari LEGAMI INTERMOLECOLARI
- Forze di van der Waals
- Legami a idrogeno (più forti)
- Legami dipolo-dipolo
- Legami ione-dipolo
- Forze di dispersione di London (forza intermedia) (dipoli istantanei/indotti, più deboli)
02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Forze di dispersione di London
8Forze di dispersione di London Si tratta di attrazione e repulsione di debole intensità che si forma tra dipoli di breve durata, dovuti al movimento degli atomi, causando «bipolarità» nella molecola. Le forze di London permettono di rendere liquidi i gas nobili e giustificano lo stato fisico degli alogeni (es. Iodio). Più elettroni disponibili permettono forze attrattive maggiori. 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Legame dipolo-dipolo
9Legame dipolo-dipolo Si tratta di attrazione e repulsione tra molecole polari, ovvero che possiedono dipoli permanenti. Le cariche parziali positive attrarranno le cariche parziali negative. Le cariche dello stesso segno si respingono. Es: Adesivi, piani molecolari di grafite Structure Of Graphite carbon atom, C covalent bond weak forces between layers 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Legame ione-dipolo
10Legame ione-dipolo Si tratta di attrazione tra solidi ionici e molecole polari, ad esempio NaCl e H2O. La somma delle forze di interazione ione-dipolo permette di indebolire il cristallo ionico portandolo alla solvatazione 8+ H O H 8- ione Na+ - - + + - + - + - + + + - + - + - + I - + + - Na+ 1 1 - + - H 8+ O 8- H 1 1 1 1 CI- 1 1 - - 1 I - + 1 1 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Legame a idrogeno
11Legame a idrogeno È la forza tra dipoli più forte, si forma tra atomi di idrogeno ed elementi molto elettronegativi come Fluoro (F), Ossigeno (O). Permette all'acqua di essere liquida a temperature relativamente alte, se confrontata a molecole simili. La struttura compatta del ghiaccio intrappola l'aria e quindi permette al ghiaccio di galleggiare. molecola d'acqua idrogeno ossigeno legame idrogeno 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Stato solido
12Stato Solido Lo stato solido è caratterizzato da unità elementari (atomi o molecole) unite da legami ad elevata energia. Nello stato cristallino, si ha la ripetizione nello spazio di una cella elementare, una piccola struttura formata da alcuni atomi che, ripetuta nello spazio, permette di rappresentare un reticolo cristallino. 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Solidi cristallini
13Solidi cristallini La cella elementare rappresenta una struttura ordinata a corto raggio (la distanza tra gli atomi è prossima alla distanza di legame). Il reticolo cristallino è invece una struttura ordinata a lungo raggio: l'ordine che si ottiene è di dolti ordini di grandezza rispetto all'unità ripetitiva. lattice structure unit cell 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Solidi amorfi
14Solidi amorfi Alcuni solidi non sono cristallini. I solidi non cristallini si chiamano amorfi. I solidi amorfi sono caratterizzati dall'avere solamente ordine a corto raggio e non a lungo raggio. Si riconoscono perché sono generalmente trasparenti (es: vetro, materie plastiche) Quarzo SiO2 (cristallino) a sinistra. · Si .O Vetro di silice SiO2 (amorfo) a destra. 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO
Solidi cristallini ionici
15Solidi cristallini ionici Sono solidi formati da forti cariche elettrostatiche tra ioni di carica opposta. Es. NaCl. Layer slips + + - + - + - + - + - + + + - + - + - + I - + + - 02/02/2025 SCIENZE E TECNOLOGIE CHIMICHE - LICEO PASSONI - TORINO 16 + + - + - + -