Biologia Molecolare: Apoptosi, meccanismi e proteine chiave
Documento di Biologia Molecolare – Bernassola Lezione 6 del 21/11/2024 sull'apoptosi. Il Pdf esplora la morte cellulare programmata, i meccanismi molecolari e le proteine chiave come caspasi e BCL-2, utile per studenti universitari di Biologia.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
BIOLOGIA MOLECOLARE - BERNASSOLA lezione 6 del 21/11/2024
Nella lezione precedente siamo partiti dal vertice degli eventi biochimici che culminano con la fase terminale dell'apoptosi che è la fase degradativa, i costituenti cellulari vengono degradati e portano poi la cellula alla morte. All'apice di questa cascata ci sono delle proteine che si chiamano BH3-only che ricevono lo stimolo apoptotico e fanno parte di una grande famiglia caratterizzata da questi numeri BH che sono diversi nelle varie sottofamiglie.
Le proteine BH3-only hanno il compito di ricevere lo stimolo e di attivarsi per andare ad attivare altri membri di questa sottofamiglia di cui BCL-2 è il capostipite. A questo punto inibendo BCL-2 che rappresenta un segnale inibitorio per l'apoptosi, viene rilasciata l'inibizione delle proteine BCL-2 like che esercitano sui membri di un'altra sottofamiglia di proteine appartenenti alla famiglia di BCL-2 che sono però pro-apoptotiche di cui abbiamo fatto l'esempio: BAX e BAK.
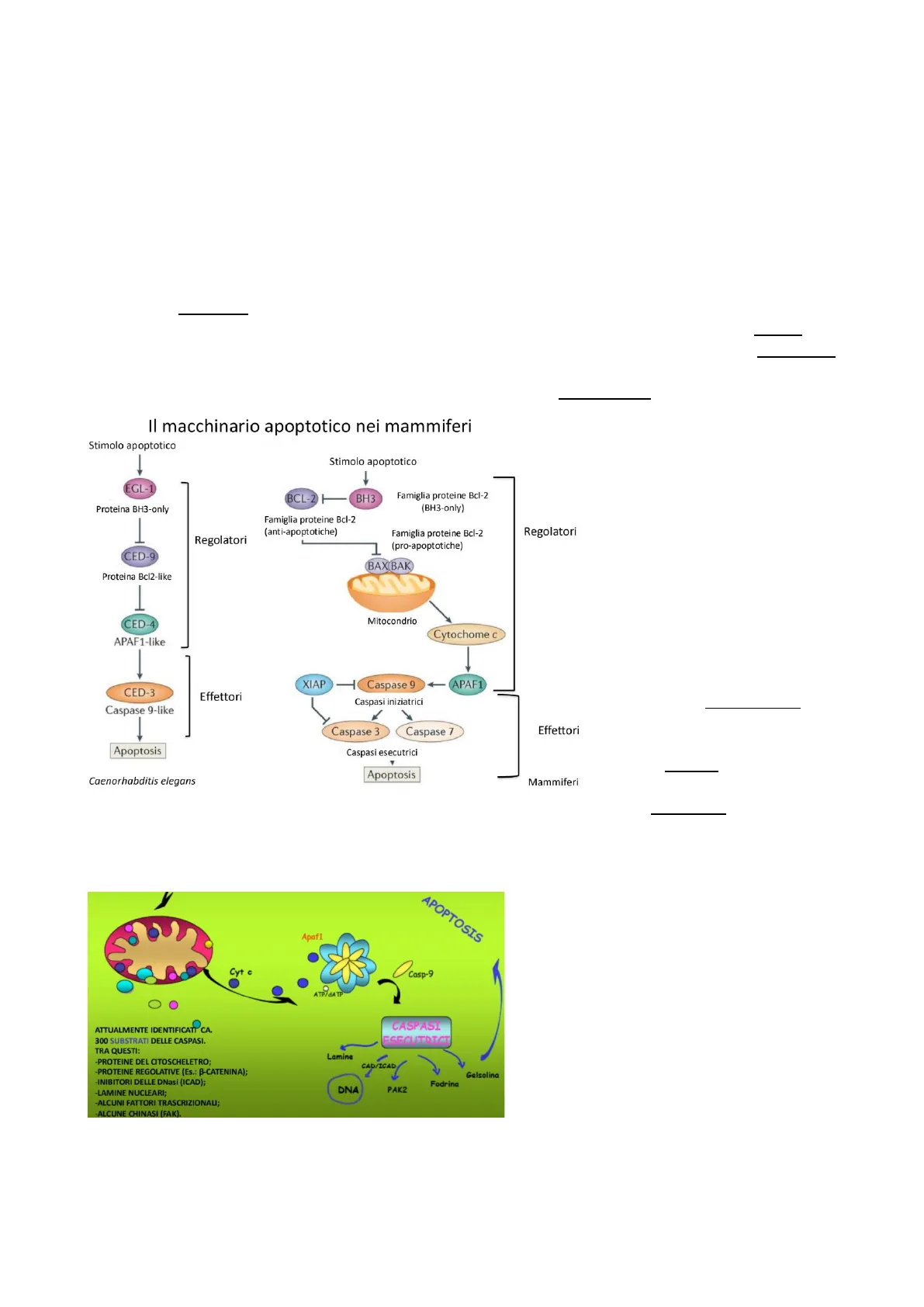
Il macchinario apoptotico nei mammiferi
Le pro-apoptotiche sono quelle Stimolo apoptotico che ricevono lo stimolo, Stimolo apoptotico rilasciano l'inibizione sulle anti- - EGL-1 BCL-2 H BH3 Famiglia proteine Bcl-2 (BH3-only) apoptotiche che a questo punto Proteina BH3-only Famiglia proteine Bcl-2 Regolatori Regolatori (anti-apoptotiche) portano all'attivazione di BAX e Famiglia proteine Bcl-2 (pro-apoptotiche) BAK, in particolare queste CED-9 proteine vanno a formare un BAX BAK Proteina Bcl2-like poro a livello della membrana esterna del mitocondrio e CED-4 Mitocondrio questo determina il rilascio di APAF1-like Cytochome c altre proteine pro-apoptotiche importanti per le fasi XIAP Caspase 9 APAF1 successive. Tra queste CED-3 Effettori Caspasi iniziatrici ricordiamo: Il citocromo C che Caspase 9-like Caspase 3 Caspase 7 Effettori nel citoplasma si complessa con Apoptosis Caspasi esecutrici una molecola adattatrice che si chiama APAF1 la quale in Caenorhabditis elegans Apoptosis maniera ATP-dipendente forma un complesso adattatorio per reclutare un enzima proteolitico che è la caspasi 9, una proteasi iniziatrice che svolge il suo compito andando ad attivare altre proteasi (sempre caspasi) che definiremo esecutrici o effettrici, poiché sono quelle deputate alla proteolisi ossia alla degradazione dei costituenti cellulari e quindi a portare la cellula alla fase effettiva di morte.
Mammiferi
1 1 1 APOPTOSIS Apaf1 Cyt c Casp-9 ATP/ dATP ATTUALMENTE IDENTIFICATI CA. 300 SUBSTRATI DELLE CASPASI. TRA QUESTI:
- PROTEINE DEL CITOSCHELETRO;
- PROTEINE REGOLATIVE (Es .: ß-CATENINA);
- INIBITORI DELLE DNasi (ICAD);
- LAMINE NUCLEARI;
- ALCUNI FATTORI TRASCRIZIONALI;
- ALCUNE CHINASI (FAK).
CASPASI ESECUTRICI Lamine CAD/ICAD Gelsolina Fodrina DNA PAK2 La caspasi 9 viene reclutata dal complesso che si chiama apoptosoma da forma inattiva a forma attiva ed è in grado quindi di agire attivando le caspasi 3, 6, 7. Vediamo uno zoom sull'azioene delle caspasi: una volta rilasciato il citocromo C si froma l'apoptosoma che recluta la caspasi 9 che va ad attivare le caspasi esecutrici. Queste andranno a tagliare tutta una serie di costituenti cellulari che sono fondamentali per il funzionamento cellulare, i substrati sono circa 300:
- Proteine del citoscheletro
- PROTEINE REGOLATIVE (Es .: ß-CATENINA);- INIBITORI DELLE DNasi (ICAD);
- LAMINE NUCLEARI;
- ALCUNI FATTORI TRASCRIZIONALI;
- ALCUNE CHINASI (FAK).
Correlazione substrati caspasi e aspetti morfologici
Adesso vediamo di correlare alcuni substrati delle caspasi con quelli che sono gli aspetti morfologici tipici della cellula apoptotica, in manera da ricondurre questo discorso della degradazione dei costituenti intracellulari da parte delle caspasi a un particolare fenotipo. Tipicamente il nucleo si frammenta, la cromatina e il citoplasma si condensano, fino a che la condensazione va così avanti che si formano delle invaginazioni a livello della membrana plasmatica per cui vediamo che protudono delle vescicole citoplasmatiche che si chiamano corpi apoptotici rilasciate dalla cellula. Se andiamo ad analizzare i diversi substrati delle caspasi vediamo: le lamine nucleari che rivestono il nucleo e, il taglio di queste, implica la distruzione dell'involucro nucleare ed è il primo contributo della degradazione che avviene nel nucleo.
ICAD e DNasi
ICAD ->(Inhibitor of caspase-3-activated Dnase) > quando il mitocondrio va incontro all'alterazione della permeabilità della membrana esterna porta alla fuoriuscita delle molecole anti-apoptotiche come il citocromo C che scatena tutto quello che viene a valle, ma non si tratta dell'unico fattore pro- apoptotico che esce in quel momento, ce ne sono altri tra cui la DNasi in particolare la DNasi CAD che si chiama caspase-3-activated Dnase. Un'altra endonucleasi AIF -> inducing apoptotic factor e un'altra endonucelasi che si chiama endonucelasi G. Tutte queste escono dal mitocondrio e quelle che intervengono in maniera caspasi indipendente sono il fattore AIF e l'edonucleasi G che iniziano a tagliare il DNA e contestualmente iniziano a favorire la condensazione della cromatina, soprattutto nella parte periferica. Quando ICAD ossia l'inibitore della DNasi che si chiama CAD viene tagliato dalle caspasi, l'inibitore non funziona più e quindi CAD si attiva, è libera di entrare nel nucleo e lì va a tagliare il DNA in maniera sequenza non specifica ma taglia dove è disponibile il DNA facendo dei tagli internucleari. Quindi anche lei contribuisce a condensare il DNA, le endonucleari tagliano e condensano il DNA.
PARP e riparazione del DNA
PARP > interviene nella riparazione del DNA, quindi anche in questo caso è importante che nel momento in cui viene tagliata dalle caspasi perde la sua attività: aveva I'N-terminale che è il dominio attraverso il cui lega il DNA poi un dominio centrale di automodificazione ossia un dominio a cui si attaccano i polimeri ATP-ribosio, un dominio C-terminale che è il dominio catalitico. Quindi quando viene tagliata si forma un frammento che perde il dominio di legame al DNA e quindi di conseguenza viene espulso nel citoplasma e rimane il frammento più piccolo che ancora ha il dominio di legame al DNA. Questo si va a legare al DNA e a questo punto agisce da dominante negativo nei confronti della proteina normale. Quindi PARP non funziona più, una volta che le caspasi lo tagliano non ripara contribuendo a creare lo strato di frammentazione del DNA e della cromatina.
Proteine del citoscheletro
Alcune proteine del citoscheletro come actina, tubulina e gelsolina > queste sono importanti poiché se noi digeriamo queste proteine del citoscheletro, questo collassa e si condensa, questo per spiegare la condensazione citoplasmatica e il fatto che alla fine la cellula si frammenta formando delle porzioni del citoplasma che si chiamano corpi apoptotici. La actina, tubulina e gelsolina sono proteine citoscheletriche: la gelsolina ha a funzione più di polimerizzatore dell'actina, nel momento in cui viene tagliata, viene meno la sua funzione di polimerizzare l'actina e quindi il taglio della gelsolina contribuisce alla distruzione del citoscheletro.
FAK e attacco del citoscheletro
FAK-> è una chinasi che regola l'attacco del citoscheletro alla membrana plasmatica, viene tagliata e il citoscheletro perde il contatto con la membrana plasmatica e alla fine otteniamo una cellula fatta a seguito del taglio delle caspasi.
LE CASPASI
Le caspasi sono una famiglia di proteine, di proteasi in cui il nome deriva dal fatto che sono delle proteasi a cisteina quindi:
- C sta per cisteina ossia il sito catalitico è una cisteina,
- Asp sta per il fatto che definisce la specificità per il substrato perché tagliano delle sequenze bersaglio e tagliano sempre dopo un residuo di aspartato, un esempio del sito bersaglio è: X-Glu-X-Asp.
Inoltre, distinguiamo le caspasi iniziatrici, per ora abbiamo parlato solo della 9 ma sono 4: 2, 8, 9, 10 e sono quelle che svolgono la funzione di attivare quelle effettrici che poi vanno a tagliare i costituenti cellulari e che si attivano generalmente quando vengono reclutate da una proteina adattatrice, nel caso della 9 è Apap. Le caspasi iniziatrici si autoattivano mediante taglio proteolitico del precursore, in seguito all'interazione con una molecola adattatrice. L'attivazione della caspasi 9 richiede l'intervento dell'apoptosoma.
Le caspasi esecutrici sono 3: 3, 6, 7 e vengono attivate dalle caspasi iniziatrici mediante taglio proteolitico dei precursori; tagliano proteine cellulari vitali innescando il processo apoptotico.
Distinguiamo una terza famiglia che sono le caspasi infiammatorie e sono la: 1, 4, 5 che sono convolte nel processo apoptotico, la 1 è convolta nel processo di morte cellulare programmata che si chiama piroptosi ma generalmente sono coinvolte nella maturazione delle citochine.
Struttura delle caspasi
La struttura di queste proteine è abbastanza conservata e distinguiamo: le esecutrici ed effettrici in ~p20 -p10 28 27 751 Le caspasi esecutrici alto in rosso e quelle iniziatrici in viola. Per Casp-3 hanno un prodominio N- 23 198 terminale corto (20-30 Casp-7 residui aminoacidi) generare la molecola matura è necessario che intervengano delle proteasi per rimuovere 23 179] |194 290 Casp-6 dei domini che sono presenti solo nel 216 374 385 479 .Casp-8 DED precursore per formare la molecola matura. DEL 4151 219| 521 Le caspasi iniziatrici hanno un prodominio N-terminale molto esteso Casp-10 DED DEC 315 33 416 (>90 aminoacidi) che contiene motivi di riconoscimento (es Casp-9 CARD 152| 3161 33 435 omo- o etero-tipiche, importanti Casp-2 CARD 270| 1290 per loro attivazione. CARD) coinvolti in interazioni Noi distinguiamo in tutte le caspasi un prodominio N-terminale che per le caspasi esecutrici è molto piccolo e massimo arriva a 30 residui amminoacidici, mentre è più grande p20 subunità maggiore linker intersubunità nelle caspasi iniziatrici poiché in questo p10 subunità minore protominio sono contenute delle sequenze che servono a queste caspasi in dorma di precursore a stabilire delle interazioni proteina-proteina che possono essere o di tipo omotipico quindi delle stesse molecole oppure di tipo eterotipico con molecole diverse. Nel caso della caspasi 9 il dominio CAD presente solo nel proenzima è quello che va ad interagire con un medesimo dominio CAD presente sulla molecola Apap 1 quindi si forma l'interazione tra Apap 1 e la procaspasi 9 grazie alla presenza di questo dominio che poi nella caspasi matura deve essere perso poiché a quel punto la caspasi dele lasciare l'apoptosoma nel citoplasma e deve andare a tagliare le caspasi esecutrici.
La presenza di questi domini e l'interazione proteina-proteina conferisce una grandezza maggiore (32-53kDa) QACXG D- D- procaspasi prodominio (3-24 kDa) Subunità grande p20 (17-21 kDa) Subunità piccola p10 (10-13 kDa) Una subunità piccola ed una grande si assemblano a formare un dimero caspasi (dimeriche) Due subunità piccole e due grandi si assemblano a formare un tetramero attivo caspasi (tetrameri attivi) caspasi 9 tetrameri attivi quando legati ad APAF1 al dominio N-terminale delle caspasi esecutrici. Tutte hanno una subunità che definiamo maggiore il cui peso molecolare che definiamo maggiore, infatti, va a seconda della caspasi da 17 a 21 kDa e uno più piccolo al C-terminale che ha circa un peso di 10-13 kDa. Quando le caspasi devono essere attivate, sia che siano iniziatrici e quindi attraverso un meccanismo autocatalitico o che siano