Stati della materia, passaggi di stato e leggi dei gas in chimica
Slide di Università sulla materia, i passaggi di stato e le leggi dei gas. Il Pdf esplora gli stati della materia (solido, liquido, gassoso) e le loro proprietà, i passaggi di stato come fusione ed ebollizione, e le leggi dei gas, inclusi i gas reali, per la materia di Chimica.
Mostra di più53 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
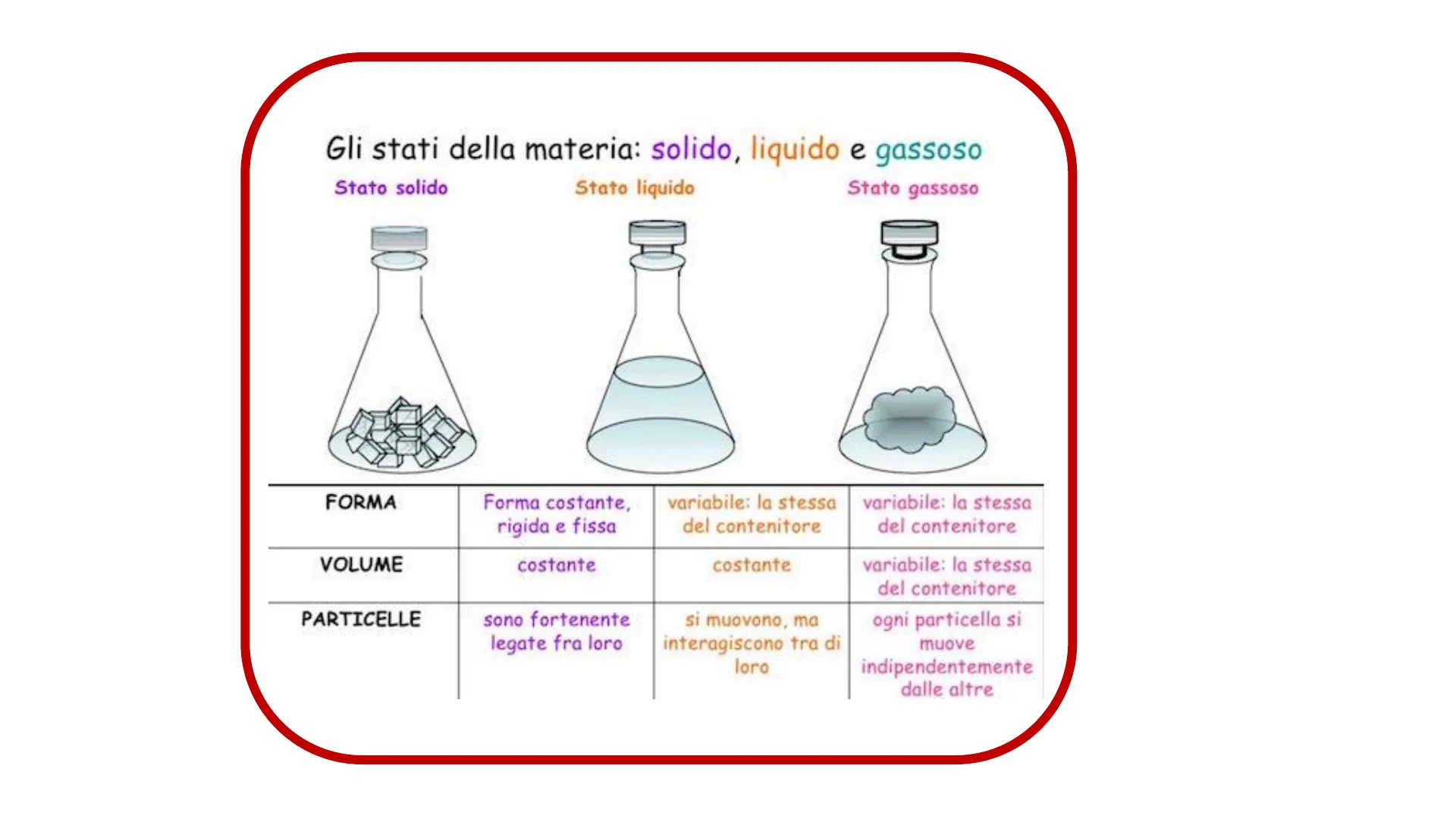
Gli stati della materia: solido, liquido e gassoso
Stato solido
Stato liquido
Stato gassoso
FORMA
Forma costante,
rigida e fissa
variabile: la stessa
del contenitore
variabile: la stessa
del contenitore
VOLUME
costante
costante
variabile: la stessa
del contenitore
PARTICELLE
sono fortenente
legate fra loro
si muovono, ma
interagiscono tra di
loro
ogni particella si
muove
indipendentemente
dalle altre
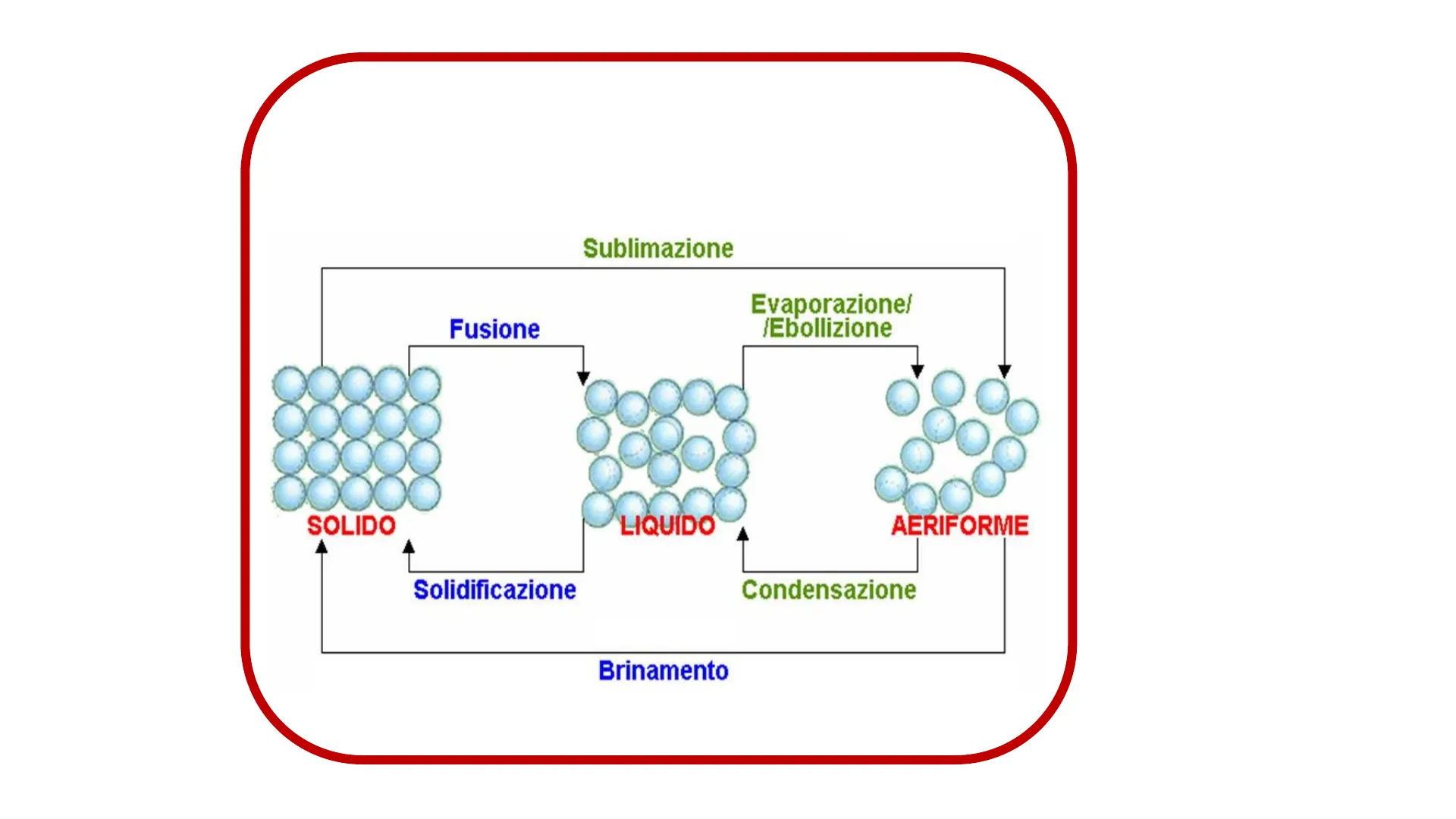
Passaggi di stato
1Passaggi di stato:
trasformazione Fisica
Sublimazione
Evaporazione/
/Ebollizione
Fusione
SOLIDO
LIQUIDO
AERIFORME
4
Solidificazione
Condensazione
Brinamento
Fasi condensate e forze intermolecolari
2Fasi condensate e forze
intermolecolari
C
O
Secondo la teoria cinetica molecolare, allo stato
gassoso le molecole sono molto distanti tra loro, tanto
da poter essere considerate puntiformi.
Perché si formano le fasi condensate?
Perché esistono forze intermolecolari, cioè forze di
attrazione di tipo elettrostatico più deboli (circa il 15%)
di quelle tra ioni di carica opposta, che fanno sì che le
molecole si attraggano tra loro.Passaggio di stato
Il passaggio da una fase ad un'altra è
determinata dal bilancio tra energia
potenziale della molecola (cioè l'energia
dei legami intermolecolari) ed energia
cinetica (cioè legata al movimento delle
molecole) delle molecole che tende a
disperderle.
- All'aumentare della temperatura, aumenta
l'energia cinetica media e quindi le particelle
che si muovono a velocità maggiore possono
vincere più facilmente le attrazioni. - Una diminuzione di temperatura, invece,
permette alle forze intermolecolari di
riavvicinare l'una all'altra le molecole che si
muovo a velocità più bassa.
Influenza delle forze intermolecolari
Le forze intermolecolari influiscono sul:
- punto di ebollizione, punto di
liquefazione; - sulla solubilità di gas, liquidi e solidi
in vari solventi.
I gas
Nel 1630 fu usato per la prima volta il
termine gas: Van Helmont che lo
inventò, pensava però che non fosse
possibile contenere un gas in un
recipiente, perché aveva una natura e
una composizione diversa dai liquidi e
dai solidi.
Aria
Il primo scienziato a raccogliere una
sostanza aeriforme fu Robert Boyle.
Egli teorizzò che l'aria fosse costituita
da microscopici corpuscoli in
movimento capaci di legarsi tra loro per
formare aggregati macroscopici.
Composizione dell'aria
Aria
Nonostante per molti secoli si sia
creduto che l'aria fosse una sostanza
elementare, essa è in realtà una
miscela di gas composta
prevalentemente da ossigeno e azoto
e da altri numerosi componenti.
LA COMPOSIZIONE DELL'ARIA
Neon, Elio, Metano, Kripton, Xeno, Idrogeno e Ozono; poiché
questi gas sono presenti in quantità ridottissime, vengono
comunemente chiamati "elementi in tracce"
Argon 0,9%
Altri Gas
0,1%
È un gas inodore e insapore. Per il
suo effetto "asfissiante" viene usato
anche per estinguere incendi
Ossigeno
20,9 %
Azoto 78,1%
È un gas inodore, incolore e
insapore, ma indispensabile per la
respirazione di tutti gli esseri viventi
>
È un gas presente nell'aria, che non può essere
utilizzato direttamente dalla maggior parte degli
esseri viventi, perché è velenoso se respirato
senza ossigeno
I gas ideali e la teoria cinetico-molecolare
I gas ideali e la teoria cinetico-
molecolare
I gas dal punto di vista macroscopico
hanno tutti lo stesso comportamento, che
tuttavia risulta sensibile alle variazioni di
temperatura e pressione.
La teoria cinetico-molecolare ne spiega
la natura sulla base del modello dei gas
ideali o perfetti.
Modello del gas ideale
Modello del gas ideale
· l'energia cinetica media delle particelle
è proporzionale alla temperatura
assoluta;
· non si attraggono reciprocamente;
· sono puntiformi e il loro volume è
trascurabile;
· si muovono a grande velocità in tutte le
direzioni con un movimento disordinato.
Le particelle si muovono
nel vuoto a grande veloci-
tà in tutte le direzioni.
Il moto delle particelle è
interrotto dagli urti tra di
esse e con le pareti del
contenitore.
Pressione
I gas non hanno forma propria, ma
occupano quella del recipiente che li
contiene: le particelle, quando sono
lontane le une dalle altre, non risentono
delle forze attrattive.
In generale, la pressione p è data dal
rapporto tra la forza F, che agisce
perpendicolarmente a una superficie, e
l'area s della superficie stessa.
forza esercitata
sulla superficie
pressione
E
S
area della
superficie
Unità di misura della pressione
Pressione
La pressione è una
grandezza intensiva.
L'unità di misura della
pressione nel Sistema
Internazionale è il pascal
(Pa), pari a un newton (N)
per metro quadrato (m2).
1 Pa = 1N / m2
Misurazione della pressione atmosferica
Torricelli
Nel 1644 Torricelli costruì un dispositivo per
misurare la pressione atmosferica: il primo
barometro a mercurio.
Prese un lungo tubo di vetro, chiuso ad una
estremità, lo riempì di mercurio e lo
capovolse.
A livello del mare, il livello del mercurio nel
tubo si abbassava ad un'altezza di 760 mm.
VUOTO
76 cm
PRESSIONE
ATMOSFERICA
1
1
Il livello raggiunto dal mercurio fornisce la
misura della pressione atmosferica
esercitata sulla superficie del mercurio
nella bacinella, espressa in millimetri di
mercurio (mmHg).
MANOMETRO
Uno strumento per misurare la pressione
Conversioni di pressione
Conversioni
1 atmosfera =760 mm Hg =
= 101.325 KPa = 1.01325 bar
1bar = 1x105 Pa= 1x 102 Kpa = 0.9872 atm
Legge di Boyle
Legge di Boyle
Sperimentalmente, Boyle ha dimostrato
che, a temperatura costante, la
pressione di una data quantità di gas è
inversamente proporzionale al suo
volume.
pV = k con T costante
Questa è la legge di Boyle:
comprimibilità dei gas.
V1
V2 < V1
Il numero totale di parti-
celle resta lo stesso, ma
aumenta il loro numero
nell'unità di volume.
P1
P2>P1
100 190
150 100
8
La pressione aumenta
perché aumenta la fre-
quenza degli urti.
ISOTERME
ISOTERME
d
Q
Volume, V
1/Volume, 1/V
Meccanica respiratoria
MECCANICA RESPIRATORIA
L'alternanza di inspirazione ed espirazione consente di ventilare i polmoni
i muscoli intercostali
si contraggono la
cassa toracica si
espande
Aria
inspirata
Legge di Boyle
PV=K
i muscoli intercostali
si rilassano la cassa
toracica si contrae
aria
espirata
Inspirazione: la
cassa toracica si
espande,
la
pressione
interna
cala,
l'aria
viene
inspirata
Espirazione
Il diaframma si contrae (si abbassa)
Il diaframma si rilassa (si alza)
Espirazione: la cassa toracica si contrae, la pressione interna aumenta,
l'aria viene espirata
APPARATO RESPIRATORIO
9
Polmone
Diaframma
Inspirazione
La Fisica subacquea
La Fisica
subacquea
alb
a
cd
· Ipotizziamo di immettere in un contenitore una
quantità d'aria pari a quella preesistente, lo
spazio disponibile nel recipiente dovrà essere
diviso necessariamente tra le due dosi d'aeriforme
e se raddoppiamo ancora la quantità d'aria,
nell'involucro ci saranno 4 parti d'aria (a, b, c, d)
che occuperanno insieme lo stesso spazio
precedentemente occupato dalla quantità iniziale
· E' intuitivo che alla riduzione di volume di ogni
singola dose d'aria, corrisponderà un aumento
della relativa pressione che varierà così in modo
inverso.
Legge di Boyle Mariotte
Legge di Boyle Mariotte:
A temperatura costante, il volume di una certa quantità di gas è
inversamente proporzionale alla sua pressione.
Torniamo alla nostra bombola!
Per quanto detto, caricarla alla pressione di 200 atm
significa immettere in essa una quantità d'aria
200 volte maggiore della capacità del contenitore.
Pertanto, se abbiamo una bombola da 15 litri carica
a 200 atm, in essa ci saranno:
15 X 200 = 3.000 litri d'aria
a disposizione che rappresenteranno
la nostra scorta vitale in immersione.
A
Esempio di applicazione della Legge di Boyle
La Fisica subacquea
PROFONDITA' ATA VOL. ARIA
0 m
10m
2
1/2
20m
3
1/3
30m
4
1/4
40m
5
1/5
· Facciamo un altro esempio: prendiamo una palla da
spiaggia (di quelle viniliche con cui giocano i
bambini), mettiamola in un retino insieme a dei
sassi, in modo da annullare la sua spinta positiva
(Principio di Archimede) e portiamola in
immersione.
. Man mano che scendiamo la pressione esterna
costringe la palla ad una riduzione di volume a cui
corrisponde un aumento della pressione interna
(fig.2).
· E' chiaro che, risalendo in superficie, la palla
riprenderà il suo iniziale volume e la pressione
interna ritornerà ai valori esistenti
precedentemente all'immersione.
1
0 m = 1 ATM
10 m = 2 ATM
1/2
20 m = 3 ATM
1/3
30 m = 4 ATM
1/4
40 m = 5 ATM
1/5
Legge di Boyle
e il sommozzatore
PV = K
Legge di Charles
Legge di Charles.
Charles dimostrò sperimentalmente che, a
pressione costante, il volume di una data
quantità di gas è direttamente proporzionale
alla sua temperatura assoluta
V/T = k
con T temperatura assoluta e p costante
Questa è la legge di Charles: effetto della
temperatura sul volume dei gas.
V1
T1
P1
T2 > T1
V2> V1
Raddoppiando la
temperatura as-
soluta, il volume
raddoppia.
P2=P1(A
Gonfiemo il palloncino
e aumentiamo la massa
e il volume del gas.
B
Riscaldiano L'aria
contenuta nel palloncino:
il volume del gas
aimente.
(C) Raffreddiamo l'aria
contenuta nel palloncino:
il volume del gas
diminuisce.
Comprimiamo H palloncino
gordin: ridluciano il volume
del gins e aumentiamo la
su pression
Zero assoluto
-273,15 ℃ è lo zero assoluto (0 K), ovvero la
temperatura alla quale il volume dei gas si annulla.
50
40
Volume del gas (mL)
Idrogeno (H2)
330
Zero assoluto
20
-273.15℃
Ossigeno (02)
10
-300
-200
-100
0
100
200
300
Temperatura (℃)
Legge di Gay-Lussac
Legge di Gay-Lussacc
Sperimentalmente Gay-Lussac ha dimostrato
che, a volume costante, la pressione di una
data quantità di gas è direttamente
proporzionale alla sua temperatura assoluta.
p/T = k
con V costante.
Questa è la legge di Gay-Lussac.
La velocità delle particelle aumenta.
T1
T2 > T1
V2 = V1
Raddoppiando la
temperatura as-
soluta, la pressio-
ne raddoppia.
P1
P2> P1
-
Legge di Charles e Gay-Lussac
Legge di Charles e Gay-Lussacc
ISOBARA
ISOCORA
P
>
5
Temperatura, T
Temperatura, T
Le reazioni dei gas e il principio di Avogadro
Le reazioni dei gas e il principio
di Avogadro
Le ricerche condotte da Gay-Lussac sui
gas confermarono l'esistenza di rapporti di
combinazione ben precisi tra i loro volumi.
Gay-Lussac arrivò quindi a formulare la
legge di combinazione dei volumi.
Il rapporto tra i volumi di gas che
reagiscono tra loro è espresso da numeri
interi e piccoli.
Principio di Avogadro
Le reazioni dei gas e il principio
di Avogadro
La legge di combinazione dei volumi di
Gay-Lussac e la teoria atomica di Dalton
furono messe in relazione dal principio di
Avogadro.
Volumi uguali di gas diversi, alla stessa
pressione e temperatura, contengono lo
stesso numero di molecole
V
V
O2
Cl2
Massa di atomi e molecole
Quanto pesano un atomo o una
molecola?
Sappiamo che, a parità di pressione e
temperatura, in un litro di gas ossigeno
(O2) e in un litro di gas idrogeno (H2) vi è
lo stesso numero di molecole.
Il rapporto tra la massa dell'ossigeno e la
massa dell'idrogeno è pari a 16.