Modificazioni istoniche e il loro impatto sull'espressione genica
Documento della Prof.ssa Maria Letizia Penolazzi sulle modificazioni istoniche. Il Pdf, utile per lo studio universitario di Biologia, esplora i meccanismi molecolari che regolano l'accessibilità del DNA e la trascrizione, con diagrammi esplicativi e un focus su acetilazione, metilazione e splicing.
Mostra di più17 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Biochimica, Lezione 32, 29/11/2023
Prof.ssa Maria Letizia Penolazzi
Modificazioni istoniche
La professoressa riprende l'ultimo concetto trattato nella lezione precedente. Le variazioni di espressione di un gene di una proteina possono dipendere non solo da variazioni di sequenza nucleotidica (mutazioni a livello delle sequenze di DNA), ma anche da meccanismi di controllo legati all'epigenetica. In particolare si è trattato delle modifiche istoniche di acetilazione e deacetilazione degli istoni e metilazione del DNA. Entrambi questi fattori sono in grado di condizionare l'accessibilità della sequenza nucleotidica. Abbiamo visto come il DNA risulti essere avvolto attorno alle proteine istoniche, l'ottamero di H3, H4 e H2A, H2B. L'unità chimica della cromatina, ovvero il nucleosoma, dà da una parte il vantaggio di avere una abbondantissima informazione in pochissimo spazio, dall'altra parte l'accessibilità a questa informazione deve essere strettamente discriminata per rendere veloce il passaggio della trascrizione.
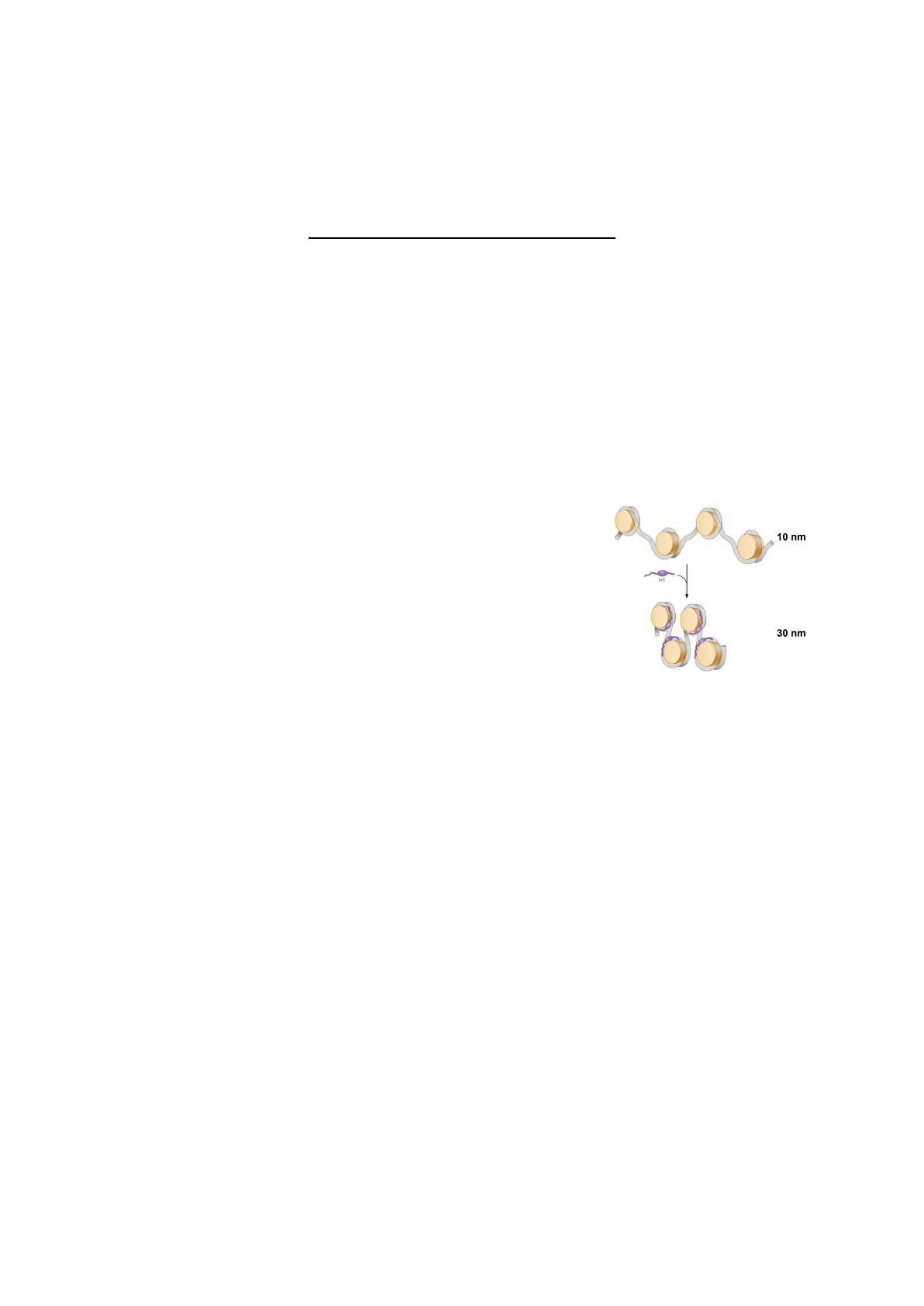
10 nm 30 nm
Ruolo delle code N-ter
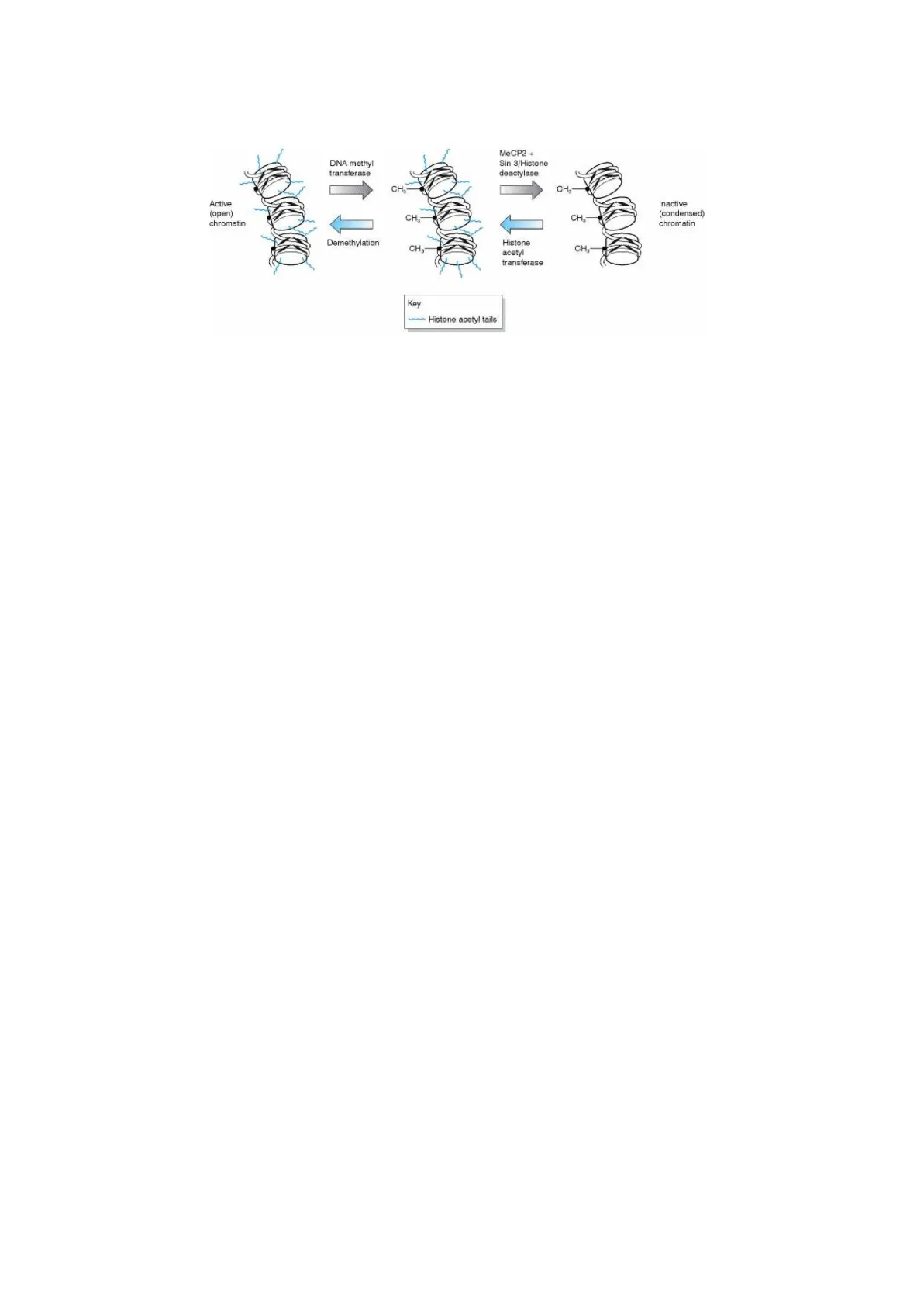
La compattazione della cromatina attorno alle proteine istoniche, specialmente H1, serve per creare le strutture di 30 nm. Le parti terminali di queste proteine istoniche, chiamate code N-ter, possono subire processi di modificazione covalente. I processi di acetilazione, fosforilazione e metilazione tendono a rendere più accessibile la molecola di DNA. La metilazione invece a livello dei nucleotidi richiama proteine leganti le citosine metilate o delle istone deacetilasi, rende quindi ancora più silenziata una determinata zona della cromatina. Gli effetti di questo tipo avvengono solo su zone particolari della proteina, le code n-terminali. In esse sono presenti residui di serina, lisina o treonina che possono subire fosforilazione, acetilazione, metilazione, o può intervenire l'ubiquitina che va a degradare la proteina istonica. Le istone deacetilasi insieme alle proteine leganti il DNA metilato creano questo complesso che rende "repressa" la cromatina, non più accessibile dal macchinario di trascrizione. Le citosine metilate recepiscono l'arrivo di altre proteine piuttosto che le RNA polimerasi; inoltre vengono riconosciute in modo specifico da proteine sensibili alle citosine metilate, e quindi poi richiamano altre proteine e insieme reprimono la cromatina.Nella foto sono rappresentate le CpG binding proteins, responsabili della repressione della cromatina.
DNA methyl transferase MeCP2 + Sin 3/Histone deactylase CH3 CH Active (open) chromatin CH3 CH Inactive (condensed) chromatin Demethylation CH3 Histone acetyl transferase CH3 Key: ~ Histone acetyl tails
Metabolismo ed epigenetica
Il metabolismo ha un ruolo importante sull'epigenetica. L'istone acetilasi o deacetilasi può essere più o meno attiva in relazione alla quantità di acetato e di acetil-coenzima A che è presente in quel momento nella cellula. È sensibile alla quantità di NAD+ e NADH presente nel citoplasma. Uno sbilanciamento metabolico dovuto a un evento stressante per l'organismo, ad esempio l'abuso di alcol, può riflettersi su questi meccanismi, perché interferisce in un meccanismo legato allo stato di acetilazione degli istoni. Il ciclo del metile è legato al ruolo della metionina nel determinare la formazione della s-adenosil- metionina, il trasportatore principale del metile nelle metiltransferasi, le quali intervengono a livello di reazioni metaboliche, nella metilazione delle citosine e delle proteine istoniche. Una volta che ha ceduto il suo metile, la s-adenosil-metionina diventa s-adenosil-omocisteina e poi omocisteina. Grazie all'intervento del tetraidrofolato e della vitamina B12, viene poi ripristinata con metionina.
Differenziamento cellulare e accesso alla cromatina
L'accesso alla cromatina è diversamente regolato anche a seconda dello stato di differenziamento delle cellule. Nello zigote, le cellule embrionali pluripotenti che possono diventare tutte le linee di sviluppo embrionale nel nostro organismo. Le cellule multipotenti (di origine ectodermica, mesodermica, endodermica), una volta individuato un lineage, lo mantengono. Una cellula della linea mesodermica non può diventare una cellula della linea ectodermica; questo avviene solo nel caso della pluripotenza. L'ultimo step sono le cellule somatiche, differenziate, per le quali non c'è più un transdifferenziamento. Osservando il pattern di metilazione della cromatina di queste tipologie cellulari, si può vedere come in uno stesso organismo, dalla prima cellula del nuovo individuo a una cellula specializzata ad esempio dell'epitelio intestinale, il livello di metilazione del DNA aumenta. Dal punto di vista genetico l'organismo è già determinato. Le cellule del nuovo individuo non sono diverse geneticamente; il genotipo dell'organismo è lo stesso per tutte le cellule. Cambia però il fenotipo, quello che la cellula riesce ad esprimere.Da cosa dipende la differenza tra le cellule? Da quanto il DNA è accessibile. Si osserva in cellule a diverso stadio di differenziamento la quantità di cromatina accessibile che hanno a disposizione la DNA polimerasi e i sistemi legati a trascrizione e traduzione. La cellula totipotente è altamente accessibile, ha una percentuale bassissima di DNA metilato. I neuroni invece, che sono altamente differenziati, hanno la cromatina molto meno accessibile e più metilata.
RNA regolatori
Esistono alcune brevi sequenze di RNA non classificabili come RNA transfer, messaggero, ribosomiale, alle quali fino a qualche anno fa non era stato attribuito un ruolo funzionale. Questi RNA molto corti nascono per regolare, interferire con altri meccanismi. Il loro ruolo fisiologico è nell'ambito dell'epigenetica. Molti di questi hanno una sequenza genica, un promotore, che porta alla loro produzione ma il loro ruolo non è strutturale bensì prettamente regolatorio. Nel momento in cui sono funzionali sono costituiti da 20/23 nucleotidi. Presentano zone a doppio filamento, altre zone che formano forcine o loop, altre ancora a single strand. Nascono come double strand e svolgono la loro attività a single strand. Prendono il nome di microRNA. Nascono come pre-mir, un RNA messaggero fatto di tante copie di questa sequenza di microRNA. Prima subiscono l'azione di una RNAsi, costituendo il pre-microRNA. Poi attraverso una esportina passano dal nucleo al citoplasma. Qui subiscono l'azione di un'altra RNAsi che forma il microRNA maturo, prima in forma double strand e poi nelle due forme single strand. Le due emieliche di RNA sono quindi 3p o 5p. Cosa fanno i microRNA? Si assemblano con proteine chiamate RISC (RNA-induced silencing complex), particolari RNAsi attive solo se interagiscono con questi microRNA a single strand. In base alla complementarietà tra la sequenza del microRNA e quella dell'RNA messaggero, vanno a bloccare i processi di traduzione dell'RNA messaggero, o ne innescano la distruzione (il cosiddetto mRNA cleavage). Troviamo un meccanismo simile anche per i cRNA, i RNA interferenti: questi non hanno esito in proteina bensì nascono con funzione regolativa, ma questo non significa che abbiano minor importanza metabolica. Anzi i cRNA sono stati individuati come marcatori in alcune patologie. Esiste quindi una nuova parte della diagnostica legata all'individuazione dei microRNA circolanti a livello ematico: la loro presenza è sintomo di forme patologiche o tumorali. La molecola di RNA è a single strand ed è molto delicata. Le RNAsi sono dappertutto; quando si lavora con RNA in laboratorio si presta molta attenzione perché la molecola si degrada facilmente. Essendo invece i microRNA molto piccoli, sono più resistenti e meno attaccabili dalle RNAsi.Recentemente è stato individuato che per riuscire ad ovviare al problema della veicolabilità dei microRNA, spesso questi sono complessati all'interno di vescicole. Accade in particolare nelle cellule tumorali. I microRNA, piuttosto che essere rilasciati a livello ematico, vengono protetti da un doppio strato fosfolipidico e possono raggiungere altre cellule protette da questo doppio strato. Attualmente i microRNA vengono impiegati in diagnostica come marcatori tumorali. Questi meccanismi saranno ripresi dalla professoressa Bianchi.
Trascrizione nei procarioti
Molti dei concetti sono stati trattati quando si parlava del metabolismo. Nei procarioti l'unità fondamentale dell'informazione genica è l'operone. Quando avviene la trascrizione, si crea un mRNA il quale codifica tutti gli mRNA corrispondenti alle proteine coinvolte ad esempio nella metabolizzazione di un aminoacido. Nei procarioti la trascrizione è accoppiata alla traduzione, quindi il processo avviene rapidamente. Negli eucarioti invece la trascrizione avviene nel nucleo, poi il mRNA modificato arriva nel citoplasma, dove subirà il processo di traduzione. Dal punto di vista chimico, la polimerizzazione che porta alla formazione di mRNA prevede l'attacco di nucleotidi (non di desossiribonucleotidi), in modo simile al processo che avviene nella sintesi del DNA, con la creazione di bolle trascrizionali in cui il mRNA è la copia complementare di una delle due emieliche del DNA. La differenza rispetto alla polimerizzazione del DNA è che in questo caso non è necessario un primer. Non si parte da un 3' libero, ma viene inserito direttamente il primo nucleotide. Ogni volta che l'enzima RNA polimerasi si attacca, si indirizza verso una zona specifica della cromatina. L'indirizzamento è dato da sequenze presenti nella regione promotrice.
Promoter procariotico
Promoter Utilizzando come esempio un operone +1 procariotico (nell'immagine), quindi più 5' 3' TT GACa 5' 3' AACTGt semplice, si può individuare il punto TAt Aa T AT a Tt A d'inizio della trascrizione indicato come - 35 Sequence - 10 Sequence Transcription start +1. In posizione -10, a sinistra del punto 4-Upstream Downstream-> in cui viene inserito il primo nucleotide, si trova la TATA box (negli eucarioti in un'altra posizione). Questa sequenza TATA BOX TATAT è riconosciuta in modo specifico ed è un fortissimo promotore. Quando la RNA polimerasi la intercetta, si posiziona in quel punto. Il promotore classico procariotico prevede anche in posizione -35 un'altra box, la cui sequenza è TTGACA, anche questa riconosciuta come forte promotore. Queste posizioni sono fortemente conservate poiché fisicamente la RNA polimerasi può posizionarsi considerando le specifiche distanze tra le sequenze promotrici.