Chimica inorganica: ossidi, pH e sali per la scuola superiore
Documento di Chimica inorganica. Il Pdf esplora concetti fondamentali come ossidi, pH e sali, ed è utile per lo studio della Chimica nella scuola superiore.
Mostra di più8 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Chimica inorganica
52 011 Chimica inorganica 5C 4 4 CuSO CoSO O NiCL2 NAH K2Cr2O7 MO L-DOPA NH2 0 Me NOOH 1 NO 1 Me 0 NaMnO7 21 Me I K2 CO: 3N AC NA Ketone N I
Ossidi
Se osservi del legno bruciato e del ferro arrugginito ti sembrerà che non abbiano niente in comune. In realtà, il carbonio presente nel legno e il ferro hanno subito entrambi una reazione chimica chiamata ossidazione. Il carbonio (non metallo) e il ferro (metallo) hanno infatti reagito con l'ossigeno presente nell'aria formando nuovi composti, chiamati ossidi.
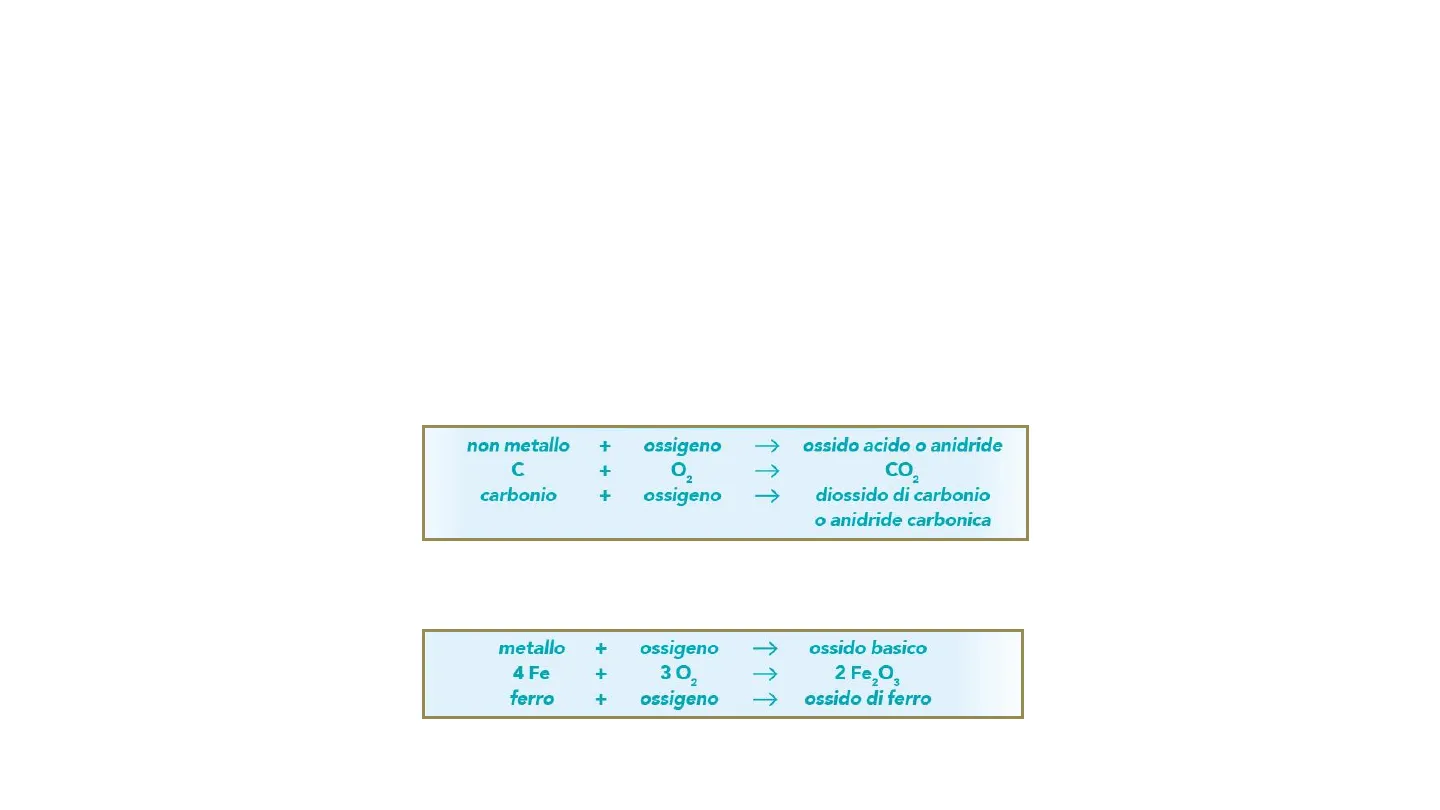
La reazione di ossidazione tra un non metallo e l'ossigeno dà origine a ossidi acidi o anidridi: non metallo C carbonio + ossigeno ossido acido o anidride + + O2 ossigeno -> CO2 diossido di carbonio o anidride carbonica
La reazione di ossidazione tra un metallo e l'ossigeno da origine a ossidi basici o semplicemente ossidi: + ossigeno 302 -> ossido basico metallo 4 Fe + ferro + ossigeno 2 Fe,O3 ossido di ferro
Acidi
Molti dei liquidi con cui abbiamo a che fare quotidianamente sono acidi, come l'aceto.
Gli acidi sono composti che derivano dalla reazione di un ossido acido (ossido di un non metallo) con l'acqua.
CO2 diossido di carbonio (o anidride carbonica) + H2O H2CO3 acido carbonico H H H O C + C H O
SO 3 + H2O -> H2SO acido solforico triossido di zolfo (o anidride solforica) + acqua H H O O S + O S O H H + acqua
Basi
Anche le basi sono sostanze familiari. Alcune le usiamo per pulire la casa, come l'ammoniaca. Sono sostanze che possono bruciare la pelle.
Facendo reagire un ossido basico (ossido di un metallo) con l'acqua, si ottiene una base o idrossido.
CuO ossido di rame + HO acqua Cu(OH)2 idrossido di rame H H O Cu + O Cu H C H
Na,O ossido di sodio + H2O -> + acqua -> 2NaOH idrossido di sodio (soda caustica) Na Na O H H O Na + O H Na O H +
Il pH
La dissociazione
Gli acidi e le basi sono generalmente composti ionici; i legami fra i loro atomi sono legami ionici. Quando un acido o una base vengono messi in acqua, questi legami ionici si rompono (dissociazione), liberando ioni che danno proprietà particolari alle soluzioni in cui si trovano.
I composti acidi liberano in acqua ioni H+ e la soluzione che ne risulta diventa acida. I composti basici liberano ioni OH- e la soluzione diventa basica. Anche la molecola dell'acqua si separa in ioni H+ e OH-, ma se all'acqua pura non viene aggiunta nessun'altra sostanza, la quantità di ioni positivi e negativi è uguale: H+ = OH -.
+ In queste condizioni ci dira cho l'acqua è neutra. cloridrico Na A Idrossido di sodio H2O Molecola di acqua H+ lone idrogeno OH lone ossidrile La dissociazione di un acido. CI lone ossidrile La dissociazione di una base. Na + lone ossidrile O lone idrogeno lone Oidrogeno O C C La dissociazione dell'acqua. lone ossidrile lone O idrogeno In un bicchiere d'acqua solo poche molecole sono dissociate
Il pH: concentrazione degli ioni
Come facciamo a capire quanto è acida (o basica) una soluzione, cioè qual è la concentrazione degli ioni H+ e OH ? Un modo per esprimere queste concentrazioni è stato introdotto dal chimico danese Søren P. R. Sørensen: egli chiamò pH il numero che esprime la concentrazione degli ioni H+, in una scala che va da 0 a 14. Secondo questa scala le sostanze acide hanno valori di pH compresi tra 0 e 7, quelle basiche hanno valori di pH compresi tra 7 e 14, quelle neutre (come l'acqua pura) hanno pH esattamente uguale a 7.
LA SCALA DI PH ammoniaca succo gastrico mela acqua distillata bicarbonato di sodio latte uovo sapone mani prodotti per la pulizia 1 2 3 4 5 6 7 8 9 10 11 12 13 14 NEUTRO ACIDO FORTE BASE FORTE caffè idrossido di sodio succo di limone pomodoro
Il pH: indicatori
Per sapere se si è in presenza di una base o di un acido si possono usare gli indicatori, particolari sostanze che hanno la proprietà di cambiare colore a seconda del pH.
Un indicatore di uso molto comune è il tornasole, un composto di origine vegetale con cui vengono imbevute strisce di carta che si colorano di rosso in ambiente acido e di blu in ambiente basico. Più il colore è intenso e più l'acido o la base sono forti.
Con l'acqua e i sali neutri la cartina non si colora.
ACETO Sapon liquid SODA CAUSTICA
Sali
Il sale è un composto che si ottiene facendo reagire un acido e una base.
Il sale più noto è il cloruro di sodio, il sale da cucina, NaCI, che si trova nell'acqua di mare o, come minerale, nei giacimenti di salgemma.
Un altro esempio di sale è il carbonato di calcio, che è un costituente di molte rocce.
H H Cl + Na OH Na + 0 Cl H Carbonato di calcio.