Capitolo 1: Struttura dei Metalli, Legami Atomici e Reticoli Cristallini
Documento di Chimica sull'analisi della struttura dei metalli, dei legami atomici e delle deformazioni dei reticoli cristallini. Il Pdf, utile per lo studio universitario, descrive i legami ionici, covalenti e metallici, i reticoli cristallini e le loro deformazioni, con un focus specifico sul caso del ferro.
Mostra di più9 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
STRUTTURA DEI METALLI
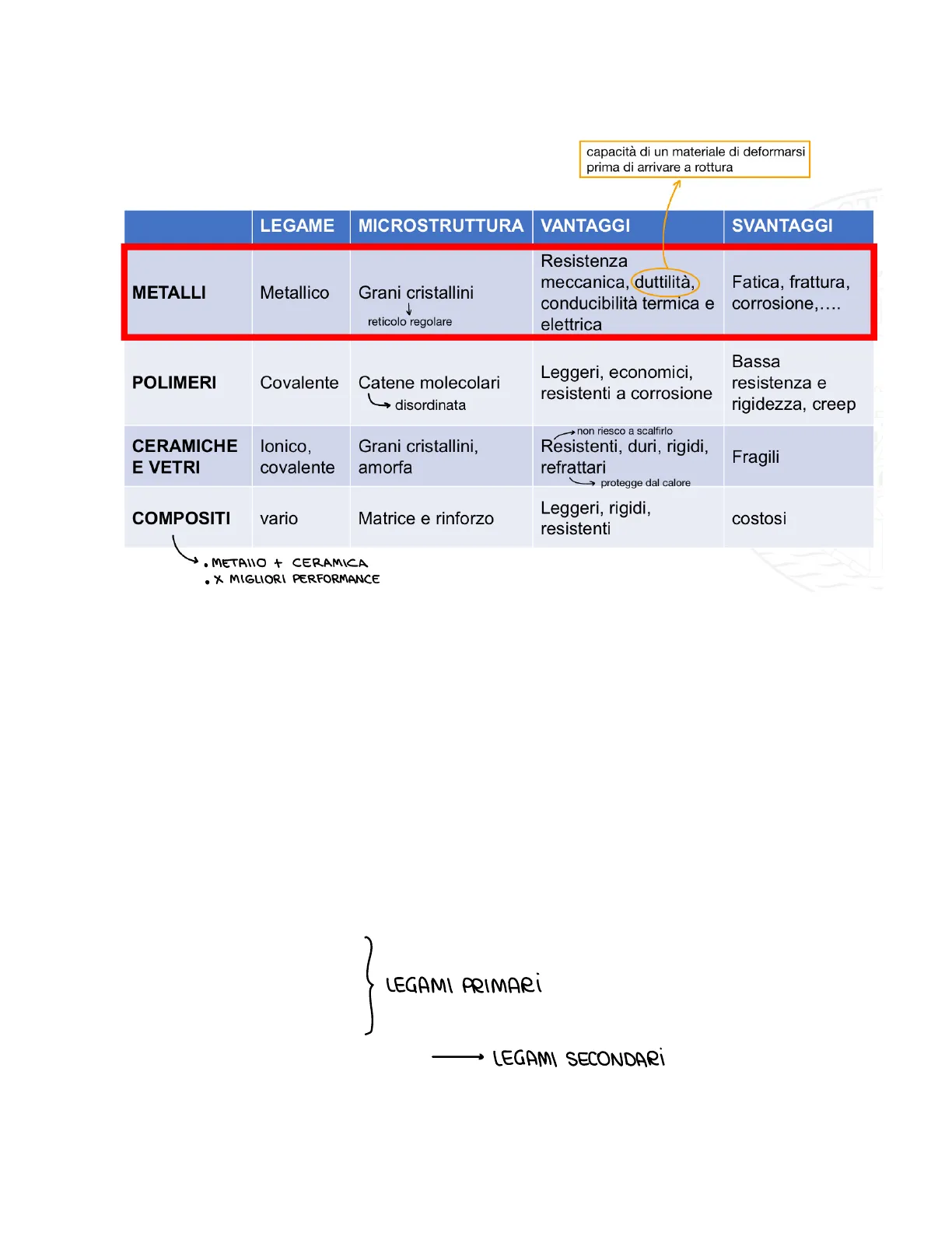
Possiamo suddividere i materiali in 4 categorie:
capacità di un materiale di deformarsi
prima di arrivare a rottura
LEGAME
MICROSTRUTTURA
VANTAGGI
SVANTAGGI
METALLI
Metallico
Grani cristallini
reticolo regolare
Resistenza
meccanica, duttilità,
conducibilità termica e
elettrica
Fatica, frattura,
corrosione, ....
POLIMERI
Covalente
Catene molecolari
disordinata
Leggeri, economici,
resistenti a corrosione
Bassa
resistenza e
rigidezza, creep
CERAMICHE E VETRI
lonico,
covalente
Grani cristallini,
amorfa
› non riesco a scalfirlo
Resistenti, duri, rigidi,
refrattari
Fragili
› protegge dal calore
COMPOSITI
vario
Matrice e rinforzo
Leggeri, rigidi,
resistenti
costosi
>. METALLO + CERAMICA
. X MIGLIORI PERFORMANCE
Fatica di un materiale = progressiva degradazione di un materiale sottoposto a carichi variabili nel
tempo che può portare alla sua rottura;
Creep=deformazione permanente di un materiale sottoposto per un certo periodo di tempo ad alte
temperature, a sforzi costanti o a sollecitazioni dovute al peso;
Amorfa=molecole distribuite in modo casuale
I LEGAMI ATOMICI
La struttura e le proprietà di un materiale dipendono dalla natura dei legami atomici.
I principali legami atomici sono:
- Legame ionico
- Legame covalente
1
1
LEGAMI PRIMARI
3. Legame metallico
7
4. Legame di Van der Waals
LEGAMI SECONDARI
la formazione dei legami atomici prevede il coinvolgimento degli elettroni di valenza degli atomi,
cioè quelli che occupano i livelli energetici più esterni. Quando i livelli energetici esterni non sono
completamente occupati, l'atomo ha una configurazione instabile e perciò tende ad assumere una
configurazione più stabile cedendo o acquisendo o condividendo elettroni.
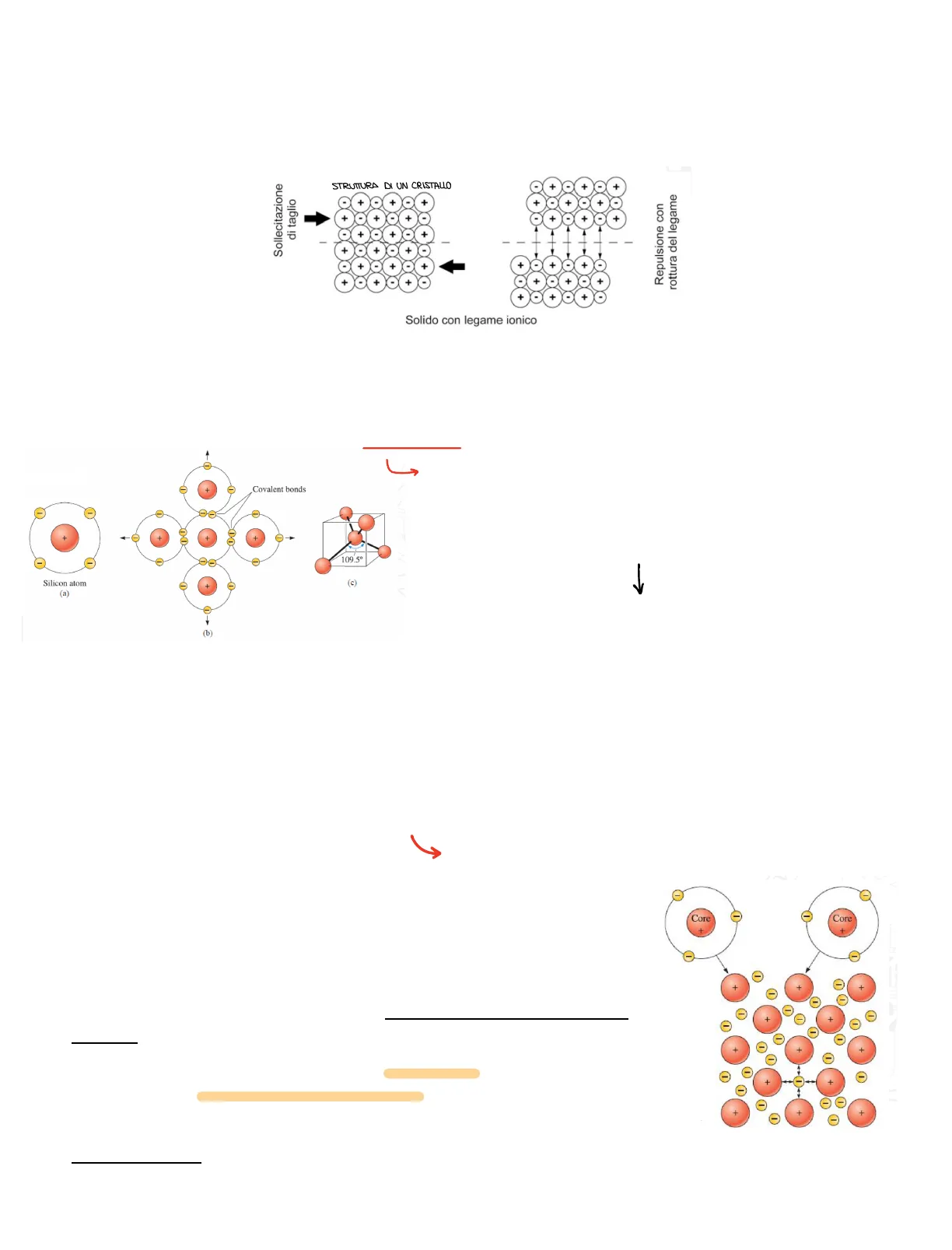
Legame ionico
- È presente nei composti formati dall'unione di un metallo di un non metallo (NaCl)
- Le forze attrattive sono di tipo columbiano, adirezionali.
- L' elettrone viene ceduto da un atomo e acquisito da un altro atomo.
Sollecitazione
STRUTTURA DI UN CRISTALLO
+
+
+
di taglio
+
+
+
+
+
+
+
+
-
+
+
-
+
+
+
+
+
-
+
-
+
-
+
Repulsione con
rottura del legame
Solido con legame ionico
Legame covalente
- Si stabilisce in seguito alla condivisione di alcuni elettroni da parte di atomi adiacenti (CH4).
- Le forze attrattive sono di tipo direzionale
- struttura che occupa un volume in tre dimensioni
- atomi disposti in una certa direzione
- atomi posti ai vertici => angolo fisso
+
+
- struttura inscritta in un cubo
-
Silicon atom
(a)
Struttura con geometria e orientazione nello spazio
Legame metallico
- prevede la condivisione degli elettroni da parte di più atomi;
- gli elettroni di valenza non sono legati ad un particolare atomo della struttura ma sono in
grado di spostarsi all'interno dell'intera struttura metallica;
MARE DI ELETTRONI o NUVOLA ELETTRONICA - gli elettroni liberi schermano le cariche positive degli ioni
che altrimenti si respingerebbero e formano un collante per
trattenere insieme gli ioni positivi;
Per gli elettroni liberi i metalli sono buoni conduttori termici ed
elettrici
-> vale principalmente per i metalli puri perchè hanno
una struttura molto omogenea
D
Core
I
Core
+
+
-
+
+
-
+
+
+
-
+
buona duttilità perchè il legame metallico è adirezionale (non c'è una direzione preferenziale)
Covalent bonds
109.5°
(c)
(b)
+
+
+
+
RETICOLI CRISTALLINI
quando abbiamo molti atomi, come si dispongono?
I solidi possono essere classificati in base alla disposizione degli atomi nello spazio:
> solidi cristallini : con un reticolo cristallino e una geometria precisa (metalli), a loro
volta classificati in base al tipo di reticolo che influenza le proprietà;
> solidi amorfi : disordinati (vetri, ceramiche);
> solidi a struttura mista : (polimeri).
Nei materiali gli atomi si dispongono nello spazio in posizioni regolari e periodiche secondo
precise simmetrie (reticolo cristallino)
ci permette di dedurre le proprietà macroscopiche
-> materiali con la stessa composizione chimica possono avere proprietà diverse perché
varia la struttura e dunque il reticolo
> cella elementare
nei solidi cristallini si può individuare la ripetizione delle caratteristiche geometriche di legame
secondo un certo modulo o unità ripetitiva, detta cella
elementare o unitaria.
mi permette di suddividere la struttura tante unità ripetitive e
capire che reticolo cristallino ha il materiale considerato
> come si rappresentano?
Modello delle sfere rigide
considera gli atomi come sfere in
contatto le une con le altre
Modello delle sfere ridotte
considera gli atomi come punti
coincidenti con la loro posizione
centrale (più facile da visualizzare)
Strutture dei reticoli
le strutture più comuni per i metalli sono 3 :
- Reticolo cubico a facce centrate (C.F.C.);
- Reticolo cubico a corpo centrato (C.C.C.);
- Reticolo esagonale compatto (E.C.).
La maggior parte delle strutture cristalline dei metalli è caratterizzata da una buona duttilità
Reticolo cubico a facce centrate (C.F.C.)
- 8 atomi ai vertici;
- 6 atomi al centro di ogni faccia;
- più densa/compatta;
- più deformabile;
- Alluminio, Argento, Rame, Ferro (y) ...
Reticolo cubico a corpo centrato (C.C.C.)
- 8 atomi ai vertici;
- 1 atomo al centro del cubo;
- Ferro (d), Cromo ...
Reticolo esagonale compatto (E.C.)
H
T
0
DI
B
A
- 6 atomi alla base;
- 1 atomo al centro di ogni base;
- poco deformabile;
- 3 atomi al centro a metà altezza della struttura;
- Zinco, Titanio, Cobalto, Magnesio ...
IL CASO DEL FERRO
il ferro può cambiare struttura in funzione della sua temperatura
a temperatura ambiente è caratterizzato da un reticolo cubico a corpo centrato : FERRO (y).
una volta scaldato cambia il reticolo cristallino e diventa a facce centrate : FERRO (a), più
deformabile
Deformazione dei reticoli
avviene come scorrimento di atomi lungo alcuni piani e direzioni preferenziali, che sono quelli a
maggiore densità atomica
F
Î
PIANO DI
SCORRIMENTO
TIRO UN FILO METALLICO
VOLUME SI E SPOSTATO
1
STRUTTURA SCORRE LUNGO
IL PIANO
F
F
Il numero di queste direzioni varia a seconda del reticolo cristallino
1
2
B
3
Reticolo (c.f.c.) e (e.c.)
3 direzioni
1
2
A
A
A
A
A
A
A
Reticolo (c.c.c)
2 direzioni
La combinazione del piano di scorrimento e della direzione di scorrimento viene definita
sistema di scorrimento
! NO MEMORIA
Tipo di reticolo
nº piani di
scorrimento
nº direzioni di
scorrimento
nº sistemi di
scorrimento
Reticolo e.c.
1
3
3
Reticolo c.f.c.
4
3
12
Reticolo c.c.c.
6
2
12
RSITA
-> i materiali con reticolo E.C. sono poco deformabili
-> il reticolo C.F.C. è quello più deformabile perché rispetto al reticolo C.C.C. ha un maggiore
numero di direzioni di slittamento e richiede minore energia per lo scorrimento dei piani
atomici
DIFETTI RETICOLARI
= fattore di disturbo della periodicità tridimensionale degli atomi o degli ioni in un reticolo
cristallino ideale
-> irregolarità che influenzano le proprietà dei metalli
> spesso utilizzati per creare leghe metalliche
I principali sono:
- Difetti di punto;
- Difetti di linea;
- Difetti di superficie;
- Difetti di volume.
Difetti di punto
il più semplice tra questi è la vacanza reticolare
= DELLO STESSO
1 ELEMENTO
un atomo autointerstiziale
è un atomo che si trova
stipato un un piccolo spazio
del reticolo cristallino
normalmente vuoto
Self-interstitial
Vacancy
H
1
i metalli, anche quelli "puri",
contengono sempre delle
impurezze o atomi estranei
nelle leghe vengono aggiunte
per migliorare le proprietà
Gli atomi sfruttano gli spazi interstiziali o le vacanze reticolari:
VACANZE RETICOLARI
Atomo interstiziale
DI UN ELEMENTO
DIVERSO
Atomo sostituzionale
(piccolo)
Atomo sostituzionale
(grande)
La presenza di atomi di altri elementi introduce delle deformazioni del reticolo
Elementi di lega e impurezze
Se aggiunto elementi di lega nel metallo puro e questo contiene delle impurezze mi si
presentano 3 possibilità:
- si forma una soluzione solida
- si formano dei composti: gli atomi si
dispongono ordinati e in rapporto
stechiometrico, il reticolo cristallino è diverso
da quello del materiale di base, non sono più
legati dal legame metallico.
Si verifica se supero il limite di miscibilità e
aggiungo troppo materiale
B
A
Soluzione solida
di A e B
Composto di
A e B - gli elementi rimangono separati nella lega: immiscibilità
-> soluzioni solide
sono spesso presenti nelle leghe metalliche
Viene considerata una soluzione cristallina quando la
struttura cristallina del solvente rimane inalterata dopo
l'aggiunta del soluto.
= miscela omogenea
Substitutional
impurity atom
Interstitial
Impurity atom
# dai composti in quanto nel caso di un composto nel
reticolo vi sono 2 o più tipi di atomi diversi e sono disposti in
modo ordinato, con un reticolo diverso da quello del materiale di base
Possono essere:
> sostituzionali = la struttura cristallina rimane inalterata, le
dimensioni della cella unitaria variano progressivamente
con l'aggiunta di soluto, fino a raggiungere una variazione
massima.
! spesso la massima solubilità del soluto è limitata, e se
dovesse essere superata si può formare un composto
O
Atomo di solvente - ALLUMINIO
Atomo di soluto - SILICIO
> interstiziali = gli atomi del soluto sono sufficientemente
piccoli da poter occupare i vuoti tra gli atomi del solvente,
all'interno del reticolo cristallino.
elementi non metallici con dimensioni sufficientemente
piccole da creare soluzioni interstiziali : C, N, H, ...
La massima frazione di soluto che può sciogliersi nel
solvente è generalmente piccola e dipende dagli spazi disponibili nel solvente
Difetti di Linea
una dislocazione è un difetto lineare attorno a cui gli atomi sono fuori posto e che può
spostarsi nel reticolo sotto l'azione di sforzi applicati creando una deformazione del reticolo
== > è il loro movimento a rendere possibile la deformazione plastica
Burgers vector
b
UN
Edge
dislocation
line
1
può essere a spigolo, a vite oppure mista
Le dislocazioni possono spostarsi nel reticolo sotto l'azione di sforzi applicati.
Shear stress
Shear stress
Slip
plane
-
(a)
(b)
(c)
(d)
IL LEGAME TENDE A ROMPERSI > NUOVI LEGAMI LA DISLOCAZIONE SI SPOSTA
Le dislocazioni possono essere considerate come piani incompleti di atomi
Movimento dislocazioni == > scorrimento fra i piani => deformazione plastica permanente
Si applica uno sforzo ~ ad un cristallo contenente una dislocazione,
questa può muoversi e rompere i legami fra atomi di un piano
il piano tagliato si muove e stabilisce nuovi legami
processo continua finchè la dislocazione attraversa il
cristallo, che viene deformato in modo permanente