Ciclo cellulare: complessi ciclina-Cdk e ruolo della proteina p53
Documento da Sapienza Università di Roma su Ciclo Cellulare (terza Parte). Il Pdf, di livello universitario e incentrato sulla Biologia, esplora il ciclo cellulare, i complessi ciclina-Cdk e la regolazione tramite fosforilazione, con schemi esplicativi sul controllo e la risposta al danno del DNA.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Sapienza Università di Roma
Facoltà di Farmacia e Medicina
Corso di laurea magistrale a ciclo unico in Medicina e chirurgia "A" A.A. 2024/2025 Lezione di: biologia 10/03/2024 1° ora (11:00-12:00) Docente: prof.ssa Amicone Sbobinatore: Alessandra Cinti Revisore: Tania Abdul
Ciclo cellulare (terza parte)
La professoressa prima di iniziare gli argomenti della lezione fa un riepilogo degli argomenti affrontati nelle due lezioni precedenti sul ciclo cellulare. avvio del'apparato mitotico
- M-Co ciclina M O M Odk mitotica Ook inattiva Có inattiva G S di fase & O S-Cdk cicira $ joão del'apparato replicativo
Abbiamo parlato dei complessi ciclina Cdk, abbiamo visto facendo l'esempio del complesso ciclina Cdk di fase M, come questi complessi possano essere controllati nella loro funzione catalitica che è quella chinasica, in cui ritroviamo tutto un gioco di fosforilazioni attivatrici , inibitorie, di attività di fosfatasi, di proteine che possono associarsi e possono inibire i complessi etc. quindi un multilivello di regolazione che può variare in base al complesso che stiamo considerando.
Noi abbiamo preso come esempio, con dei nomi specifici delle molecole che lavorano ,il complesso ciclina Cdk di fase M, quello della ciclina B Cdk nei mammiferi. Questo discorso può valere però per varie cicline e complessi cicline Cdk, abbiamo capito l'armonia con cui questi complessi si formano e si inattivano a mano a mano che procede il ciclo cellulare. Il modo in cui i vari complessi si sostituiscono tra loro con un armonico passaggio unidirezionale da una fase all'altra del ciclo.
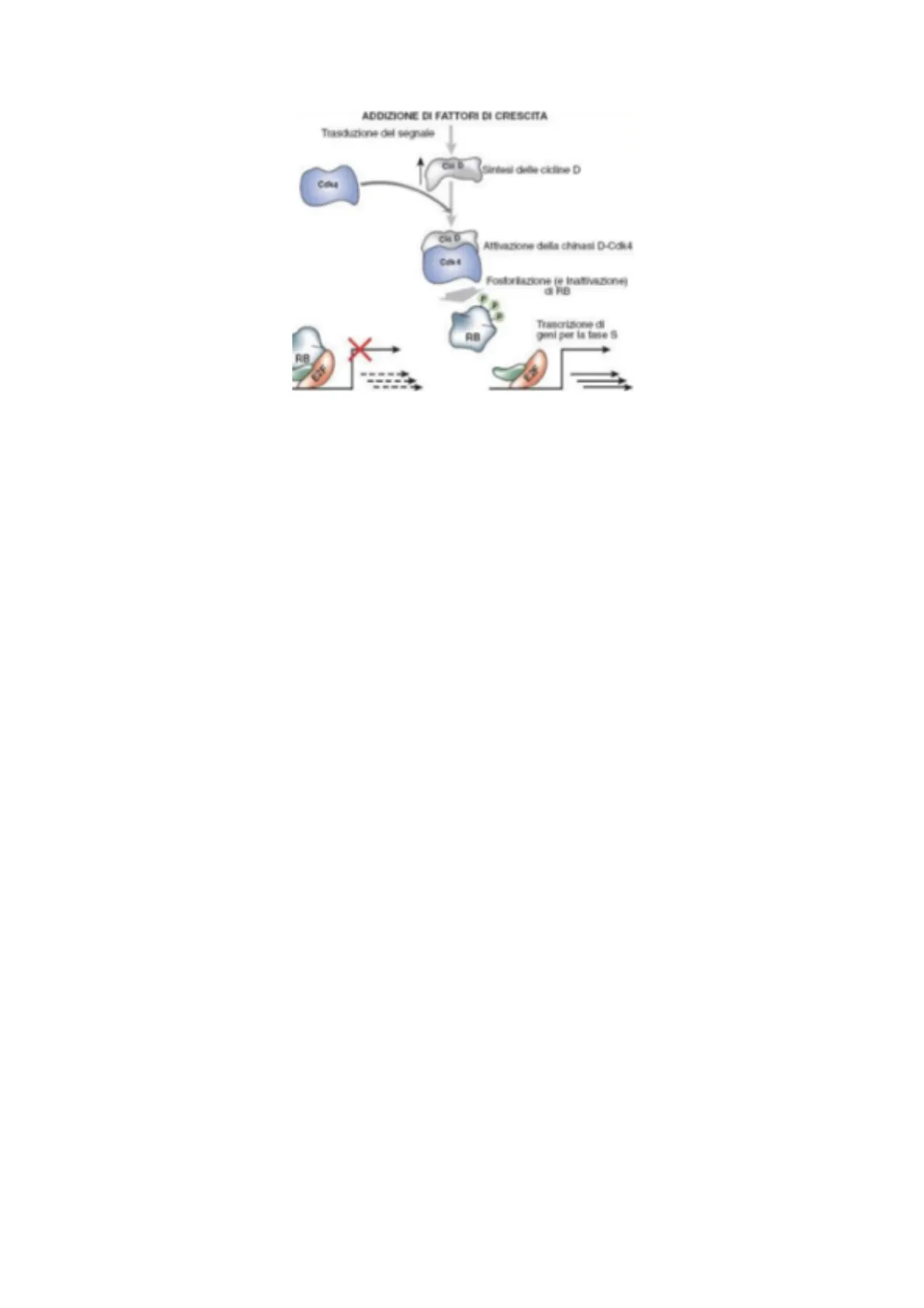
Siamo arrivati a capire , o meglio iniziare a capire, come poi questa attività chinasica, questa attività fosforilante abbia un effetto, cioè quali sono i target e quindi gli effetti della fosforilazione su questi target e come si traducono negli eventi del ciclo cellulare (duplicazione DNA e le fasi in cui c'è maggiore necessità di controllo come la fase S e la fase mitotica).ADDIZIONE DI FATTORI DI CRESCITA Trasduzione del segnale Sintesi delle cicline D Cou Attivazione della chinasi D-Cdk4 Fostortazione (e Inattivazione) a RB RB Trascrizione di geni per la fase S RB
Target dei complessi ciclina Cdk
Abbiamo cominciato a vedere un po' quali sono i target di questi complessi ciclina Cdk. Abbiamo iniziato con quelli della fase G1 che vanno a controllare questa famosissima proteina, una delle prime proteine caratterizzate in senso oncosoppressivo (in senso inibitorio del ciclo cellulare), ovvero Rb (retinoblastoma), la cui fosforilazione sta a valle di una serie di processi, i quali in una cellula che fino in quel momento stava in G0, dipendono dall'attivazione dei recettori che si legano a dei fattori di crescita e che quindi stanno rispondendo a stimoli esterni e finiscono con la fosforilazione di questo Rb, proteina che è stata legata ad un fattore trascrizionale. Quando viene fosforilata si stacca e inizia un programma di espressione genica e quindi la trascrizione di geni che sono correlati al ciclo cellulare permettendo l'entrata in fase S.
I complessi ciclina CDK della fase G1 tardiva sono quelli che essenzialmente sono caratterizzati dal legame con una particolare ciclina, la ciclina E, tipica del passaggio G1/ S e della fase S.
- cosa succede nella fase S? Questa ciclina va innanzitutto a fosforilare uno degli inibitori di altri complessi ciclina Cdk, andando a legare delle proteine inibitrici. Queste proteine inibitrici stanno in fase S tenendo sottocontrollo alcuni complessi ciclina Cdk che devono essere attivati quando è ora. E lo fa proprio l'attività fosforilante dei complessi ciclina Cdk precedenti che vanno a fosforilare questi inibitori e li fanno staccare o li mandano in degradazione e quindi si liberano quelli che poi effettivamente dovranno lavorare nella replicazione del DNA.
- Cosa fanno questi fattori che poi vengono attivati? Possono essere attivati anche da un punto di vista trascrizionale cioè si attivano i geni che codificano per esempio per gli enzimi che servono per la sintesi dei nucleotidi oppure la sintesi delle proteine che compongono i grossi complessi della DNA polimerasi. Cominceranno inoltre a trascrivere i successivi geni che servono per la progressione per il ciclo cellulare.
Controllo dell'ORC
L'altra volta abbiamo fatto un esempio: abbiamo iniziato a capire il controllo del cosiddetto ORC ( Complesso di Riconoscimento dell'Origine ), un importante complesso molecolare fatto di tante proteine che si siede sulle ARS, origini di replicazione multiple soprattutto in individui con un genoma complesso come i mammiferi. E' la regolazione per fosforilazione di alcuni componenti della ORC che la rendono , fino ad un certo punto la possiamo definire come una pre -ORC perché ancora non funziona, un vero e proprio complesso di replicazione attivo e anche qui è importante l'utilità della fosforilazione dei complessi ciclina Cdk, poiché essi sono importanti per la fosforilazione di alcuni di questi componenti, alcuni dei quali dopo la fosforilazione si devono spaccare e devono liberare in qualche modo l'attività di questo complesso di replicazione.
Altre fosforilazioni sono invece quelle attivanti, principalmente quelle che riguardano l' elicasi, quindi i target delle fosforilazioni dei complessi ciclina Cdk sono sia i componenti che stanno tenendo fermo il complesso di replicazione, sia le fosforilazioni che vanno a lavorare sulle MCM, nome delle elicasi in questi complessi eucariotici superiori, che invece devono essere attivate.
- Cosa succede quando tutto si stacca e le MCM si attivano? ORC MCM G ORC MCM DINA Polimerasi S MCM M
Comincia la replicazione del DNA. Intanto le altre cicline Cdk hanno provveduto alla sintesi degli altri componenti, inizia la replicazione del DNA sulle molecole di DNA di sintesi, si organizza un pre ORC con ancora l'impegno delle MCM nell'apertura della doppia elica dei vari repliconi. Si arriverà alla fase M in cui una fosforilazione a questo punto, o meglio iperfosforilazione delle MCM da parte dei complessi ciclina Cdk di fase M le faranno staccare. Finita la replicazione di DNA.
Nella G1 delle cellule cicliche a mano a mano che scende l'attività chinasica e quindi agisce un'attività fosfatasica costitutiva si ripristina una situazione iniziale, si riattacca tutto , gli MCM ed altri complessi e siamo pronti ad affrontare una nuova fase S. Quindi si tratta di un gioco armonico di fosforilazione.
Se ci pensate bene quello che abbiamo descritto è un meccanismo che garantisce che tutto questo processo avvenga in una maniera temporalmente coordinata. Cosa garantisce? Che questi complessi si formino e agiscano una sola volta per ciclo cellulare.
Regolazione della duplicazione del DNA
E quindi impediscono che il DNA di una cellula in fase S si duplichi più di una volta. Perché gli ORC si vanno a ricostituire sulle molecole di DNA.
Facciamo altri esempi di attività ciclina Cdk che lavorano su cose:
per esempio, I'MPF, il nome che viene dato a questo complesso si basa sugli esperimenti fatti in rana, quando si parla di MPF che originariamente significava maturation promoting factor, in cui successivamente la M è diventata mitosis , mitosis promoting factor, è il complesso ciclina Cdk di fase M, quindi quello con la ciclina B. In questa fase la fosforilazione del tratto di questo complesso incide molto su delle proteine che lavorano sulla condensazione dei cromosomi, sulla forma del fuso mitotico e che sono importanti per la frammentazione dell'involucro nucleare, che nella fase M si deve disgregare per permettere che i cromatidi fratelli si separino e raggiungano l'estremità della cellula per poi riorganizzarsi nei cromosomi monocromatidici che formeranno poi il contenuto nei nuclei.
Frammentazione della membrana nucleare
Facendo riferimento a quest'ultimo aspetto, la frammentazione della membrana nucleare. Quali sono i target dell'MPF? Le famose lamine nucleari (quando abbiamo parlato della lamina nucleare abbiamo parlato delle lamine nucleari, le proteine che costituiscono la struttura che sta internamente al nucleo sotto la membrana nucleare). La fosforilazione tramite I'MPF di queste lamine determina una destabilizzazione della membrana e lavora molto nella direzione della frammentazione della membrana stessa nel momento in cui si devono separare i cromatidi fratelli.
- Quello che accade in realtà è un processo molto ordinato: La membrana nucleare si frammenta per poi riorganizzarsi sia per coalescenza di questi frammenti di membrana sia per l'intervento del RER, si riorganizzera la membrana nucleare prima intorno addirittura ai singoli cromosomi a formare i cariomeri, per poi avere la coalescenze delle membrane di questi cariomeri per formare i nuclei delle cellule figlie. Quindi anche questi processi sono figli di un'attività chinasica di un complesso ciclina Cdk.
E poi i cromatidi fratelli non si separano finché non è tutto pronto. C'è anche qui un controllo di un complesso ciclina Cdk sul far separare i cromatidi fratelli nel momento in cui si possono separare e possono migrare per trazione di quella componente microtubulare del fuso mitotico.
In questo gioco abbiamo già visto all'inizio chi interviene : Interviene il famoso APC ( Anaphase -Promoting Complex ) , la cui componente essenziale è una ubiquitina ligasi che viene attiva da chi?
- Dai complessi ciclina cdk, per fosforilazione. Si attiva la sua attività ubiquitina ligasi che legando uno specifico cofattore, che abbiamo detto essere all'inizio CDK1, che rende specifica l'attività di poliubiquitinazione su un inibitore di una separasi, che è questa proteasi che digerisce le coesine, cioè le proteine che tengono insieme i cromatidi fratelli.
Quindi si ha l'attività chinasica del complesso ciclina Cdk , l'attivazione dell'APC , l'APC che si lega al cofattore con una specificità di azione di poliubiquitinazione , si separano i cromatidi fratelli , l'APC cambia poi cofattore e si lega a cdc2 che sarà invece il cofattore che rende specifica la poliubiquitinazione sulla stessa ciclina che nel complesso ciclina Cdk ha attivitato l'APC. In seguito a questo processo la cellula è pronta ad uscire dal ciclo.
- Vediamo quindi come queste attività di fosforilazione hanno degli effetti: Ci sono anche altri target ancora più avanti, nel momento della citodieresi. Vengono fosforilate delle componenti di proteine motrici, per esempio I'MPF fosforila la catena leggera della miosina che fino ad un certo punto deve essere tenuta sotto controllo perché legandosi all'actina farebbe la citochinesi. Ma poi la ciclina B viene degradata, questa fosforilazione diminuisce, la miosina si attacca all'actina e lavora su quella parte finale della citodieresi, ovvero quella della separazione dei citoplasmi, processo finemente e temporalmente controllato.
Mitosi senza citochinesi
Descrizione di uno fenomeno che avviene all'interno della cellula tramite l'immagine : L'immagine mostra che in alcune situazioni possono avvenire delle mitosi nella stessa cellula senza citochinesi. Vediamo una serie di nuclei che sono tutti figli di una cellula, cosa molto particolare che avviene nell'embrione precoce di Drosophila. Sono una serie di mitosi non seguite da citodieresi e si avrà un'organizzazione della cellula attorno a tutte le mitosi soltanto in una fase successiva.
Ci sono delle situazioni anche nell'uomo, in alcuni tessuti, in cui può verificarsi effettivamente una duplicazione del DNA senza citodieresi. Un esempio è il fegato. Il fegato adulto è caratterizzato da una situazione cromosomica strana. Se si va a fare un cariotipo, quindi una mappa cromosomica, vediamo che non è regolare. Tanto che la maggioranza degli epatociti maturi ha un corredo cromosomico particolare ( il termine usato dalla professoressa più volte per definire il particolare corredo cromosomico degli