Modello atomico: elementi, composti e particelle elementari della materia
Slide sul modello atomico che distingue tra elementi e composti, spiegando le particelle elementari della materia. Il Pdf, pensato per la scuola superiore, illustra il linguaggio simbolico della chimica per rappresentare le particelle e facilitare la comprensione dei concetti fondamentali della materia.
Mostra di più11 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Elementi e Composti
A cura della prof.ssa A. Naglieri
MODELLO ATOMICO
Gli elementi e i composti
- Le sostanze pure formate da componenti più semplici si chiamano composti.
- Le sostanze che non possono essere trasformate, con gli ordinari mezzi chimici, in sostanze più semplici si chiamano elementi.
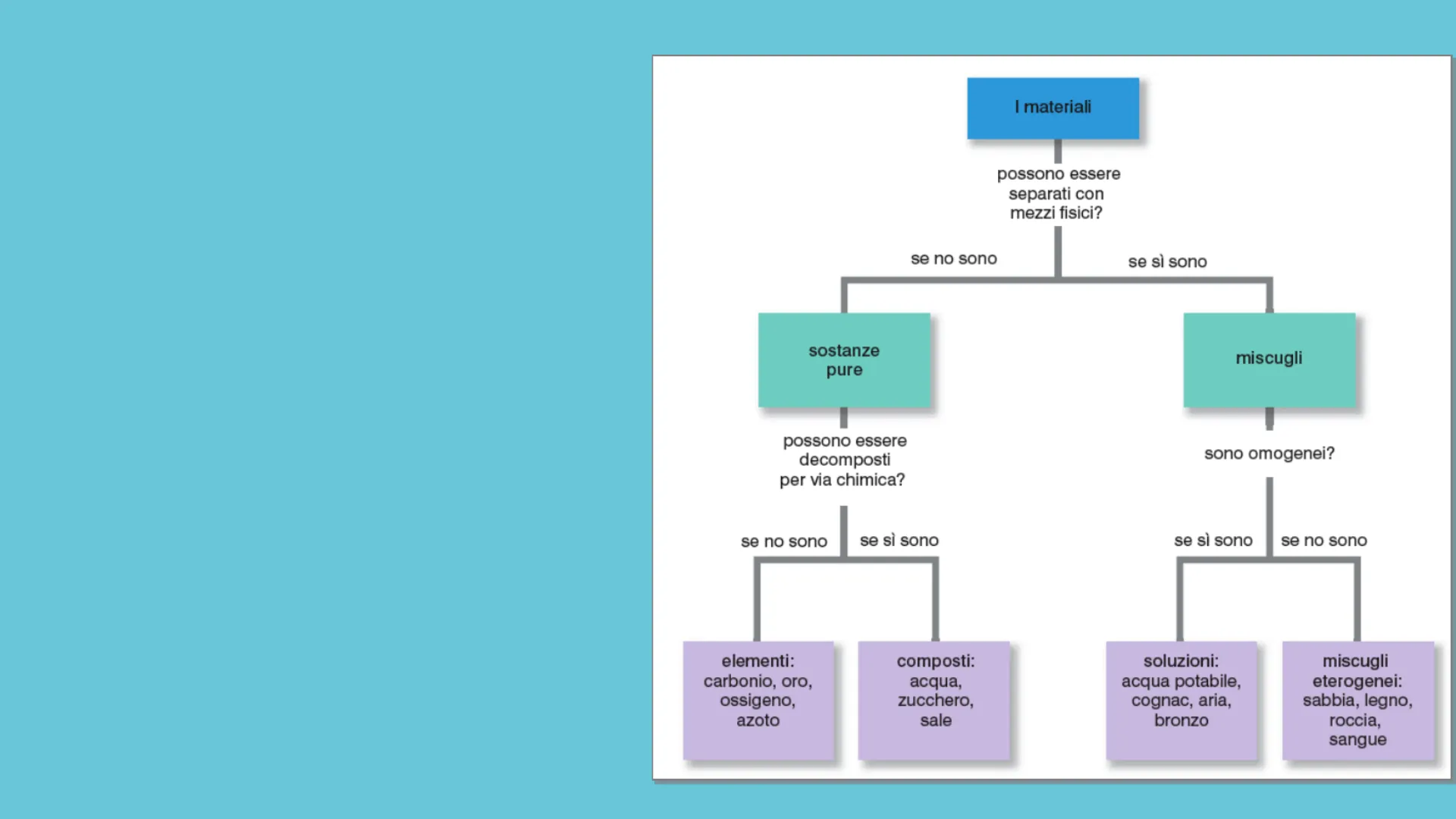
I materiali possono essere separati con mezzi fisici?
se no sono se sì sono
miscugli sono omogenei?
se sì sono se no sono
elementi: carbonio, oro, ossigeno, azoto
composti: acqua, zucchero, sale
soluzioni: acqua potabile, cognac, aria, bronzo
miscugli eterogenei: sabbia, legno, roccia, sangue
sostanze pure
possono essere decomposti per via chimica?
se no sono se sì sono
Teoria Atomica di Dalton
Ipotesi del Modello Atomico
Nel 1803 John Dalton ipotizzò il primo MODELLO ATOMICO sulle basi sperimentali degli studi di Antoine Lavoisier e di Joseph-Louis Proust.
La sua teoria si basa sui seguenti punti:
«la materia è fatta di atomi piccolissimi che sono indivisibili e indistruttibili;
## tutti gli atomi di uno stesso elemento sono identici e hanno la stessa massa, atomi di elementi diversi sono diversi e hanno massa diversa;
H N CI
Principi della Teoria Atomica di Dalton
gli atomi di un elemento non possono essere convertiti in atomi di altri elementi;
N CI
## gli atomi di un elemento si combinano solo con numeri interi di atomi di altri elementi;
anidride carbonica metano
Trasferimento di Atomi
gli atomi non possono essere né creati né distrutti, ma si trasferiscono interi da un composto all'altro.
NO2 CO NO CO2
+ + REAGENTI PRODOTTI
Un atomo di ossigeno si trasferisce dall'azoto al carbonio
Conformità del Modello di Dalton alle Leggi Fondamentali
Il modello atomico di Dalton rispetta le leggi di Lavoisier e di Proust:
- La legge di Lavoisier è rispettata perché gli atomi dei reagenti si ritrovano nei prodotti, pertanto la massa si conserva
- La legge di Proust è coerente con il modello perché in un composto c'è un numero fisso di atomi di ciascun elemento, pertanto la composizione è costante
+ ferro zolfo solfuro di ferro
massa zolfo massa ferro = = 0,57
Le Particelle Elementari della Materia
Componenti Fondamentali
Le particelle che costituiscono la materia sono:
- ATOMI
- MOLECOLE
- IONI
- ATOMO La più piccola particella della materia che ne conserva le proprietà chimiche
- MOLECOLA Particella formata da due o più atomi legati. Molecola di elemento se gli atomi sono uguali, composto se sono diversi
- IONE Particella formata da uno o più atomi dotato di carica elettrica. Catione con carica positiva (+) Anione con carica negativa (-)
Molecole di Elementi
Esistono molecole formate da atomi dello stesso tipo come le molecole biatomiche (formate da due atomi) o poliatomiche (più di due atomi).
Si tratta di molecole di elementi
H2 O2 N2 Cl2
I2 S8 P 4
molecole biatomiche molecole poliatomiche
IDROGENO-AZOTO-OSSIGENO-FLUORO-CLORO-BROMO-IODIO
Molecole di Composti
Esistono molecole formate da atomi diversi.
Si tratta di molecole di composti
anidride carbonica metano
Composti Ionici
Ioni di carica opposta si attraggono per formare composti detti ionici, come nel comune sale da cucina (cloruro di sodio) formato da ioni Cl- e Na+
- catione Na+ + + I - + 1 + + + 1 + 1 + + 1 anione CI-
Il Linguaggio Simbolico: Rappresentazione delle Particelle
Formule Chimiche e Simboli
Le sostanze vengono rappresentate mediante formule chimiche in cui sono riportati i simboli del/degli elemento/i da cui sono formate, con dei pedici numerici che indicano il numero di atomi dell'elemento a cui si riferiscono:
Pedici
H2SO4 2 atomi di idrogeno, 1 di zolfo e 4 di ossigeno
Al2S3 1
Ca(OH)2 1 atomo di calcio, 2 di ossigeno e 2 di idrogeno
1 Simboli degli elementi
Fe2(CO3)3 3/3 2 atomi di ferro, 3 di carbonio e 9 di ossigeno
N.B. Il pedice fuori dalla parentesi è valido per tutto ciò che è in parentesi