Ammine: struttura, proprietà e reazioni di preparazione
Slide dall'Università San Raffaele su Ammine. Il Pdf è una presentazione universitaria di Chimica che esplora la struttura tetraedrica, le proprietà basiche e nucleofile, e i metodi di preparazione delle ammine, inclusa l'alchilazione diretta e la riduzione delle immine.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Università San Raffaele Roma
Professore Gilda Aiello
AmmineT
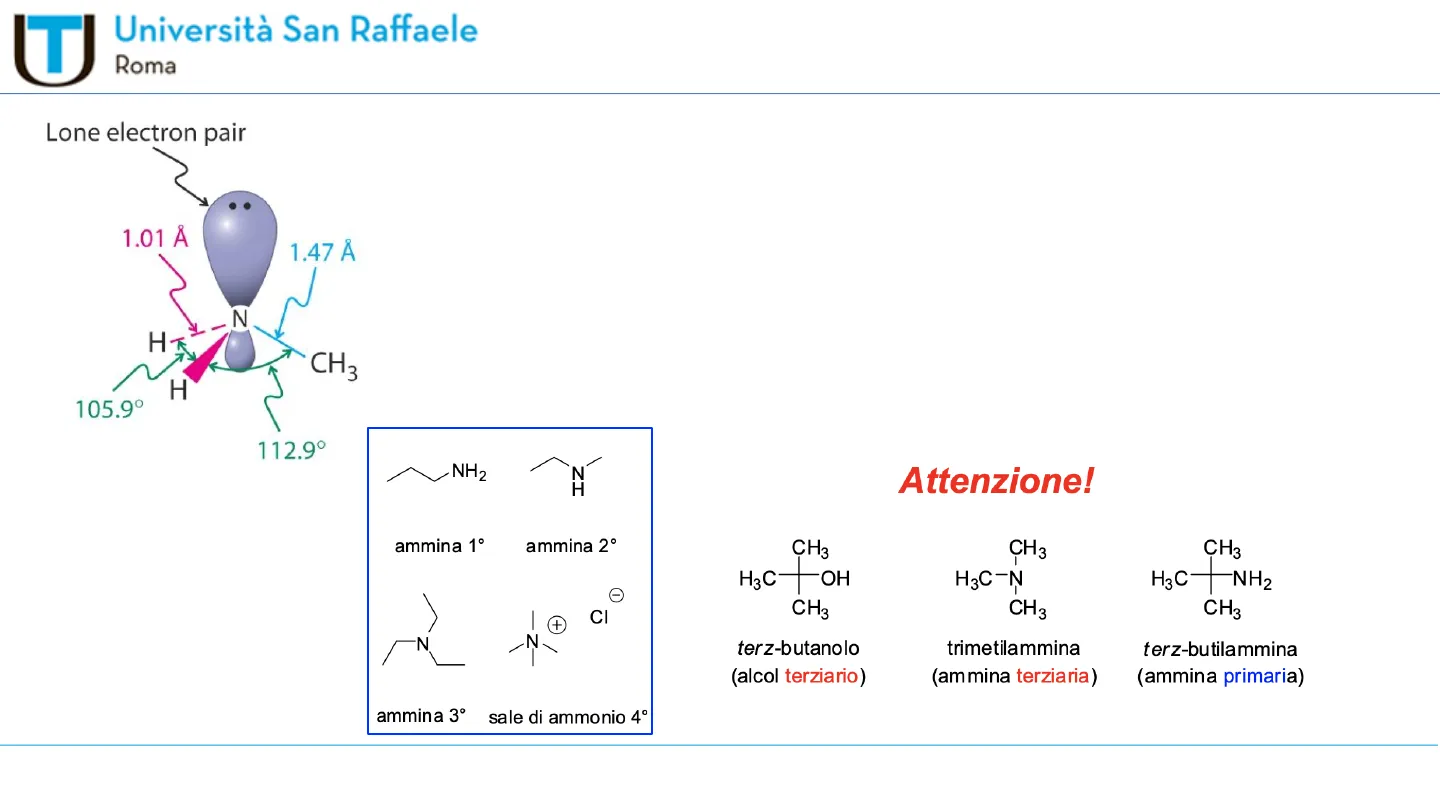
Lone electron pair
1.01 Å 1.47 Å - N HT CH3 H 105.9º
Ammine
Sono derivati dell'ammoniaca in cui uno o più idrogeni sono stati sostituiti da gruppi alchilici (R) o arilici (Ar). - azoto ibridizzato sp3. - geometria tetraedrica. - basiche e nucleofile: doppietto elettronico disponibile. 112.9º NH2 H ammina 1º ammina 2° O 1 CI N Z- / ammina 3º sale di ammonio 4°
Attenzione!
CH3 H3C-OH CH3 terz-butanolo (alcol terziario) CH3 H3C-N CH3 trimetilammina (ammina terziaria) CH3 H3CNH2 CH3 terz-butilammina (ammina primaria)
Nomenclatura delle ammine
Vengono comunemente utilizzati almeno 2 sistemi: · Nome sistematico: le ammine prendono il nome dell'alcano corrispondente aggiungendo il suffisso -ammina. · Nome comune: si elencano i gruppi legati all'azoto come sostituenti (alchil o aril) in ordine alfabetico e aggiungendo il suffisso -ammina H2 H3C 3 C 1 NH2 C 2 4 H2 0 H2 a 1º amine Sistematico Comune Butanammina N-butilammina 1 CH3 H3C-C-NH2 3 21 1 CH3 a 1º amine 2-metil-2-propanammina Terz-butilammina H2 H3C 2 C. 3 ~CH3 H2 1 H a 2º amine N-metilpropanammina N-metilpropilammina CH3 H3C-CH2-N: CH3 a 3º amine N,N-dimetiletanammina N,N-dimetiletilammina
Ammine 2° e 3º omosostituite
H N N diisobutilammina trietilammina Se NH2 è un sostituente viene chiamato gruppo ammino ŅH2 OH 2-ammino-1-pentanolo
Ammine cicliche alifatiche
N aziridina azetidina IZ pirrolidina IZ piperidina
Ammine aromatiche (arilammine)
ŅH2 anilina ŅH2 CH3 o-toluidina
Ammine eterocicliche
IZ N N N H pirrolo imidazolo indolo N N N N piridina pirimidina chino lina HNT
Composti azotati in natura
Con il termine alcaloidi si indica una grande varietà di composti basici azotati di origine vegetale molti dei quali risultano essere dotati di attività biologica. CH3 H3C Ń HO NH2 N H Serotonin an important neurochemical Caffeine Nicotine (tobacco) Muscarine (from Amanita muscaria) HO H CH30 0 H- -Na -H OH Quinine antimalarial Atropt belladonna Joel Raynaud NH2 CN-CH3 e N Ci S H2CM H3C (CH2)2-OH Atropine Thiamine vitamin B1 + CH340 0 wCH2-N(CH3)3 CI N N CH3 Nº OH CH3 CH2-OH H3C-IN C6H5 HO* Morphine (opium) analgesic
Proprietà fisiche: p.e. e legame idrogeno
Le ammine sono composti polari e sia le ammine primarie che quelle secondarie formano legami a idrogeno intermolecolari. Il legame a idrogeno N-H ---- N è più debole di quello O-H ---- O perché la differenza di elettronegatività tra l'azoto e l'idrogeno è minore di quella tra l'ossigeno e l'idrogeno. H3CH N „H H- N H CH3 H H N-H- N-CH3 H3C H
Conseguenze
I p.e. delle ammine sono decisamente inferiori a quelli degli alcoli a ugual peso molecolare Alcano Alcol Ammina 1° Alcano Alcol Ammina 1° Composto CH3CH3 CH3 OH CH3NH2 CH3CH2CH3 CH3CH2OH CH3CH2NH2 P.M. 30 32 31 44 46 45 p.e. ºC -88.6° 65° -6.0° -42° 78.5° 16.6° Poiché le primarie hanno due idrogeni disponibili per il legame a idrogeno si osservano punti di ebollizione maggiori rispetto alle secondarie e ancora maggiori rispetto alle terziarie che non hanno idrogeni disponibili. NB: La ramificazione riduce i punti di ebollizione. Alcol Ammina 1° Ammina 2° Ammina 1° ramificata Ammina 3° Composto CH3(CH2)2OH CH3(CH2)2NH2 CH3CH2NHCH3 (CH3)2CHNH2 (CH3)3N P.M. 60 59 59 59 59 p.e. º℃ 97º 48° 37° 34° 3º
Proprietà fisiche delle ammine
Le ammine sono più solubili in acqua degli idrocarburi a ugual peso molecolare. Le ammine a basso P.M. (meno di 5 atomi di carbonio) sono completamente solubili in acqua. Le ammine volatili hanno odori caratteristici spesso sgradevoli. H H 1 / H N-H H3C i N-H ammoniaca metilammina odore ammoniacale H3C IZ N-CH3 H3C trime tilammina piperidina odore di pesce Le ammine aromatiche come l'anilina sono tossiche e la loro pericolosità deriva dal fatto che possono essere assorbite attraverso la cute. NH2 NH2 anilina ß-naftilammina H2N NH2 1,5-pentandiammina detta cadaverina
Basicità delle ammine
Come l'ammoniaca tutte le ammine sono basi deboli e le loro soluzioni acquose sono basiche. Come di consueto l'equilibrio favorisce la formazione dell'acido e della base più deboli. CH3-N : I-Z-I H-O-H - CH3-N-H + :O-H CH3NH2 + H2O + 0 OH base più debole acido più debole pKa 15.7 acido più forte pKa 10.64 base più forte + CH3NH2 + CH3COOH CH 3NH3 + CH3COO O base più forte acido più forte pKa 4.76 acido più debole pKa 10.64 base più debole H H + CH3NH3T
Basicità delle ammine alifatiche
Tutte le ammine alifatiche hanno circa la stessa basicità e sono basi poco più forti dell'ammoniaca: NH2 エ ー .N 1 HH エ H CH3 N N pKb: 4.7 3.3 3.0 3.3 - basico + basico La carica positiva è parzialmente delocalizzata sul gruppo alchilico H 8+ 18+ R-CH2-N-H H
Basicità delle ammine aromatiche
L'anilina e le ammine aromatiche in generale sono molto meno basiche delle ammine alifatiche perché il doppietto elettronico è meno disponibile essendo delocalizzato sull'anello aromatico. ŅH2 H N N Z H 工 H pKb: 4.7 3.3 3.0 3.3 9.4 13.0 Sostituenti elettronattrattori (p.e. nitro gruppo) diminuiscono ulteriormente la basicità riducendo la disponibilità elettronica, mentre sostituenti elettrondonatori hanno l' effetto opposto. 工 H +H H +H HOH 1 H-N-H N 0 4 0 NO2 N- NO2 NO2 NO2 ŅH2 CH3 O2N NH2 0 *
Spiegazione della basicità delle ammine
N CH3 più basica di più basica di N N H pKb = 3.3 pKb = 8.7 pKb = 13.6 Lone electron pair 1.01 Å 1.47 Å sp3 1. CH3 H 105.9º 112.9º Gli elettroni in un orbitale con maggiore carattere s sono trattenuti più vicino al nucleo e quindi sono meno disponibili these electrons are part of the Tr cloud these electrons are in an sp2 orbital perpendicular to the p orbitals H Gli elettroni spaiati dell'azoto del pirrolo fanno parte del sestetto aromatico quindi NON sono per niente disponibili!
Formazioni di sali
Le ammine sia solubili sia insolubili in acqua reagiscono quantitativamente con acidi forti formando sali sempre solubili in acqua NH2 ŅH3 CI + HCI Per la sua capacità di dare sali, una ammina insolubile in acqua può solubilizzarsi in presenza di acidi diluiti. Gli alcaloidi si estraggono dalle foglie o dalla corteccia con acido diluito
Farmaci e sali di ammine
Molti farmaci vengono spesso somministrati sotto forma di sali, per la loro maggiore solubilità in acqua HCI N NH2 N NH3 CI D novocaina insolubile in acqua novocaina cloridrato solubile in acqua
Reazioni di preparazione delle ammine
Reazioni di sostituzione nucleofila
- Alchilazione diretta.
- Apertura nucleofila dell'anello epossidico con ammoniaca o ammine.
Metodi Riduttivi
- Riduzione di immine.
1. Alchilazione diretta
Sono reazioni di sostituzione nucleofila. La nucleofilia dell'azoto consente la reazione con alogeno derivati alchilici. 8 H エ s+ Hun.C O HI.C. + + 1 H H + H H CH3 N H CH3 CH3 :N. H + CH3 HI Attenzione: l'ammina secondaria che si forma è un nucleofilo ancora migliore dell'ammina primaria di partenza! Si può quindi avere una seconda reazione di sostituzione nucleofila con formazione dell'ammina terziaria 18- 18+ H H - HunC I + HI NOCH3 H CH3 CH3 : N.CH3 CH3 NOCH3 H H
Alchilazione diretta: formazione del sale di ammonio quaternario
Attenzione: la ammina terziaria che si forma è un nucleofilo ancora migliore dell'ammina secondaria! Si può quindi avere una terza reazione di sostituzione nucleofila con formazione del sale di ammonio quaternario (CH3)3N + CH3l + (CH3)4N I - + - Processo totale: CH3NH2 + CH3l (in eccesso) (CH3)4N I A causa di tutto ciò l'interesse sintetico è limitato
2. Apertura degli epossidi con nucleofili azotati
H2C-CH2 + NH3 O > HOCH2CH 2NH2 2-amminoetanolo H2C-CH2 + NHMe2 O > HOCH2CH 2NMe 2 2-(dimetilammino)etanolo C O O OH + MYLAN 6180 MYLAN propranololo (beta-bloccante per cardiopatie) Nota la regiochimica e la stereochimica ZI NH2T
3. Riduzione di immine ed enammine (amminazione riduttiva)
da immine posso ottenere ammine 1° e 2° 0 CH3CO2H catalyst N-H NH2 -H2O H2 & Ni (catalyst) NH3 + NH 2 1º an imine CH3CO2H (catalyst) H2 & Ni (catalyst) H 2° =0 + -NH2 -N: -H2O imine da enammine posso ottenere ammine 3° 0 CH3CO2H (catalyst) H H H2 & Ni (catalyst) C2H5 + : N-H N= N N-C3H7 - H2O C2H5 NaBH3CN H iminium ion enamine H3C 3º N.B .: Il metodo riduttivo più utilizzato il lab per convertire immine ed enammine in ammine è il sodio cianoboroidruro (NaBH3CN); simile al sodio boroidruro ma più stabile in ambiente debolmente acido. Gli intermedi non vengono isolati prima della riduzione. L OH