Il Metabolismo del Glicogeno e la sua regolazione ormonale, Appunti UNIFE
Documento dall'Università degli Studi di Ferrara sul Metabolismo del Glicogeno. Il Pdf, utile per lo studio universitario di Biologia, esplora la sintesi e la degradazione del glicogeno, con schemi che illustrano i processi biochimici e le strutture molecolari.
Mostra di più12 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Il Metabolismo del Glicogeno
Il glicogeno fa parte di una serie di polisaccaridi che ha la funzione di riserva nell'organismo ed è una sorgente alimentare (insieme all'amido). L'amido è un polimero costituito da unità monomeriche di glucosio e ne rappresenta la maggiore sorgente di esso. La cellulosa invece, seppur simile, non verrà trattata in quanto non abbiamo gli enzimi per digerirla.
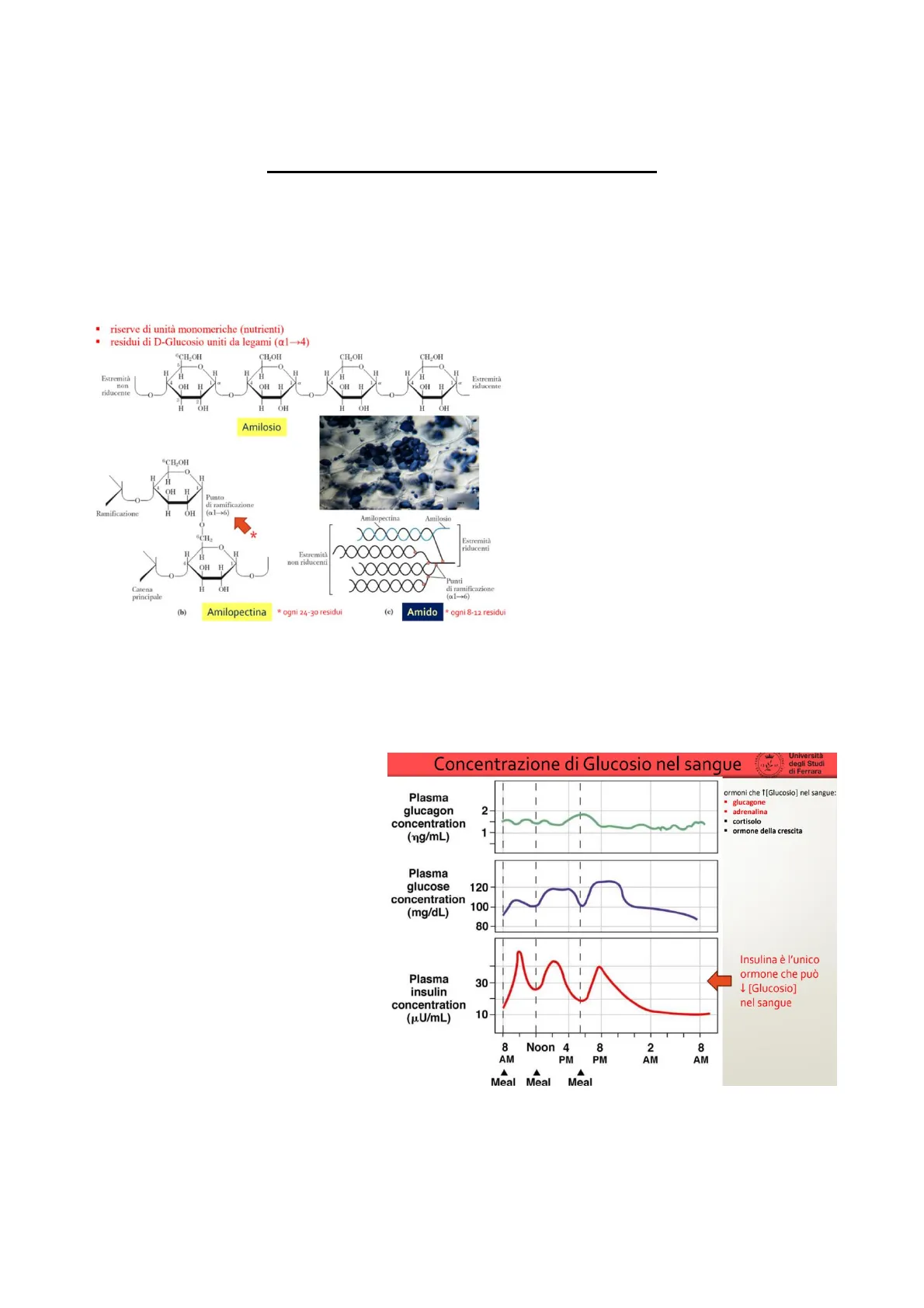
- riserve di unità monomeriche (nutrienti)
- residui di D-Glucosio uniti da legami (a1->4)
6CH_OH CH.OH CHỊOH CH_OH 5 O 0 O H H H H H H Estremità H H Estremità riducente nor riducente OH OH OH H OH H 3 2 H OH H OH H OH Amilosio 6CH.OH 0 H = H OH H Punto di ramificazione (a1-+6) Ramificazione ÓH Amilopectina Amilosio O * H H Estremità non riducenti 4 OH 0000000 H ÓH *Punti di ramificazione (x1-+6) (b) Amilopectina * ogni 24-30 residui (c) Amido * ogni 8-12 residui
L'amido è contenuto nelle piante ed è costituito da più catene di amilosio, nel quale sono presenti legami glucosidici a 1-4. Differentemente l'amilopectina si lega all'amilosio con legame a 1-6 per andare a costituire le ramificazioni nell'amido.
Degradazione dell'Amido
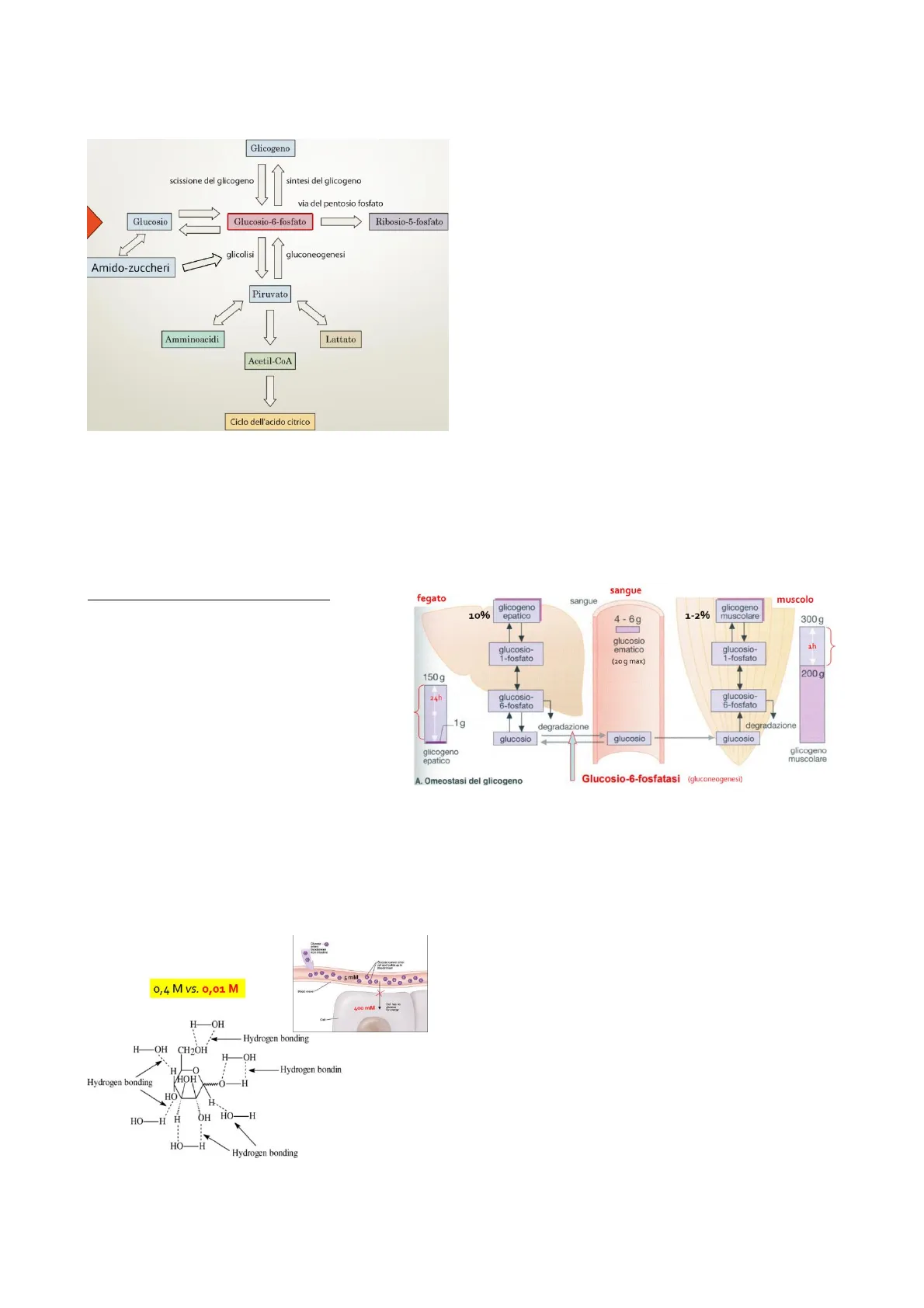
Come viene degradato l'amido? Viene secreta l'amilasi di tipo a che frantuma i polimeri in dimeri e trimeri (es maltotriosio, maltosio, isomaltosio e destrina). L'enzima amilasi funziona in un ambiente con ph vicino a 7. Infatti, già a livello della bocca, attraverso la saliva, avviene una prima digestione, la quale è interrotta a livello dello stomaco. Si continua il processo nel duodeno quando è secreta l'amilasi pancreatica. Dunque, il glucosio attraversa la barriera intestinale ed arriva a livello del circolo sanguineo, dove è regolato principalmente da due ormoni: l'insulina e il glucagone. La prima è secreta subito dopo i pasti, e in particolare si ha il picco di questo ormone dopo un Concentrazione di Glucosio nel sangue Università degli Studi di Ferrara F-F paio di ore dall'ingestione del cibo. La Plasma ormoni che 1[Glucosio] nel sangue: glucagon 2 · adrenalina · glucagone concentration · cortisolo (mg/mL) sua azione è quella di far calare la 1 · ormone della crescita concentrazione di glucosio nel sangue, - Plasma - glucose 120 concentration (mg/dL) stimolandone l'internalizzazione a livello 100 dei tessuti. Il glucagone, invece, è indotto 80 soprattutto la notte, in corrispondenza - Insulina è l'unico Plasma 30 insulin concentration (pU/mL) ormone che può I [Glucosio] nel sangue della massima diminuzione di glucosio e ne stimola la gluconeogenesi e la 10- scissione di glicogeno. Oltre al glucagone, 8 Noon 4 8 2 8 la medesima azione è svolta Meal Meal AM PM PM AM AM Meal dall'adrenalina, dal cortisolo e dall'ormone della crescita, i quali demoliscono le riserve di glicogeno liberando il glucosio nel sangue. Al contrario, l'azione dell'insulina non è sostituibile da altri ormoni. Non esistendo altri sistemi alternativi spesso si incorre nella patologia del diabete mellito. La concentrazione di glucosio è di 90 mg/dl e di 5 mM e si hanno delle fluttuazioni che seguono il ritmo circadiano.
Vie Metaboliche del Glucosio
1 EL H H @ a H H H Catena principale Estremità riducenti 2000000Glicogeno scissione del glicogeno sintesi del glicogeno via del pentosio fosfato Glucosio Glucosio-6-fosfato Ribosio-5-fosfato glicolisi gluconeogenesi Amido-zuccheri Piruvato Amminoacidi Lattato Acetil-CoA Ciclo dell'acido citrico Il metabolismo del glucosio verte su delle vie principali: la fosforilazione del glucosio come 6 fosfato e l'internalizzazione come zuccheri. La molecola di 6 fosfato può seguire o la via dell'ossidazione, oppure negli epatociti e nelle cellule muscolari può essere internalizzato sotto forma di glicogeno (per essere in seguito demolito in molecole di glucosio in caso di necessità). Si è anche precedentemente analizzata la via del pentoso fosfato che in caso di necessità produce NADPH o ribosio e può generare i nucleotidi. Ora si analizzerà il meccanismo che regola la sintesi di glicogeno e la gluconeogenesi. Tutto ciò è necessario per mantenere a un livello costante il glucosio 6 fosfato, per fare in modo che questo segua la via della glicogenesi oppure sia rimosso il fosfato e il glucosio sia rilasciato a livello del circolo.
L'Omeostasi del Glucosio
Il glucosio nel sangue mantiene una certa concentrazione ed è regolato per la maggior parte dalle riserve epatiche. Il fegato può incamerare glicogeno fino a 1,5 1g degradazione litri, il quale in caso di digiuno prolungato può glucosio glucosio glucosio degradazione glicogeno epatico glicogeno muscolare esaurirsi completamente. Nel muscolo, A. Omeostasi del glicogeno Glucosio-6-fosfatasi (gluconeogenesi) invece, si hanno maggiori quantità di glicogeno, ma queste riserve non possono essere completamente depauperate. Infatti, solo 1/3 delle riserve è spendibile energeticamente. La parte restante è necessaria per la produzione di ATP per la contrazione muscolare in caso di una fuga immediata o di una scarica di adrenalina. Il fegato è l'organo che più velocemente rende disponibile il glucosio in caso di necessità.
Molecola di Glucosio e Polimeri
0,4 M vs. 0,01 M Brat vorsel 400 mM Cal H -OH - Hydrogen bonding H-OH CH2OH H -O Hydrogen bondin WHOH\ Hydrogen bonding HO H HO-H H OH HO-H HO-H Hydrogen bonding sangue fegato sangue glicogeno epatico 4 - 6g 1-2% glicogeno muscolare 300 g 1h glucosio- 1-fosfato glucosio ematico (20 g max) glucosio- 1-fosfato 150g 1 200 g 24h glucosio- 6-fosfato glucosio- 6-fosfato muscolo 10% @ 5 mM Si analizza la molecola di glucosio: questa può essere idratata, aumentando il suo ingombro. Per cui se la molecola di glucosio idratata fosse incamerata singolarmente nel fegato, si avrebbe un peso maggiore con un corrispettivo aumento della molarità. Ciò causerebbe l'impossibilità per il glucosio di entrare negli epatociti, poiché i GLUT non sarebbero in grado di internalizzarli. Grazie alla creazione dei polimeri si è in grado di 2abbassare la concentrazione a 0,01M ed è possibile incamerare un numero molto maggiore di molecole di glucosio con l'utilizzo di un minore spazio.
Il Glicogeno
Le molecole di glicogeno si strutturano in granuli malin molto grandi e si organizzano dall'unità monomerica PP16 LF PTG ฿ che può formare circa 30 "rosette" a, visibili al Stbd1 AMPK Glycogen GS microscopio elettronico. A queste strutture sono GN PH DBE a PH Kinase ancorati tutti gli enzimi responsabili del 3 G PP1c metabolismo del glicogeno, come le fosforilasi, le . Fosforilasi (PH) . Enzima deramificante (DBE) sintasi e molti altri enzimi regolativi. In tal modo essi · Fosforilasi chinasi (PH Kinase) sono già posizionati e pronti ad essere attivati o · Glicogeno sintasi (GS) inibiti. Infatti, quando l'organismo richiede glucosio, ad esempio nel cervello, lo richiede immediatamente. I polimeri di glucosio si organizzano attorno a un dimero proteico, formato da due estremità legate a una catena in crescita, dalla quale nascono le ramificazioni. L'estremità legata alla glicogenina è un'estremità riducente, più reattiva, mentre l'estremità non riducente è rappresentata dall'estremità libera esposta. Esistono due differenti tipi di legame tra le molecole di glucosio: a 1-4 e a 1-6. Ogni 8/10 unità di glucosio nasce una ramificazione. Ogni estremità può essere attaccata da un enzima, quindi molto glucosio può essere liberato rapidamente.
Scissione del Legame Glicosidico
Come è staccato il legame glicosidico? O Esistono due modi: attraverso O HO- Glicogeno -OH fosforilasi idrolisi di una molecola d'acqua a livello del legame glicosidico, oppure per aggiunta di un gruppo Idrolisi ~H-O-H fosforico, ovvero fosforolisi. Infatti, Glicogeno O Enzima O deramificante fosforilasi Enzima deramificante l'enzima fosforilasi porta alla lisi legame glicosidico del glicogeno attraverso la O fosforilazione. La glicogeno Fosforolisi -HO-P-OH OF Insulina Glicogeno Digiuno O O esaurito fosforilasi, similmente ad un Glucagone gluconeogenesi (giorni) O-P-OH "pacman", stacca un glucosio per OH O 6-12 hrs 1-2 hrs Glicemia volta a partire dall'estremità non HO Un pasto alicogemolisi riducente, fino a quando non restano 4 residui di glucosio alla successiva ramificazione, poi interviene un altro enzima, detto deramificante. Esso rimuove tre monomeri e li sposta nella ramificazione accanto e scinde l'ultimo glucosio legato con a 1-6 attraverso idrolisi, liberando del glucosio puro e non fosforilato come la glicogeno fosforilasi. Quindi, la glicogeno fosforilasi rappresenta l'enzima principale, tuttavia a causa di un ingombro sterico, necessita dell'azione dell'enzima deramificante per rompere i punti di giunzione.
Digiuno Prolungato e Gluconeogenesi
Digiuno prolungato 3Quando il glucagone stimola la liberazione di glucosio, è stimolata la gluconeogenesi ma anche la glicogenolisi. La gluconeogenesi è il Fosfoglucomutasi vs. Fosfoglicerato mutasi processo che si mantiene quando il Ser vs. His Glucosio 1-fosfato 1 -2-02PO digiuno è prolungato, la quale attinge a Glucosio Ser Glucosio - Ser 2-O,PO H 6-fosfato 1,6-bisfosfato Ser H COPO H COH H COPO O O Ħ tutto ciò che ha a disposizione, soprattutto H H HO 2 H H H H 0 HO OPO OH H HO OPO H HO HO OH H OH H amminoacidi. Una volta consumate le H HO H HO OH riserve sia del fegato che muscolari, si ha Fosfoglucomutasi Glicolisi (muscolo) uscita dalle cellule nel sangue (fegato) la possibilità di attingere al glucosio Figura 15.29 La reazione catalizzata dalla fosfoglucomutasi. 1,6-bisfosfato. Nella tappa @, il gruppo fosforico sull'atomo C-1 del glucosio 1,6-bisfosfato (in rosso) viene riportato sull'enzima, riformando il fosfoenzima e producendo glucosio 6-fosfato. La reazione ha inizio con la fosforilazione dell'enzima su un residuo di Ser. Nella tappa 0, l'enzima cede il suo gruppo fosforico (in blu) al glucosio 1-fosfato, producendo glucosio attraverso gli amminoacidi, facendo calare la massa muscolare. Ricapitolando, è l'enzima deramificante a staccare il glucosio 1 fosfato. Questo è convertito da una fosfoglucomutasi in glucosio 6 fosfato, per cui il gruppo fosforico è spostato da C1 a C6. Ciò avviene soprattutto negli epatociti per fare in modo che in seguito sia rimosso il gruppo fosforico attraverso l'azione della glucosio 6 fosfatasi. Questo enzima permettere al glucosio di uscire dalla cellula ed immettersi nel circolo sanguineo. La fosfoglucomutasi è simile all'enzima fosfoglicero mutasi usata durante la glicolisi. La loro differenza consiste nell'amminoacido fosforilato: mentre l'istidina si trova nella fosfogliceromutasi, permettendo la creazione di glucosio bifosfato 1-6, la serina è oggetto della fosfoglucomutasi. Entrambe lavorano attraverso lo scambio di un gruppo fosforico.
Sintesi di Glicogeno
Zuccheri-nucleotidi
O O CHỊOH Zucchero o-P-O- + 0-P-O-P-O- 0 Ribosio Base Come avviene la sintesi di glicogeno? OH 0- 0- Per sintetizzare il glicogeno occorre attaccare H O HO Zucchero fosforilato NTP OH condensazione di un esosio 1-fosfato con un NDP-zucchero pirofosforilasi -Base -0-P- 2. Possono formare molti legami non covalenti con gli enzimi e P. -O-P- O favorire i processi catalitici. nucleotide trifosfato Uridine diphosphate glucose (UDPG) glucosio, tuttavia queste reazioni non sono favorite. -0 -0-P -0- Zucchero legato 0 0 Pirofosfato (PP;) AGF0 = - 19,2 KJ/mole al nucleotide (NDP-zucchero) Zucchero Ribosio 1. Formazione metabolicamente irreversibile O AG10 = - 31,9 KJ/mole Serve, dunque, "attivare" le molecole di glucosio tramite l'attacco di uridinadifosfato (un pezzo di 3. i gruppi nucleotidilici UMP (o AMP) sono ottimi gruppi uscenti perché attivano il carbonio anomerico del Glucosio al quale sono legati e si prestato ad attacchi nucleofili. pirofosfatasi inorganica nucleotide bifosfato legato allo zucchero, il quale è un composto molto energetico). Per cui, quando lo 4. i gruppi nucleotidilici sono un 2 -O-P-OH 0- modo per marcarli e per stoccarli in modo diverso, separandoli Fosfato (P;) Luis Leloir (1953) dagli zuccheri aventi altri destini. zucchero è attaccato dal nucleotide energetico si Reazione complessiva: Zucchero fosforilato + NTP - NDP-zucchero + 2P; lega a un altro zucchero, si rompe il legame con UDP e si libera energia. Legare l'UDP al glucosio significa "ipotecare" gli zuccheri: quando il glucosio entra nella cellula, questo può essere fosforilato, può seguire le vie del pentoso fosfato e della glicolisi, ma una volta che esso è legato all'UDP, investiamo lo zucchero nei processi di sintesi del glicogeno, lo direzioniamo e lo conserviamo. Liberato dal legame con l'UDP, il carbonio a anomerico in questione è reattivo e favorisce un successivo attacco nucleofilo alla catena crescente. 4