Relazione tra struttura e funzione nelle proteine: mioglobina ed emoglobina
Documento sulla relazione tra struttura e funzione nelle proteine. Il Pdf esplora il ruolo di mioglobina ed emoglobina, il gruppo Eme e gli effettori allosterici come BPG, pH e CO2, per studenti universitari di Biologia.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Mioglobina ed Emoglobina: Panoramica
RELAZIONE TRA STRUTTURA E FUNZIONE NELLE PROTEINE
Mioglobina ed emoglobina
- Globine: famiglia di proteine; struttura 1. e 3. simile
- In umani e altri mammiferi alemno 4 tipi: Mioglobina, emoglobina, neuroglobina
(in neuroni), citoglobina (partei di vasi sanguigni)
Proteine globulari (superfamiglia delle globine) capaci di legare l'ossigeno
Mioglobina: Caratteristiche e Funzione
- Mioglobina
- magazzino di ossigeno; (favorisce difusione O2 enl tessuto muscolare)
- Proteina monomerica di 153 aa (capodoglio)
- È stata la prima proteina di cui si è scoperta la struttura terziaria (tramite tecnica
·difrazione raggi X) - Localizzazione intracellulare (muscoli dei. vertebrati)
Emoglobina: Struttura e Localizzazione
- Emoglobina: proteina di trasporto dell'ossigeno (nel torrente circolatorio)
- Proteina tetramerica (2 catene - a - 141aa+2 catene -3 - 146 aa)
(catene non sono però catene alfa, ma semplicemente chiamate cosi subunità nel
tetramero) - Localizzazione intracellulare (eritrociti => cellule del sangue, trasporto ossigeno)
Ruolo dell'Emoglobina nel Trasporto di Ossigeno
Ruolo di emoglobina nel trasporto di ossigeno
- Il metabolismo aerobico richiede l'apporto di ossigeno ai tessuti
- Ossigneo necessario come accettore finale dei elettroni in sintesi di ATP
- In organismi piccoli (fino ad alcuni millimetri), la diffusione dall'esterno attraverso i
. tessuti è sufficiente - Organismi più grandi richiedono invece un sistema circolatorio
- L'ossigeno ha una bassa solubilità in acqua
-> servono proteine che trasportano O2, ma nessuna catena R dei aa idonea a legare
reversibilmente O2; svolto da ferro e rame che hanno forte tendenza a legare O2
-> apposite proteine trasportatrici di ossigeno ne aumentano la solubilità nei fluidi
circolanti
Proteine Coniugate: Mioglobina ed Emoglobina
Mioglobina ed emoglobina sono proteine coniugate
- Contengono porzione proteica e non proteica
- Proteine che contengono una porzione non peptidica .
- Quando la porzione non peptidica è una sostanza organica stabilmente legata alla
. componente proteica viene detta gruppo prostetico (permanentemente legato). - Nella mioglobina ed emoglobina, l'ossigeno non si lega alla parte proteina ma al
gruppo prostetico che contiene legato al centro un atomo di ferro (gruppo eme)
Il Gruppo Eme: Struttura e Funzione
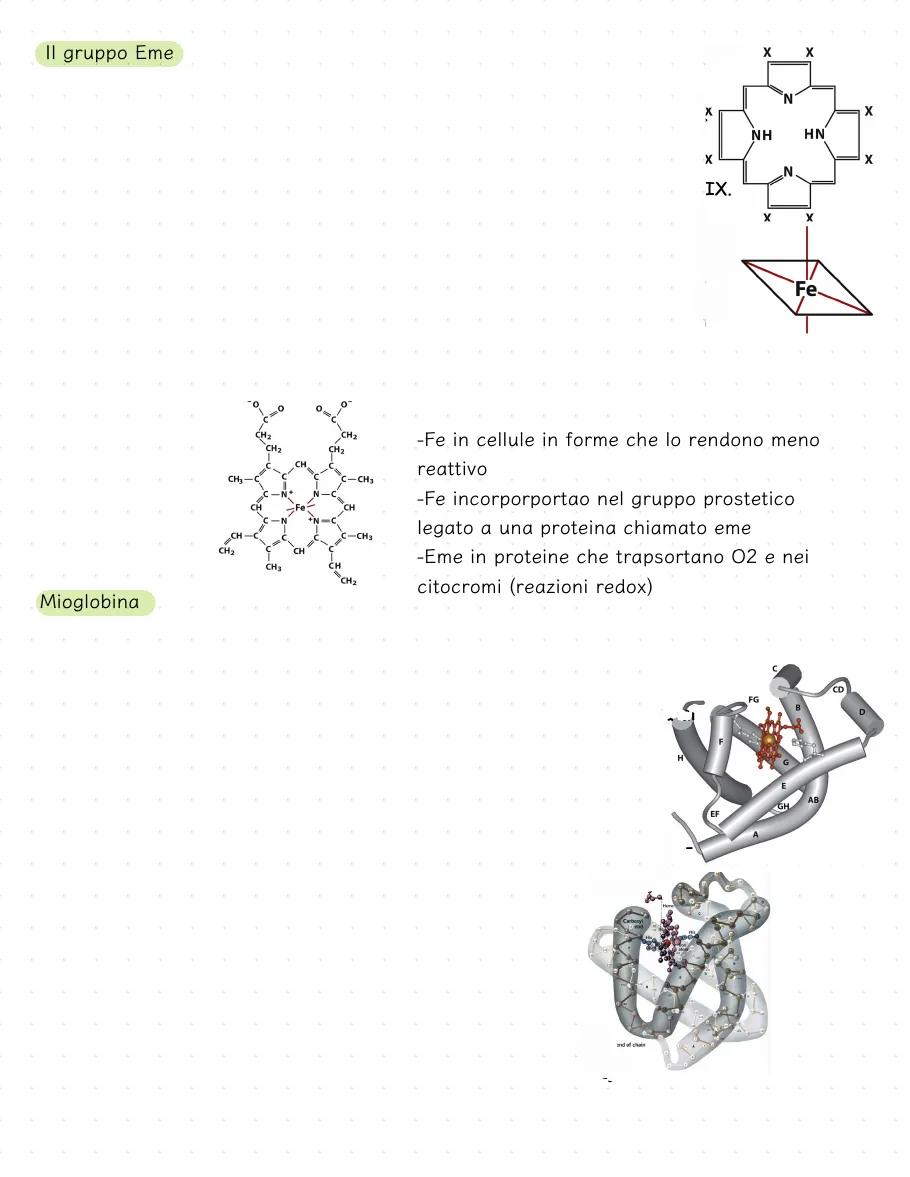
Il gruppo Eme
- Il gruppo eme è presente nella mioglobina, emoglobina e in altre
proteine chiamate proteine Eme - Il gruppo eme consiste di un complesso organico a forma di
anello, chiamato protoporfirina IX - Ad anello è legato singolo atomo di ferro in forma Fe2+
- L'atomo di ferro del gruppo eme contiene 6 legami di
coordinazione - 4 sono su stesso piano rispetto all'anello porfirinico sono legati
. ad esso (legati con 4 N dell'anello) - due sono perpendicolari all'anello, secondo i vertici di un
ottaedro
O
O
CH2
CH2
CH2
CH2
C
CH
C
/
C
C
C-CH3
.
1
N-
-C.
CH
„Fe
CH
C-N
+N =C
1
CH -
C
C
/
CH2
C
CH
CH 3
CH
`CH2
-Fe in cellule in forme che lo rendono meno
reattivo
-Fe incorporportao nel gruppo prostetico
legato a una proteina chiamato eme
-Eme in proteine che trapsortano O2 e nei
citocromi (reazioni redox)
Mioglobina: Dettagli Strutturali
Mioglobina
- Costituita da 153 aa (Kendrew, 1959 Mb di capodoglio,
determinata ai raggi X) - Funzione: lega ed immagazzina l'ossigeno
- 8 a-eliche (A-H), organizzate a sandwich 3-su-3 (BEF-AGH)
- interrotti da ripiegamenti (a vole btea ripiegamenti)
- Lega da loop, per formare struttura globulare
- Gruppo eme legato in tasca idrofobica fra elica E ed F
- Gruppo eme in rosso; ferro in oro (al centro del gruppo
prostetico) - Presente nei muscoli di tutti i mammiferi
- struttura compatta: 80% a elica, 20% random coil
- 4 eliche terminano con Pro (favorisce ripiegamento)
- assenza di Cys (pottrebbero formare ponti S)
- gli a.a. esterni e nelle anse sono polari (Glu, Asp, Asn,
(interagiscono con solvente) - gli aa. interni sono prevalentemente apolari, con due His (F8/E7)
cruciali per legare l'O2 (F/E: alfa elica su cui si trova His)
C
CD
FG
B
D
F
H
G
E
AB
GH
EF
A
Heme
Carboxyl
19 end
His
from
atom
104
e
end of chain
X
X
N
X
X
X.
NH
HN
X
X
N
IX.
X
X
Fe
CH3-C
C-N+
-C
C-CH 3
SU-
•Il gruppo Eme
Edge view
_CH
HN
N-Fe-O2
/
CH
CH2
Histidine
residue
Plane of
porphyrin
ring system
anello porfinirico (di lato)
Legame del Ferro e Ossigeno
- atomo di ferro in centro
- Fe lega da una parte ossigeno (o libero)
- Altra parte legame di coordinazione con residuo di istidina (F8)
- 'Quando si lega 02 proprietà di ferro si modificano, es. diverso
colore del sangue venoso povero di O2 (rosso scuro), sangue
arterioso ricco di O2 (rosso brillante)
Legami di Coordinazione del Ferro
Il Fe ha sei legami di coordinazione:
- 4 con gli N degli anelli pirrolici
- 2 perpendicolari all'eme, di cui uno lega l'His prossimale
F8 l'altro è libero oppure lega l'O2 (in globine) - uno legato a N della catena R di His; altro a O2
- Per funzionare correttamente, il Fe deve sempre stare nello,
stato ridotto 2+ (II)
0
1
1
HỌC=CH
CH
CH2
A
B
CH
N
N
Fe(II)
N
N
H3C-
D
C
CH3
"00C-CH2-CH2
CH2-CH2-COO
Z
HN
CH2
0
H
H
Ambiente Idrofobico e Residui Cruciali
- L'ambiente idrofobico proteico impedisce che avvenga l'ossidazione irreversibile del
· Fe quando lega l'O2 (in proteina cconversione irreversibile di Fe2+ a Fe3+ non
. avveine perchè gruppo eme immerso in profondità nella struttura) - Val e Phe (aa con catena laterale idrofobica) Mantengono in posizione l'eme
- contribusicono a ambiente idrofobico e mantenere gruppo eme in posizione
- His E7= istidina distale (forma un legame H con l'O2); non direttamente legata a
ferro o ossigeno; importante per coordinare ossigeno - His F8= istidina prossimale (5a posizione di coordinazione del Fe)
Residui che Circondano l'Eme nella Mioglobina
His E7
Val E11
Phe CD 1
O2
0,
His F8
I residui che circondando l'eme nella mioglobina
- Rosso: ferro
- Legame sopra es sotto anello
- His distale su alfa elica e
Marrone: Val e Phe
Blu: His
Rosso: ossigeno
His E7 € His distale
Phe CD1
H
Val E11
Fe
His F8
€ His prossimale
Modificazione Conformazionale dell'Eme
- C =
H3CIl legame con l'ossigeno induce una modificazione conformazionale dell'eme - Deossimioglobina: Il Ferro è fuori dal piano dell'eme di 0.055 nm (struttura a cupola)
- Ossimioglobina: il Ferro è fuori dal piano dell'eme di 0.026 nm
Val FG5
Heme
Leu
FG3
O
--- His
distale
His F8
Helix F
Leu F4
deossimioglobina
ossimioglobina:
T state
R state
Movimento Conformazionale e Regolazione Allosterica
- Movimento conformazionale indotto si trasmette all'elica F (si tira dietro istidina
prossimale) - Si trasmette a tutto il resto della proteina, influenza le altre tre subunità, impatto su
cinetica ossigeno - Questo cambiamento conformazionale non è rilevante
per la funzione della mioglobina ma è fondamentale
nella la regolazione allosterica dell'emoglobina
0,4 Å
Porfirina
O2
Ferro
His
Leganti del Gruppo Eme nell'Ossiemoglobina
Nell'ossiemoglobina
- CO, NO, H2S possono legarsi al gruppo eme delle proteine (con afinita maggiori.
. rispetto all'O2) ed "avvelenare" il gruppo eme - Da Eme all'intero, legame con ossigeno favorito; con eme dentro proteine che
legano O2 regolano accesso al ferro del CO e altre piccole molecole)
Effetti Sterici sul Legame dei Ligandi
Effetti sterici dei residui distali sul legame del leganti dell'eme
- Eme isolato ha un'affinità per CO 25000 volte maggiore rispetto all'O2
- Ciononostante, nella mioglobina, l'affinità del gruppo eme per CO è molto minore
rispetto all'eme isolato per effetto dei gruppi proteici che circondano il gruppo eme
(in particolare l'His distale) che favoriscono un legame inclinato
O
=
O
C
-Fe
Fe
X
€ His distale
X
His E
Phe CDI
H
His F8
His prossimale
£
distale
Conformazione del Legame Ossigeno e CO
- legame doppio inclinato favorito per istidina
£ - ossigeno si lega al eme formando angolo con
ferro
=> conformazione che si adatta facilmente a
spazi interni della mioglobina - CO forma piccolo angolo perchè struttura
perpendicolare impedita da His distale,
indebolisce legame del CO alla mioglobina
Cinetica di Legame dell'O2 per la Mioglobina
Cinetica di legame di O2 per la mioglobina
- Premessa: In un processo chimico reversibile e transiente: AB= > A+B all'equilibrio,
esiste una costante di dissociazione definita come:
Kd=
[AB - La molecola che si lega, tipicamente una molecola piccola, è chiamata Ligando (es.
ossigeno). - Regione dove il ligando si lega è chiamata sito di legame
- Ligando si lega tramite interazioni transienti tali per cui il legame è reversibile (deve
essere in grado di rilasciarlo quando necessario) - Nel legame reversibile di 02 a Mb, all'equilibrio: MbO2 < > Mb+O2
K=
Mb][O2]
MbO2
cioè
MbO2 =
K
Mb] [O2]
(*) - [MbO2] = concentrazione ossiMb
.- [Mb] = concentrazione deossiMb
.- [02] = concentrazione 02 non legato. - "Saturazione Y"(frazione di siti di legame di 02 occupati)
y=
[MbO2]
Mb+MbO2
K+[02]
[o2]
(concentrazione di mioglobina che lega ossigeno sulla
concetrazione totale di mioglobina) - Se sostituiamo MbO2 con quello indicato sopra (*), otteniamo:
y=
K+[02]
2
(equazione che descrive un'iperbole)
Essendo 02 un fas:
[o2]=pO2
y=
K+ pO2
pO2
(pO2 = pressione parziale)
Curva di Legame dell'Ossigeno alla Mioglobina
- Curva che descrive il legame dell'ossigeno alla mioglobina:
- nel grafico, la frazione dei siti di legame del ligando (0, theta), che corrisponde alla
saturazione Y, è tracciata contro la concentrazione del ligando (pressione parziale di
ossigeno, kilopascal, kPa)
1.U
pO2
MbO2
<>Mb+O2
y=
K+ pO2
0.5
K=
Mb][2]
[MbO]
Quando y=0.5
K=pO2
K=P50
0
P50
5
10
pO2 (kPa)
Saturazione e Affinità della Mioglobina
- grafico che va alla saturazione, tutti i legami vanno verso saturazione
1.0
0 (Theta)=
pO2
K+ pO2
pO2=Pressione
parziale
0 0.5
P50
5 - All'aumentare di pO2, aumentano i siti occupati da 02
- A pO2 elevate, si ha saturazione cioè tutti i siti di legame sono occupati
- La pendenza della curva diminuisce all' aumentare di K
- La pendenza della curva aumenta al diminuire di K
- Quando 0=0.5 -> K=pO2 (P50)
La mIoglobina è saturato al 50% dall'O2 - Quando 0= 0.5 operativamente K può essere definita come K=P50
- La mioglobina ha una p50 molto bassa e quindi un'alta affinità
per l'O2 (circa 0.4KPa) - Alle pO2 fisiologiche nel sangue (13KPa/100Torr arterie,
4KPa/30Torr vene), la mioglobina sempre saturata . - Mioglobina deve essere in grado di catturare nel citoplasma di
kPa
cellule metabolicamente attive l'O2 proveniente dal torrente circolatorio (pO2 circa
4KPa) ed essere in grado di rilasciarlo ai mitocondri (p.O2<0.5KPa) - La mioglobina non efficace per favorire passaggio di 02 dagli alveoli polmonari ai
capillari (ma per imagazzinare ossigeno a livello muscolare)
Curva di Saturazione della Mioglobina
Curva di saturazione della mioglobina
1
T
P
0,7
E
0
0,6
S
T.
0,5
S
0,4
TJ
C
0,2
T
0,1
I
0
OkPa 1 kPa 2kPa 4kPa 6 KPa 8 kPa
10
12
14
<Pa
kPa
0,8
e theta
M
0,3