Citomegalovirus e Herpesvirus: struttura, ciclo replicativo e patogenesi
Documento di Università su Citomegalovirus. Il Pdf esplora la biologia del Citomegalovirus e dell'Herpesvirus, descrivendo struttura, ciclo replicativo e meccanismi patogenici. Questo documento di Biologia analizza anche le differenze nel ciclo replicativo rispetto all'herpes simplex virus e i meccanismi patogenici dell'Epstein-Barr virus, inclusa la mononucleosi infettiva.
Mostra di più14 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Citomegalovirus: Introduzione e Caratteristiche
Il professore aveva già introdotto la parte biologica del citomegalovirus e la rivede in maniera veloce ... È un virus che ha uno spettro cellulare ampio e sono caratterizzati da un ciclo di replicazione lento e citomegalia cioè l'aumento di dimensioni delle cellule infettate. Non ce tropismo per il sistema nervoso centrale. Abbiamo uno spettro gospite ampio, intermedio.
Domanda studente: da questo momento in poi non sono più afferenti nel sistema nervoso? Risposta professore: Esatto.
Struttura del Citomegalovirus
Componenti del Virione
Virione: sferoidale, d: 250 nm (il più grande tra herpesvirus) Peplos di origine cellulare, contiene glicoproteine (g):
- gB: adsorbimento alla superficie cellulare a seguito di legame con eparan solfati
- gH: lega i recettori cellulari: EGFR (epidermal growth factor receptor), integrine, PDGFRa (platelet-derived growth factor receptor A), BST/tetherina
Tegumento (matrice): proteine virus-specifiche regolatrici la espressione a cascata dei geni a, B, Y Capsìde: icosaedrico, 100 nm, 162 capsomeri Genoma: DNA ds (240 kbp), lineare
+ Membrane + gB Nucleocapsid Tegument gH 16 Cytomegalovirus progeny into an infected cell, TEM
Virione ha una forma sferica con diametro di 250 nm, il più grande fra virus herpetici e presenta un genoma rilevante come numero di forme isomeriche più elevate (4). Il peplos è di origine cellulare formato da glicoproteine che rendono conto del tropismo ampio a livello cellulare. Per esempio la gB concentra i virus sulla superficie delle cellule sensibili, traget, a seguito del legame con gli eparan solfati che sono glicoproteine che si trovano negli spazi intercellulari e quindi coinvolti nell'interazione intercellulare. Vari sono i siti riconosciti dall'anti-recettore del virus stesso. Tra questi c'è la teterina è riconosciuto come antigene stromale di tipo midollare di classe II che forma una zattera lipidica nelle membrane cellulari. Abbiamo anche quelle molecole che si trovano sulla superficie e servono per legare fattori di crescita a dimostrazione che il virus nel corso dell'evoluzione ha cambiato una parte della sua struttura di superfice per poter essere riconosciato da questi siti. C'è un peplos e quindi anche una matrice che prevede all'intero proteine VP16 E VPS e capside icosaedrico con diametro di circa 162 subunità. Il genoma è il più grande, nell'ordine delle 240 paia di basi. Abbiamo una unit large e unit short che sono le sequenze che si ripetono (in verde) e si invertono formando siti di ricombinazione nel genoma, con un'inversione di 180 gradi creando forme isomeriche. Si ha un totale di 4 asset genomici.
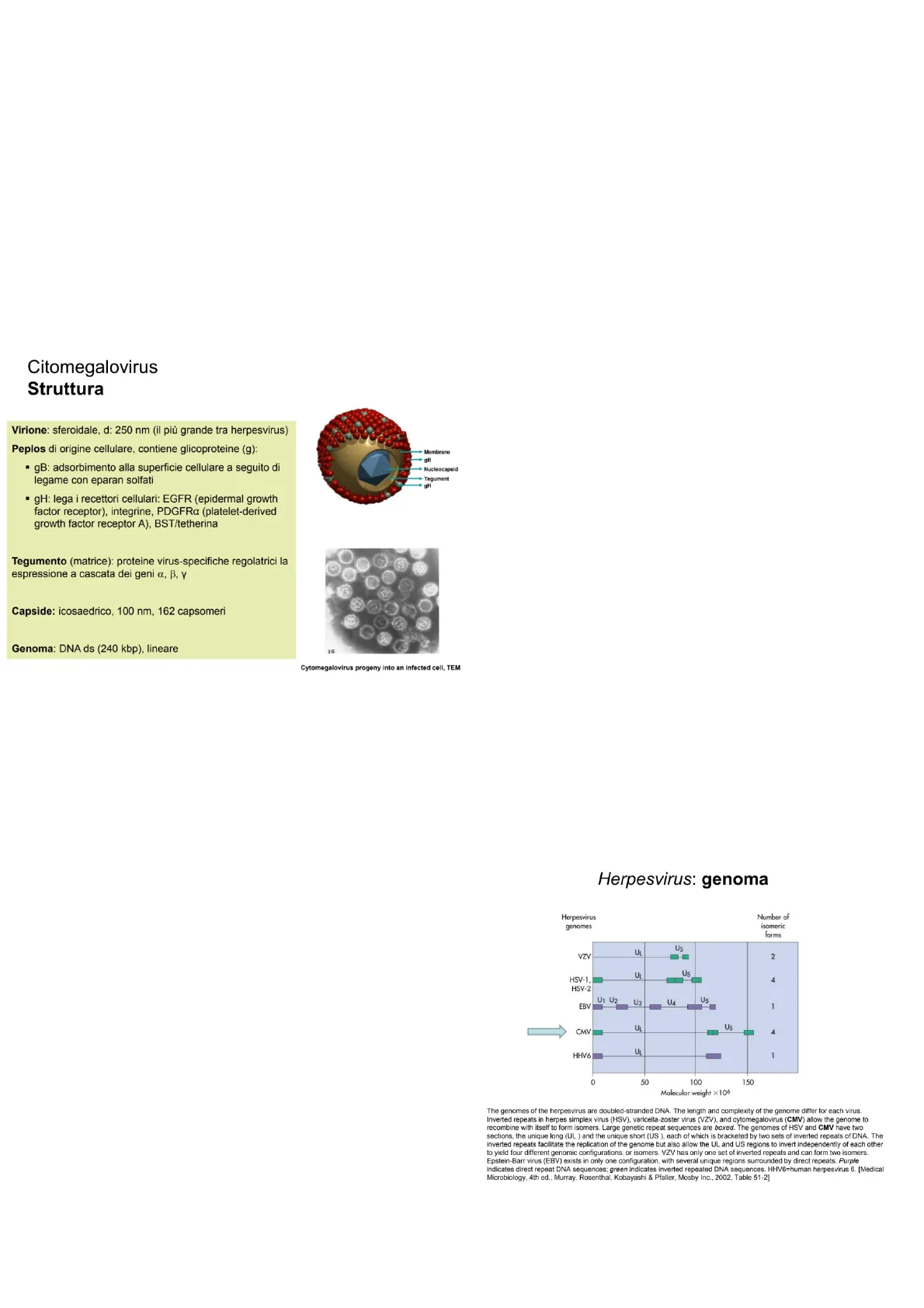
Genoma degli Herpesvirus
Herpesvirus: genoma Herpesvirus genomes Number of isomeric forms Us UL VZV 2 UL Us HSV-1 4 HSV-2 U1 U2 U3 U4 Us EBV 1 Us CMV 4 HHV6 1 0 50 100 150 Molecular weight x106 The genomes of the herpesvirus are doubled-stranded DNA. The length and complexity of the genome differ for each virus. Inverted repeats in herpes simplex virus (HSV), varicella-zoster virus (VZV), and cytomegalovirus (CMV) allow the genome to recombine with itself to form isomers. Large genetic repeat sequences are boxed. The genomes of HSV and CMV have two sections, the unique long (UL ) and the unique short (US ), each of which is bracketed by two sets of inverted repeats of DNA. The inverted repeats facilitate the replication of the genome but also allow the UL and US regions to invert independently of each other to yield four different genomic configurations, or isomers. VZV has only one set of inverted repeats and can form two isomers. Epstein-Barr virus (EBV) exists in only one configuration, with several unique regions surrounded by direct repeats. Purple indicates direct repeat DNA sequences; green indicates inverted repeated DNA sequences. HHV6=human herpesvirus 6. [Medical Microbiology, 4th ed., Murray, Rosenthal, Kobayashi & Pfaller, Mosby Inc., 2002, Table 51-2] 1 UL
Ciclo Replicativo del Citomegalovirus
Fasi del Ciclo Replicativo
Infectious particle Early Late Regulation of A epiBADrUL131 d e DE Microtubules C fibroBAD/UL 131 fibroBFXwt penome Viral gene regulation a Viral genome O replication O Nucleus - Infectious particle = Empty capsid 1 ?? . Tegument proteins . Derse bodies DE = Delayed early proteins = Genome-loaded capsid O = doONA viral genome f = Viral glycoproteins IE = Immediate early proteins L = Late proteins (A) Virions enter the cell: gB recognizes cell proteoglicans for the viral concentration at the cell surface, and then gH mediates cell penetration linking to the EGF-receptor. Two ways of entry. Tegument and capsid proteins are delivered to the cytoplasm. (B) The capsid travels to the nucleus, then the genome is delivered and circularized. Tegument proteins regulate host cell responses and initiate the temporal cascade of the expression of viral immediate early (IE) genes, followed by delayed early (DE) genes, which initiate viral genome replication, and late (L) genes. (C) Late gene expression initiates capsid assembly in the nucleus, followed by nuclear egress to the cytosol. Capsids associate with tegument proteins in the cytoplasm and are trafficked to the viral assembly complex (AC) containing components of the endoplasmic reticulum (ER), Golgi apparatus, and endosomal machinery. The capsids further acquire tegument and viral envelope by budding into intracellular vesicles at the AC. (D) Enveloped infectious particles are released along with non-infectious dense bodies. (adapted from: Jean Beltran & Cristea, 2014) Il ciclo è simile a quello dell'herpes simplex virus. Tra le differenze principali ... Il complesso che si forma nella zona al di sotto della membrana cellulare dove ci sono scambi del nucleocapside che attraversa la doppia membrana del nucleo attraverso uno dei 2 patway. Qui è riportato solo il patway in cui il nucleocapside viene avvolto da una membrana interna del nucleo che successivamente si fonde con quella esterna del nucleo per stabilire un nucleocapside classico che poi si deve dotare di peplos, nel complesso con l'apparato del Golgi che prevede poi la sintesi all'interno della membrana dell'unità con struttura classica, quindi con un nucleocapside e un peplos. L'ultima fase è quella dell'egressione, non si parla tanto di gemmazione perché la membrana che accoglie l'unità del virus va a fondersi in siti di membrana dove ci sono glicoproteine come gB, e c'è un'eliminazione dei virus sull'esterno della cellula. Ci sono anche unità virali indicate in nero perché sono unità che mancano o del genoma, e allora chiamati corpi densi oppure possono mancare sia del genoma che del capside e allora sono chiamate unità non infettanti. In entrambi i casi si producono particelle che non infettano le cellule sane e quindi è il risultato dell'eccessiva sintesi di componenti virali da parte dell'elemento cellulare. Su richiesta di uno studente il professore ripete perché non si parla di gemmazione ... Non si parla di gemmazione perché il peplos non viene acquisito direttamente dalla membrana, nella gemmazione il nucleocapside nudo arriva fino alla faccia interna della membrana e gemma, spinge sulla faccia interna di membrana mentre in questo caso il nucleocapside è già dotato di peplos e accolto dalla membrana che deriva dal trafficum che si ha nel complesso del reticolo endoplasmatico o apparato di Golgi. Ciò porta a interazione di questa membrana con quella cellulare con liberazione del nucleocapside e del peplos. Si parla di egressione, non gemmazione, cioè di attraversamento quasi della membrana cellulare.
(A host immune and stress responses a C daDNA HCMV+
Effetto Citopatico e Replicazione
Caratteristiche della Replicazione
Replicazione ed effetto citopatico La replicazione ha durata maggiore (8-14 giorni) vs. altri herpesvirus. In vitro si replica soltanto in fibroblasti umani, sebbene in vivo possa essere isolato anche da altri tipi cellulari (pancreas, endotelio, ghiandole salivari, rene). L'infezione causa un caratteristico aumento volumetrico della cellula (citomegalia) con formazione di inclusioni intranucleari (classiche degli herpesvirus) e caratteristiche inclusioni citoplasmatiche ad «occhi di gufo» a significato patognomonico. Causa lesioni focali (come in VZV) perché non viene rilasciato nel mezzo colturale ma diffonde direttamente a cellule contigue. La cellula va incontro a morte per lisi. L'infezione causa un danno a carico cellulare particolare, si parla di citomegalia e infatti citomegalovirus induce aumento di dimensioni della cellula per la formazione di una serie di inclusioni nel nucleo (visto in herpes virus, herpes simplex virus) e più caratteristicamente nel citosol "a occhio di civetta" che indicano che ci sia in atto un'infezione da CMV. Il professore aggiunge che queste sono inclusioni che hanno affinità per coloranti basici e vengono colorati con Ghimsa o l'eosina. Il virus causa la morte per lisi della cellula. Per esempio in varicella zoster il virus infetta le 9 cellule sane senza riesporsi su resto delle cellule, come se attraversasse di lato gli elementi cellulari. Questo ha meccanismo che ha strategia che tende a limitare attivazione del sistema immunitario e contenimento di infezione stessa e può diffondere da una cellula all'altra in maniera più semplificata.
Esiti Clinici dell'Infezione da Citomegalovirus
Dipendenza dallo Stato Immunologico
Dal punto di vista clinico ... Gli esiti di infezione sono dipendenti dalla compromissione dell'ospite stesso.
Possibili Esiti dell'Infezione
Possibili esiti dell'infezione ASYMPTOMATIC CARRIER Mononucleosis (Heterophile Ab negative) · La possibile malattia dipende soprattutto dallo stato immunologico del paziente Normal · Ampio tropismo dovuto al riconoscimento, da parte di gB e gC, di eparan-solfato (molecola ubiquitaria) come recettore CMV Baby of seronegative mother CYTOMEGALIC INCLUSION DISEASE AIDS Immunosuppressed MULTISITE SYMPTOMATIC DISEASE Mosby, Inc. items and derived items copyright 2002 by Mosby, Inc.
Gli individui che abitano paesi industrializzati (80%) è venuto a contatto con virus che di norma non si manifesta clinicamente se c'è sistema immunitario che lavori. In una piccola parte si possono avere esiti quando c'è una compromissione di sistema immunitario come terapia immunosoppressiva o malati di AIDS, si ha disseminazione di malattia e compare un quadro clinico che interesserà organi come occhi, fegato, colon, stomaco e anche l'esofago. La sieropositività di CMV in Italia si attesta intorno a 70-80% e l'ampia varietà dei tipi cellulari che viene interessata dall'infezione stessa è determinata da fatto che CMV si lega alle eparan solfatiche che troviamo sulla superfice di tanti tipi cellulari, ce tropismo a livello cellulare. Effetto citopatico deriva dalla replicazione del virus nelle cellule e la replicazione è più lenta, la durata arriva fino 10-14 giorni e determina periodo di incubazione lungo, anche di mesi. Si replica in vitro in laboratorio nei fibroblasti umani e in vivo da campioni biottici si è visto che può essere correlato ad altri tipi cellulari (pancreas, endotelio, ghiandole salivari, rene).
B