Ammine: classificazione e basicità dei composti organici in Chimica
Slide sulle Ammine, composti organici fondamentali in biologia e farmacia. Il Pdf illustra la classificazione e le proprietà di basicità delle ammine, distinguendo tra alchilammine e arilammine. Questo materiale di Chimica per l'Università è utile per lo studio autonomo grazie a spiegazioni chiare e schemi visivi.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
AMMINE
Nel mondo biologico l'azoto è ampiamente diffuso, infatti costituisce il quarto elemento nei composti organici, dopo C, H, e O. Il DNA, le proteine e più del 75% dei farmaci in commercio contengono azoto, di solito sotto forma di gruppo funzionale amminico. Le ammine sono considerate derivati organici dell'ammoniaca e come questa hanno un atomo di azoto con una coppia solitaria che le rende basiche e nucleofile.
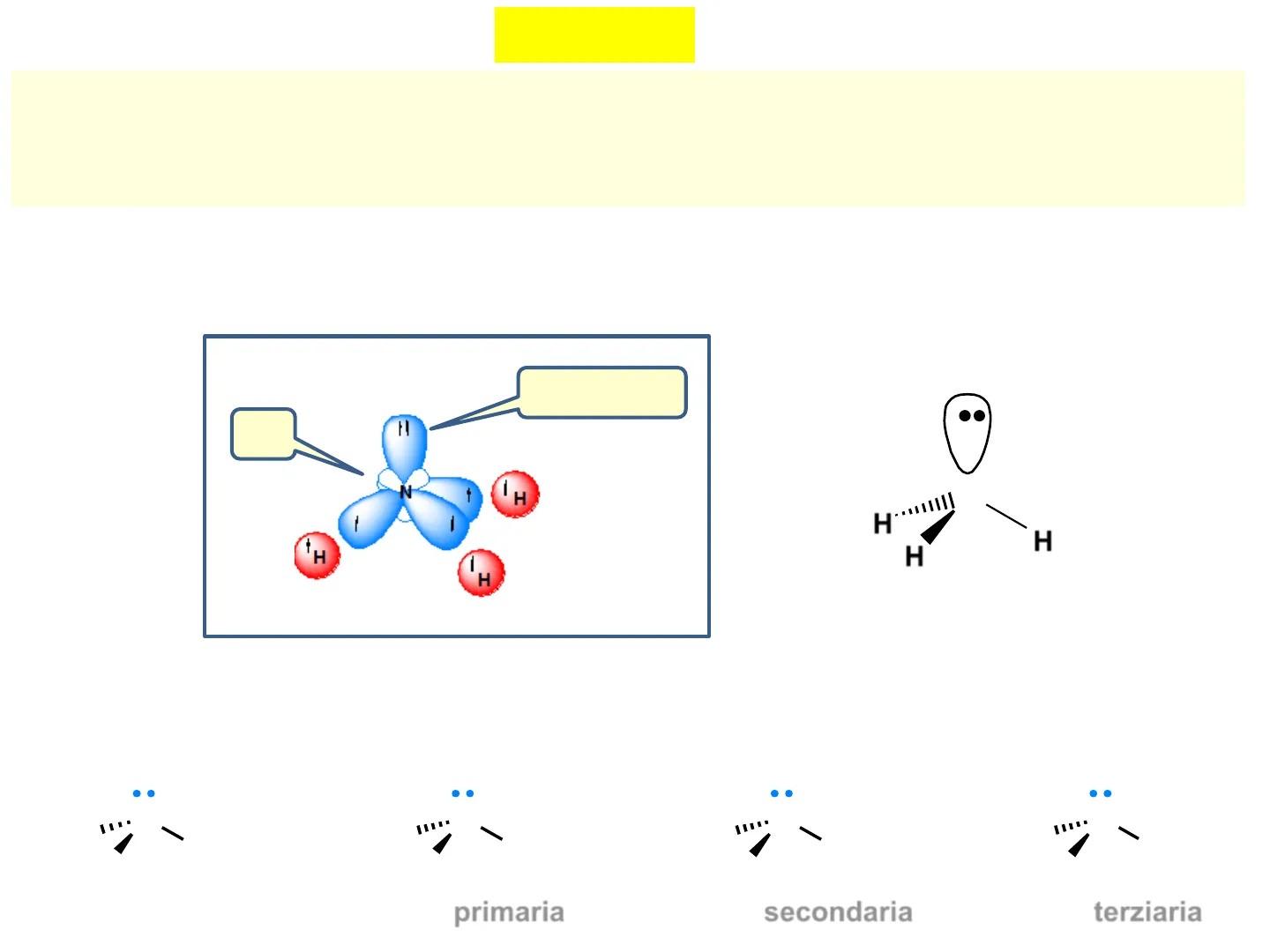
Coppia solitaria sp3
N + H N H· H H İ H ammoniaca
Classificazione: in base al numero di gruppi alchilici legati all'azoto
N ... N H' H H ammoniaca ammina primaria ammina secondaria R .. N R R H H H R N R R ammina terziaria .
AMMINE: nomenclatura
- Il nome comune delle ammine primarie si ottiene aggiungendo il suffisso -ammina al nome del gruppo alchilico (senza -e della desinenza -ile) legato all'azoto. Il nome IUPAC si ottiene sostituendo il suffisso -ammina alla -o finale dell'alcano progenitore.
CH3NH2 nome IUPAC metanammina (metilammina)
1 nome comune
NH2 2-metil-1-propanammina (isobutilammina)
NH2 H3C H3C 4,4-dimetilcicloesanammina
H2NCH2CH2CH2CH 2NH2 1,4-Butandiammina
AMMINE: nomenclatura
- Se nella struttura sono presenti gruppi funzionali a priorità più alta nella nomenclatura, il gruppo - NH2 si considera come un sostituente ammino legato alla molecola di riferimento.
NH2 I CH3CH2CHCO2H 4 3 2 1 3 0 H2NCH 2CH2CCH3 4 21 Acido 2-amminobutanoico 4-ammino-2-butanone
Ordine di priorità dei gruppi funzionali nella nomenclatura
Priorità Classe di composto Formula gruppo funzionale Nome sostituente Suffisso
1 Acido carbossilico -COOH carbossi- Acido ... -oico
2 Aldeide -CHO formil- -ale
3 Chetone -COR acil- -one
4 Alcol -OH idrossi- -olo
5 Ammina -NH2, -NHR, -NR2 ammino- alchilammino- -ammina -alchilammina
6 Eteri Solfuri Tioli -OR -SR -SH acossi- alchiltio- mercapto- -alchiletere -alchisolfuro -tiolo
7 Alchino C=C alchinil- -ino
8 Alchene C=C alchenil -ene
9 Alogenuro -X fluoro- cloro- bromo- iodo-
10 Alcano C-C alchil- -ano
AMMINE: nomenclatura
- Le ammine secondarie e terziarie con gli stessi sostituenti legati all'azoto si denominano utilizzando i prefissi di- o tri -.
H 1 N Difenilammina
CH3CH2-N-CH2CH3 I CH2CH3 Trietilammina
- Le ammine secondarie e terziarie con sostituenti diversi legati all'azoto si considerano ammine primarie N-sostituite. Nel nome IUPAC la radice del nome è data dall'ammina primaria che reca il gruppo con più atomi di carbonio.
CH3 N-CH2CH 2CH3 / CH3 N,N-Dimetil-1-propanammina N,N-Dimetilpropilammina
H3C CH 2CH3 N N-Etil-N-metilcicloesanammina N-Etil-N-metilcicloesilammina
AMMINE: nomenclatura
- Le ammine eterocicliche, composti in cui l'azoto sostituisce un atomo di carbonio dell'anello, sono molto diffuse e hanno tutte nomi comuni
4 3 2 N 1 Piridina
4 3 5 N 6 2 N 1 Pirimidina
5 4 6 3 7 2 N 8 1 Chinolina
3 2 N 1 H Pirrolo
4 3 N 1 5 2 N 1 H Imidazolo
4 3 5 2 6 N 1 7 H Indolo
4 3 2 N 1 H H Piperidina Pirrolidina 3 2 N 1
AMMINE: proprietà
Punti di ebollizione delle ammine
Le ammine primarie e secondarie formano legami idrogeno, perciò presentano punti di ebollizione più alti dei corrispondenti alcani a parità di peso molecolare:
R' R R' R 1 1 8+ 8+ .N~ N 8- H H H. H N ·N / 1 R R' R R' R R' p.e. 36℃ p.e. 56°℃ N H 8-
AMMINE: proprietà
Solubilità delle ammine
Come gli alcoli, le ammine con meno di cinque atomi di carbonio sono solubili in acqua
O H H. R-N i - H R-N. H TH -H O H H La solubilità diminuisce all'aumentare della lunghezza della catena carboniosa
I legami idrogeno che le ammine formano con H2O sono meno forti di quelli che si instaurano tra gruppi ossidrilici O-H
AMMINE: basicità
Basicità di alcune ammine comuni
Nome Struttura pKa ione ammonio
Ammoniaca NH3 9.26
Alchilammina primaria Metilammina Etilammina CH3NH2 CH3CH2NH2 10.64 10.75
Alchilammina secondaria Dietilammina (CH3CH2)2NH 10.98 11.27
Pirrolidina NH
Alchilammina terziaria Trietilammina (CH3CH2)3N 10.76
Arilammina 4.63
Anilina NH2
AMMINE: basicità
Come l'ammoniaca, le ammine sono basi deboli e le soluzioni acquose delle ammine sono basiche. Le alchilammine sono basi più forti dell'ammoniaca. Questo perché gruppi alchilici elettron donatori rendono il doppietto elettronico dell'azoto più disponibile; inoltre i gruppi alchilici elettron donatori stabilizzano lo ione alchilammonio che si forma nella reazione acido-base, stabilizzando la sua carica positiva
H N + O R H H H H 1 H 1 H Rende il doppietto elettronico dell'azoto più disponibile Stabilizza lo ione alchilammonio disperdendo la carica positiva + :OH R N +
ARILAMMINE: basicità
Le arilammine sono meno basiche delle alchilammine: la coppia elettronica dell'azoto è delocalizzata per risonanza sull'anello aromatico ed è quindi meno disponibile a legare un H+.
: NH2 NH3+ H+ Anilina (elettroni delocalizzati) Ione anilinio (carica positiva localizzata)
: NH2 : NH2 + NH2 + NH2 + NH2 € > € 1 > I > > 1
ARILAMMINE: basicità
Basicità aniline p-sostituite
Y NH2 + H2O ₹ Y + NH3 + -OH pKa ione anilinio Base più forte
-NH2 6.15
-OCH3 5.34 Gruppi elettron donatori
-CH3 5.08
-H 4.63
-CI 3.98
-Br 3.86 Gruppi elettron attrattori
-CN 1.74
-NO2 1.00 - Base più debole
Confronto basicità delle ammine e delle ammidi
Le ammidi (pKa ~ 0,5) sono molto meno basiche sia delle alchilammine che delle arilammine: il doppietto elettronico dell'azoto è stabilizzato mediante sovrapposizione orbitalica con il gruppo carbonilico ed è quindi poco disponibile ad accettare un H+.
Atomo di azoto ricco di elettroni H 1 N H3C H :0: Atomo di azoto povero di elettroni -C H HC CZ-I 1 :0: 1 .C. + H H3C N 1 H
Ammine ETEROCICLICHE
Le ammine eterocicliche sono molto diffuse e presentano importanti proprietà biologiche
NH2 OH NH2 OH H3C. N N N N N ZI N N N N `OH N OH H Adenina Guanina Citosina Timina DNA
Ammine ETEROCICLICHE
La piridina
La piridina è l'analogo eterociclico azotato del benzene. La sua struttura è simile a quella del benzene: sia i cinque atomi di carbonio che l'azoto sono ibridati sp2 e contribuiscono con un elettone it al sestetto elettronico. Gli elettroni della coppia solitaria occupano un orbitale sp2 che giace sul piano.
Orbitale sp2 Orbitale sp3 - N N N H3C'' CH3 H3C La piridina è meno basica delle alchilamnine. La minore basicità è dovuta al fatto che la coppia solitaria occupa un orbitale sp2 ed è quindi meno disponibile ad essere ceduta rispetto alla coppia solitaria di un alchil ammina su orbitale sp3.
Ammine ETEROCICLICHE
Il pirrolo
Il pirrolo possiede sei elettroni T ed è aromatico. L'azoto ibrido sp2 contribuisce con 2 elettroni dell'orbitale p non ibridato.
N-H Coppia solitaria in un orbitale p H H N-H H Ibridato sp2 H L'atomo di azoto del pirrolo è meno ricco di elettroni e quindi meno nucleofilo di un ammina alifatica. A differenze delle altre ammine non è basico (pKa = 0.4). Questo perché la protonazione dell'azoto distruggerebbe l'aromaticità dell'anello.
> + "OH + N 1 H H Pirrolo + H2O :Z-I Ione pirrolidinio (pKa = 0.4)
Alberto Cavaliere
CHIMICA IN VERSI
PIPE PASTILLATE Asgeo Signorelli-Edmure Rama
Alberto Cavaliere La chimica in versi
CHIMICA ORGANICA
Per concludere sorridendo ...
IL CORPO UMANO
Ecco un'analisi non troppo amena, che ha fatto un màcabro dottore a Jena:
Da tutto il fosforo, piedi compresi, al più ci scappano mille svedesi,
mentre distillasi dal corpo vile d'acqua ... potabile tutto un barile.
Il ferro è in minime tracce, di modo che non ci fabbrichi neppure un chiodo:
Volendo vendere questi elementi ai poco modici prezzi correnti,
ci si ricavano venti lirette: alcune scatole di sigarette!
Che cifra misera! Solo conforto, se si considera che l'uomo morto,
oscuro o celebre, ricco o pezzente, sciocco o filosofo, vale ugualmente.
Ed è ridicolo, in fondo in fondo, che, mentre vivono su questo mondo,
sia dian cert'arie tanti mortali, se poi gli scheletri son tutti uguali!
e si ricupera tanta grafite da far al massimo cento matite
I grassi abbondano - strano contrasto! - pure in chi è solito saltare il pasto.
fatto stranissimo perché da vivi di chiodi, in genere, non siamo privi.
Ma ciò che supera le previsioni più catastrofiche sono i bottoni;
ne ottieni un numero fenomenale, sì che un legittimo dubbio t'assale:
fece l'analisi quell'alchimista sopra lo scheletro d'un giornalista?
preso un cadavere, l'ha decomposto, con molto scrupolo stimando il costo.
L'ossa forniscono tanta calcina dal far l'intonaco d'una cucina,