L'acqua: una molecola speciale e le sue proprietà chimiche
Slide sull'acqua, una molecola speciale. Il Pdf esplora le caratteristiche fondamentali dell'acqua, la sua ionizzazione e la scala del pH, con esempi pratici. Questo documento di Chimica per la Scuola superiore è ideale per l'apprendimento autonomo.
Mostra di più20 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
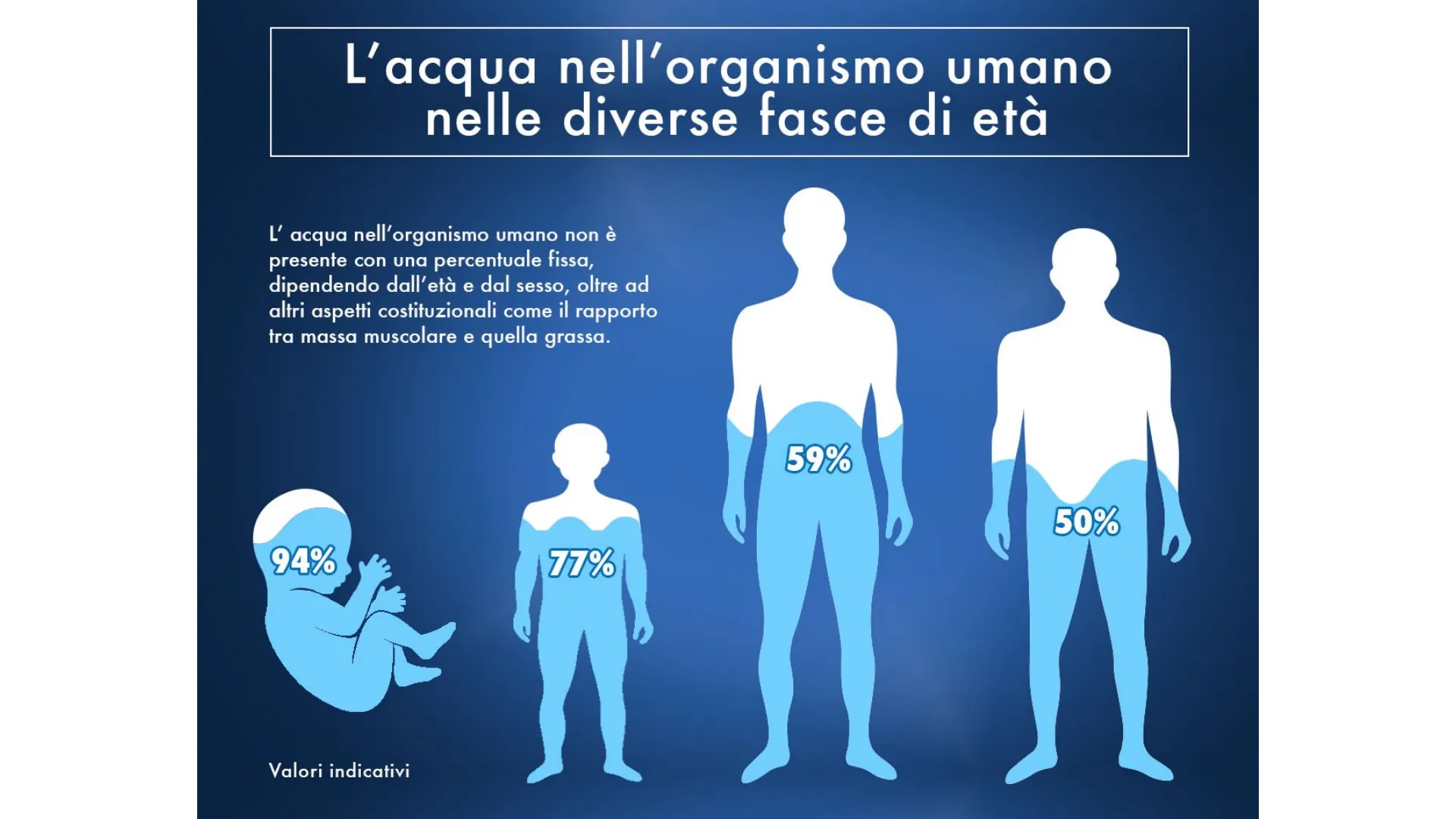
L'acqua nell'organismo umano
L'acqua nell'organismo umano non è presente con una percentuale fissa, dipendendo dall'età e dal sesso, oltre ad altri aspetti costituzionali come il rapporto tra massa muscolare e quella grassa.
59% 50% 94% 77% Valori indicativi35% solidi O Il liquido extracellulare comprende tutti i fluidi esterni alle cellule. Oltre al plasma e al liquido interstiziale, una piccola quantità di acqua è presente all'interno di alcuni organi, come l'occhio e il sistema nervoso centrale. liquidi corporei 1 2/3 liquido intracellulare 65% liquidi liquido extracellulare 1/3 liquido extracellulare 80% liquido interstiziale 20% plasma
La distribuzione delle acque dolci e salate
Nel suo complesso l'idrosfera copre oltre i 2/3 della superficie terrestre. Circa il 96% dell'idrosfera è costituito dalle acque salate che formano mari e oceani. Le acque dolci (circa l'4%) sono raccolte in cinque grandi serbatoi:
- ghiacciai;
- corsi d'acqua;
- laghi;
- acque sotterranee;
- forma gassosa (0,001%).
ghiacciai e calotte polari 68% falde idriche 30% laghi e fiumi 0,02% acque dolci 2,8% atmosfera 0,001% oceani e mari 96,7%
Gli stati dell'acqua
Solido Liquido Gassoso Fusione Riscaldamento Evaporazione Ghiaccio 0℃ 100°℃ 0℃ - 100°℃ Vapore Congelamento Raffreddamento Condensazione L'acqua è l'unica sostanza che è presente naturalmente sulla Terra in tutti e tre i suoi stati di aggregazione (solido, liquido, gassoso).
La molecola dell'acqua a livello chimico
- La molecola dell'acqua è formata da due atomi di H (idrogeno) e uno di O (ossigeno), H2O. La disposizione degli atomi nello spazio ricorda una V con un angolo di 104,5°.
- Gli atomi di H sono legati all'atomo di O mediante un legame covalente.
8 0 1 8+ H H 104.45°
La molecola dell'acqua è polare
- La polarità di una molecola dipende non soltanto dalla presenza di legami covalenti polari ma anche dalla geometria della molecola, cioè dalla disposizione nello spazio dei suoi legami.
- Nella molecola d'acqua si verifica una distribuzione asimmetrica della carica elettrica e ciò rende la molecola nel suo insieme una molecola polare o dipolo.
1 11 O + H H + + + + + + + 8+
Legame idrogeno
- Legame debole di natura elettrostatica che coinvolge l'idrogeno legato covalentemente ad un atomo fortemente elettronegativo come F, O, N.
- Ogni molecola d'acqua può formare 4 legami idrogeno.
8- ô+ I- O ô+ · · · ô- H 8+ . . 6- 6+ · . Legami a idrogeno
Legami a idrogeno
H 8+ 8 H 8+ 8+ 8+ H H 8 legame a idrogeno I legami a idrogeno fanno sì che tutte le mole- cole d'acqua siano legate tra loro da legami inter- molecolari. Una singola molecola d'acqua può for- mare fino a 4 legami a idrogeno con altre molecole d'acqua. ossigeno idrogeno E·I legame a idrogeno I -O (+) ... (-) H (+) ... (-) legame a idrogeno E ... I idrogeno ossigeno O
Le proprietà dell'acqua
- TENSIONE SUPERFICIALE (Forze di coesione)
- CAPILLARITA' (Forze di adesione)
- SOLVENTE UNIVERSALE
- CALORE SPECIFICO
- DENSITÀ D
La coesione e l'adesione
- La COESIONE: indica la capacità delle molecole d'acqua di aggregarsi in gocce (grazie ai legami idrogeno);
- L'ADESIONE: indica la capacità delle gocce d'acqua di rimanere "attaccate" alla superficie verticale di un contenitore (ad es. una provetta) senza scivolare via.
- Per questo motivo, l'acqua è un eccellente mezzo di trasporto per i nutrienti e le sostanze di rifiuto.
Adesione Coesione Adesione H H 0 0 Vetro
Tensione superficiale
- Proprietà che determina la sfericità delle gocce d'acqua e la formazione sulla sua superficie di una pellicola elastica invisibile.
- FORZE DI COESIONE!
- https://www.youtube.com/watch?v=kjJhWyBzWVU Figura 2 - Schema delle forze di attrazione fra le molecole di un liquido. Le molecole interne sono in equilibrio fra loro. Le forze che agiscono sulle molecole di superficie non sono invece equilibrate verso l'alto e da ciò risulta una compressione verso l'interno. Inoltre, la coesione fra le molecole determina una tensione tangenziale alla superficie. La su- perficie di un liquido si comporta quindi come una membrana elastica.
Capillarità
- Capacità dell'acqua di risalire in tubi molto sottili (capillari).
- FORZE DI ADESIONE!
- https://www.youtube.com/watch?v=xsm2grsOxn0
vetro H2O 2 Hg molecola d'acqua Prodetti della foll stato liquido Acqua e soli mineral
Solvente universale
- Grazie alla sua polarità, l'acqua è un buon solvente. È infatti in grado di sciogliere altre sostanze polari.
- Non è un solvente per le sostanze apolari (grassi, benzina, ecc.).
- Le molecole idrofile, come il sale, attirano l'acqua.
- Le molecole idrofobiche, invece, non attraggono l'acqua.
O H H H H 0 Na" CI- H H H H O O O 0 H H H H Un sale ionico, NaCl (Cloruro di sodio) in acqua si scioglie (le linee punteggiate indicano i legami a idrogeno).
Calore specifico
- Quantità di energia che occorre fornire a un kilogrammo di una sostanza per innalzare di 1° C la sua temperatura.
- L'acqua possiede un'elevata capacità termica grazie ai legami idrogeno. Questo le permette di ridurre gli sbalzi termici, proteggendo gli organismi dai cambiamenti termici repentini.
- suo elevato calore di vaporizzazione permette agli animali di perdere calore attraverso la sudorazione, evitando il surriscaldamento.
La densità
- L'acqua e il ghiaccio hanno densità diverse.
- A causa della sua struttura cristallina l'acqua in forma solida è meno densa di quella in forma liquida. Ciò permette al ghiaccio di galleggiare sull'acqua.
- Questa proprietà ha implicazioni importanti per la vita. Per esempio, la superficie ghiacciata di uno stagno consente agli organismi di sopravvivere nell'ambiente sottostante.
5Il ghiaccio è meno denso dell'acqua Acqua gassosa (vapore) Acqua solida (ghiaccio) Nel ghiaccio, le molecole d'acqua sono mantenute in uno stato rigido grazie ai legami a idrogeno. Nel suo stato gassoso, l'acqua non forma legami a idrogeno. I legami a idrogeno si rompono e si riformano continuamente col movimento delle molecole d'acqua. ZANICHELLI Sadava et al. La nuova biologia.blu PLUS @ Zanichelli 2016 Acqua liquida 6
La ionizzazione dell'acqua
- La reazione dei ionizzazione dell'acqua è una reazione acido-base in cui la formazione degli ioni avviene per scambio di un protone fra due molecole d'acqua.
H2O(1) + H2O(0) } H3O+ (aq) + OH (aq) acqua ione ione idronio idrossido
Acidi e basi
Livelli di pH
Acido Basico 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Neutro INTECH-CR scala del pH 0 H3O+ H3O+ OH- H3O+ - 1 soluzione acida 2 succo gastrico succo di limone H3O+ H2O+ OH - 3 aceto H3O+ - 4 succo di pomodoro - 5 pelle umana urina H3O+ OH- soluzione neutra neutralità OH- H3O [H3O+]=[OH-] 7 acqua pura sangue umano OH- 8 acqua di mare H3O+ 9 sapone 10 OH- OH OH soluzione basica OH 12 OH candeggina per uso domestico OH- OH H3O+ OH- 13 14 H3O+ OH H2O+ OH- 11 ammoniaca per uso domestico H3O H2O+ H2O+
Scala pH
Batteria Limone Pomodoro Latte Sangue Pastiglie antiacido Sapone Drenante per tubature 012 3 4 5 6 7 8 9 10 11 12 13|14 Drink Coca-Cola Delicious asd Refreshing Succo gastrico Aceto Caffè Acqua Bicarbonato di sodio Ammoniaca Candeggina ACIDO NEUTRO ALCALINO