Immunologia: il sistema del complemento e le sue patologie
Documento dall'Università sull'immunologia. Il Pdf esplora il sistema del complemento, un componente cruciale dell'immunità, dettagliando le vie di attivazione classica e della lectina. Il Pdf di Biologia è utile per lo studio autonomo, fornendo spiegazioni dettagliate sui meccanismi immunologici.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Immunologia del sistema del complemento
Il sistema del complemento è definito come un sistema di circa 30 enzimi che si attivano in sequenza, una cascata proteolitica in cui ogni componente è attivato dal componente immediatamente a monte. In ogni step di questa cascata c'è un'amplificazione, quindi un aumento degli effetti che vanno perciò finemente regolati.
Si identificano tre sistemi di attivazione del complemento:
- La via classica attivata ogni qualvolta un IgG o un IgM incontra l'antigene, formando un immunocomplesso.
- La via della lectina si attiva quando la lectina, una proteina plasmatica, incontra residui di mannosio.
- La via alternativa si può attivare in momenti diversi
L'attivazione del complemento ha un effetto citotossico diretto, ma anche un'azione opsonizzante che consiste nel potenziamento della fagocitosi. Altre funzioni in cui è coinvolto il sistema del complemento sono legate alle risposte infiammatorie.
Via classica
C1q inhibitor (C1 INH) interferes with the enzymatic activation of C1r2s2 C1q binds to antigen- complexed antibodies, resulting in activation of C1r2S2 C1 INH prevents C1r2S2 from becoming proteolytically active Il primo elemento della via classica è detto il complesso del C1, dove abbiamo tre subunità C1q, C1s, C1r. Il C1q è un esamero, ognuna delle teste globulari di C1q riconosce un sito della B C1q -C1 INH regione costante o delle IgG o delle IgM. Il Antibody C1r2S2 C1r2S2 requisito è che almeno due delle teste globulari del C1q prendano contatto con due regioni Fc di IgG o IgM legate ad antigeni, permettendo di costituire un complesso enzimaticamente attivo. Il C1q a questo punto si unisce a un dimero C1r e un dimero C1s. Quando un antigene incontra una IgM o IgG queste vanno incontro a cambio conformazionale. Questo è fondamentale per farsi riconoscere dal complesso C1. Le IgM hanno struttura pentamerica, quindi offrono cinque regioni costanti agli antigeni ed è più facile che avvenga il legame; mentre nel caso si abbiano IgG ne servono almeno due per ottenere il numero necessario di legami del complesso immunglobulina-antigene con le teste globulari di C1q. Le IgM sono quindi la classe immunoglobulinica più efficiente nell'attivare il complemento.
I substrati del complesso C1 sono il C2 e il C4, ognuno dei due viene tagliato in due pezzi: il C4 è tagliato in C4a e C4b, mentre il C2 subisce il taglio da parte di C1 dopo essersi legato a C4b ed è diviso in C2a e C2b. Questo porta alla formazione di un secondo complesso enzimaticamente attivo. Ogni volta che un componente del complemento agisce sul successivo come proteasi i due pezzi che risultano sono detti a e b. Solitamente il componente a è il più piccolo e diffonde, mentre il componente b si stabilizza.
Il C4 in uno delle sue tre catene presenta un ponte tioesterico molto fragile. Quando il C4 è integro questo legame è nascosto all'interno del trimero, ma a seguito del taglio il C4b subisce uncambiamento conformazionale per cui il legame tioesterico labile è esposto e si rompe. Si presentano quindi due estremità altamente reattive che devono immediatamente legarsi a qualcosa quindi il C4b non ha il tempo di allontanarsi. In alcuni casi può accadere che il C4b con il legame tioesterico rotto è saturato con una molecola d'acqua, questo però porta alla formazione di un C4b inattivo che blocca la cascata del complemento.
La cascata del complemento è strettamente regolata, infatti già in queste prime fasi si incontra l'inibitore del C1, che inibisce l'attivazione del complesso C1r2s2. Questo funziona da pseudosubstrato per C1r2s2 legandosi ai siti catalitici bloccando il C1r e il C1s. L'inibitore del C1 è plasmatico quindi modula negativamente dall'inizio la partenza della cascata.
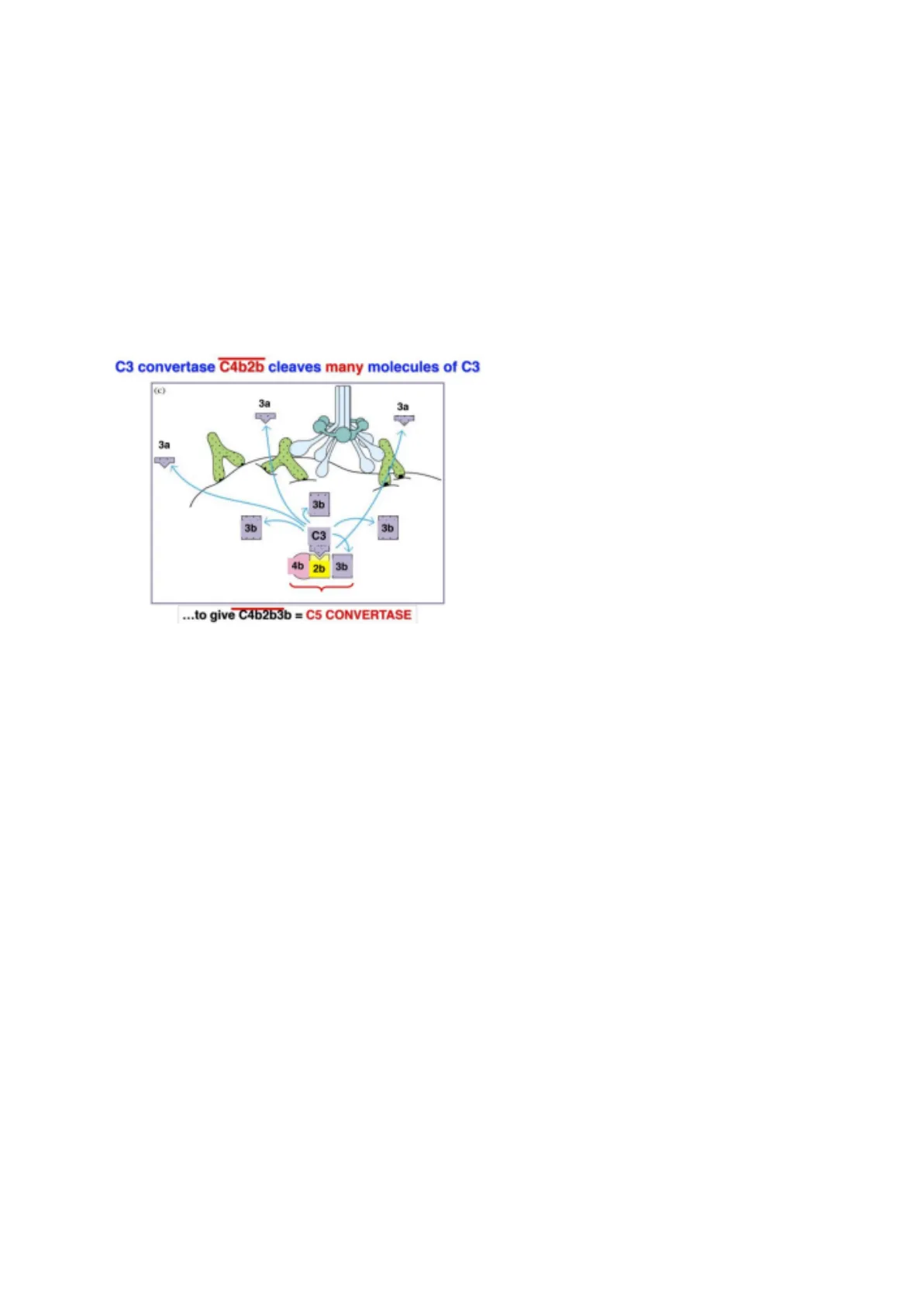
C3 convertase C4b2b cleaves many molecules of C3 Il complesso C4b2b costituisce la C3 convertasi (c) 3a che si occupa di tagliare il C3. Il C3 è il 3a componente della cascata del complemento più abbondante in circolo, anche qui con 3a l'azione della convertasi si ha un taglio e la conseguente costituzione di due componenti .. 3b C3a e C3b. Il C3a diffonde mentre il C3b 3b 3b C3 stabilisce legame covalente nelle vicinanze della c3 convertasi che lo ha generato. Si osserva un 4b 2b 3b legame labile, in questo caso un legame ... to give C4b2b3b = C5 CONVERTASE esterico rotto che può essere o saturato da una molecola d'acqua (si ferma la prosecuzione della cascata) oppure si va ad attaccare un nuovo legame covalente con le vicinanze. A seguire si costituisce un nuovo complesso enzimaticamente attivo costituito da C4b2b3b, ovvero la C5 convertasi. Attraverso questo meccanismo di rottura e riformazione dei legami labili è possibile localizzare in un luogo preciso la prosecuzione della cascata proteolitica sebbene si tratti di molecole plasmatiche (in circolo). A livello della C3 convertasi abbiamo altri meccanismi di regolazione: si osservano degli inibitori di membrana che si trovano sulla superficie delle nostre cellule e sono noti come DAF (decay accelerating factor), MCP e CR1. Insieme costituiscono una protezione da un'aberrante attivazione del complemento. È presente, inoltre, un inibitore solubile (plasmatico), ovvero la C4 binding protein. Tutti però inducono la dissociazione nella C3 convertasi di C4b e 2b. Inoltre, C4BP, CR1 e MCP hanno anche un meccanismo di associazione alla convertasi e di degradazione del C4b e del C3b da parte di una proteasi plasmatica detta fattore i bloccando la cascata del complemento.
Siamo quindi giunti alla formazione della C5 convertasi nella via classica, a cui segue un tronco comune a tutte e tre le vie del complemento. Si analizzano prima di procedere con il tronco comune le prime fasi delle altre due vie di attivazione del complemento.
Via della lectina
Inizia da una proteina plasmatica definita lectina legante il mannosio che assomiglia molto al C1. E' costituita infatti da sei subunità, che sono quelle che nelle teste globulari sono in grado di legare il mannosio, associate a due proteasi, MASP I e MASP II (presenti come zimogeni), che fanno le veci di C1r e C1s. In che modo quindi si attiverà la via della lectina? Si attiva quando le teste globularitrovano più residui di mannosio ad alta densità (quindi devono essere coinvolte molte teste) con cambiamento conformazionale che porta ad accensione delle MASP il cui substrato è il C4 e il C2. Di fatto quello che differenzia le due vie è l'INIZIATORE. La lectina legante il mannosio è una PRR che fa parte di un gruppo di proteine definite "Proteine della fase acuta" che rappresentano uno dei meccanismi di difesa dell'immunità innata perché sono proteine plasmatiche la cui concentrazione aumenta rapidamente durante le prime fasi dell'infezione (solitamente scarsamente presenti). Con l'aumento delle proteine della fase acuta l'organismo si prepara ad una risposta sistemica sentendo il patogeno. Di conseguenza non solo la Lectina legante il mannosio è in grado di attivare il complemento ma anche tutte le proteine della stessa famiglia attraverso meccanismi meno chiari e complicati. Di conseguenza non solo la Lectina legante il mannosio è in grado di attivare il complemento ma anche tutte le proteine della stessa famiglia (Ad es. La proteina C. Infatti, queste proteine sono in grado di attivare la via classica grazie all'attivazione di C1. Rappresentano un innalzamento del livello di sorveglianza sistemica quando abbiamo un'infiammazione anche locale. Questo perché l'organismo si prepara alla possibilità che l'infezione non si risolva localmente ed il patogeno invada il torrente circolatorio e quindi abbia più possibilità di invadere i tessuti, aumentando il livello di sorveglianza.
Via alternativa
La via alternativa richiede un cambiamento concettuale. Lo schema delle prime due vede una cascata inizialmente ferma che viene attivata da qualcosa captato da un sensore che attiva la cascata. La via alternativa parte da un evento completamente casuale definito fenomeno del tickover del C3 (ricordiamo che il C3 presenta un legame metastabile che, quando intero è sepolto all'interno della molecola). Normalmente, con una probabilità bassa, un piccolo numero delle molecole del C3 va incontro a questo processo di rottura del ponte labile casuale non dovuta all'attivazione della cascata. Potrà di conseguenza legarsi con qualsiasi cosa, tra cui proteine sulla superficie di un globulo rosso o molecole di acqua. Quest'ultime verranno definite C3H20 per indicare che è un C3 che nessuno ha tagliato in due ma in cui spontaneamente si è rotto il ponte e sempre spontaneamente si è legato ad una molecola d'acqua con associazione del Fattore B. Quando questo fattore si associa non covalentemente al C3H2O, può essere tagliato da una proteasi plasmatica che si chiama Fattore D. Finché il Fattore B è da solo NON potrà essere tagliato. Si generano quindi due frammenti, un C3H2O-Ba che diffonde e un C3H2O-Bb che è una C3 convertasi in fase fluida (molecola non ancorata da nessuna parte).
Ca undergoes spontaneous hydroly- sis to C3(H;O) which binds to factor B allowing it to be chaved by factor D into Ba and Bb factorD lastor !! C3(H,O) The CHH,O|Bb Complex is a C3 Convertase, clairving more C3 into C3a and C3b. C3b is rapidly Inacti- waled unless it binch to cell surface Perché questa appena descritta, ovvero C3(H2O)Bb, è chiamata C3 convertasi in fase fluida? Perché è una C3 convertasi che "viaggia/naviga" e non è ancorata da nessuna parte.
La via alternativa può avere anche un altro inizio. Precedentemente si è visto che la via aveva inizio da un evento casuale, ovvero il tickover del C3, ma ci può essere un'altra situazione che da inizio alla via alternativa: ogni volta che si genera una molecola di C3b (che può venire dalla via classica, da quella della lectina o dalla C3 convertasi in fase fluida), il fattore B gli si associa. Come si è visto precedentemente per il C3(H2O), viene tagliato in due dal fattore D, generando unframmento più grande Bb, che rimane associato a C3b, e un frammento più piccolo, cioè Ba, che diffonde. Il complesso C3bBb è la C3 convertasi della via alternativa in fase solida, ovvero immobilizzata da qualche parte. In particolare, è immobilizzato dove si era immobilizzato il C3b che ha scatenato la sua formazione.
Essendo una C3 convertasi, taglia, poi, nuove molecole di C3 in C3a e C3b, generando i frammenti piccoli C3a, che diffondono, e frammenti grandi, che invece si depositano nelle immediate vicinanze. Dato che C3 è il componente più abbondante del complemento nel plasma, ogni molecola di C3 convertasi processerà tante molecole di C3 e genererà tante molecole di C3b. Ognuna delle molecole di C3b generate ricomincia il giro, cioè si associa a una molecola di fattore B, viene tagliato in Ba e Bb e genera una nuova molecola di C3 convertasi.
Loop di amplificazione della via alternativa
amplification loop C3b from classical or lectin pathway convertases, or from alternative pathway convertases (2) C3b binds factor B Bound factor B is cleaved by plasma protease factor D into Ba and Bb ClbBb complex is a C3 convertase, cleaving many C3 molecules to CJa and C3b factor B factor D Ba Cja Bb CBbBb C3b P C3b La formazione della C3 convertasi nella via alternativa porta a un grande loop di amplificazione, perché la C3 convertasi genera il C3b e ogni molecola di C3b può creare una nuova molecola di convertasi, che, a sua volta, taglierà altre molecole di C3 e genererà altre C3b.
Questo è il motivo per cui consideriamo la via alternativa una via di amplificazione del sistema del complemento.
La via alternativa non va considerata, quindi, come una via direzionale (come la via classica e quella della lectina, in cui si parte da un evento preciso e si sviluppa una cascata), ma è una via che si può attivare addirittura per un evento casuale e serve come via di amplificazione delle altre due vie, perché utilizza il C3b formato da qualunque via per generare nuove C3 convertasi e, quindi, nuovo C3b sulle superfici dove quest'ultimo si è fermato.
Le molecole di C3 convertasi che si formano funzionano enzimaticamente (cioè tagliano nuovo C3) finché le sue due subunità rimangono insieme (C3bBb). Esistono proteine, come la properdina, che Dangerous nonself Pathogens Altered or dangerous self Apoptotic, necrotk. and malignant cells C3 convertase stabilization B C3 CJa Bacteria Viruses B CI Cla C30H4,01 C30H MI nb C3b Cb Cab CJb 5b P Danger recognition Properdin Alternative pathway promotion stabilizzano la C3 convertasi. La properdina è una proteina plasmatica che si avvicina alla C3 convertasi e la stabilizza, ovvero la fa durare di più: finché dura, essa taglia nuovo C3 e genera nuovo C3b.
In quali condizioni la properdina si avvicina alla C3 convertasi e la stabilizza?
La properdina ha la capacità di legarsi alla C3 convertasi della via alternativa su alcune superfici (e non su altre), esse sono:
- Superfici microbiche se il complemento si sta attivando su una superficie microbica le sue caratteristiche chimico-fisiche favoriscono l'arrivo della properdina, la sua associazione alla C3 convertasi e il prolungamento dell'emivita della C3 convertasi
Debris